引言
肾脏类器官作为模拟人类肾脏发育和疾病的强大工具,其发展始终面临两大核心瓶颈:结构无序(缺乏肾单位-集合管连接)和功能不成熟。近日,南加州大学的Zhongwei Li团队及其合作者在 Cell Stem Cell发表的最新研究中,通过开发一种具有一定生理功能的高阶肾脏类器官(Kidney Progenitor Assembloid, KPA)平台,为解决这些难题提供了极具开创性的方案。该研究不仅成功构建了具有空间构型和高级功能的肾脏组织,更在体内高保真地模拟了多囊肾病(ADPKD)的复杂病理微环境,为肾脏疾病研究和再生医学设立了新的标杆。
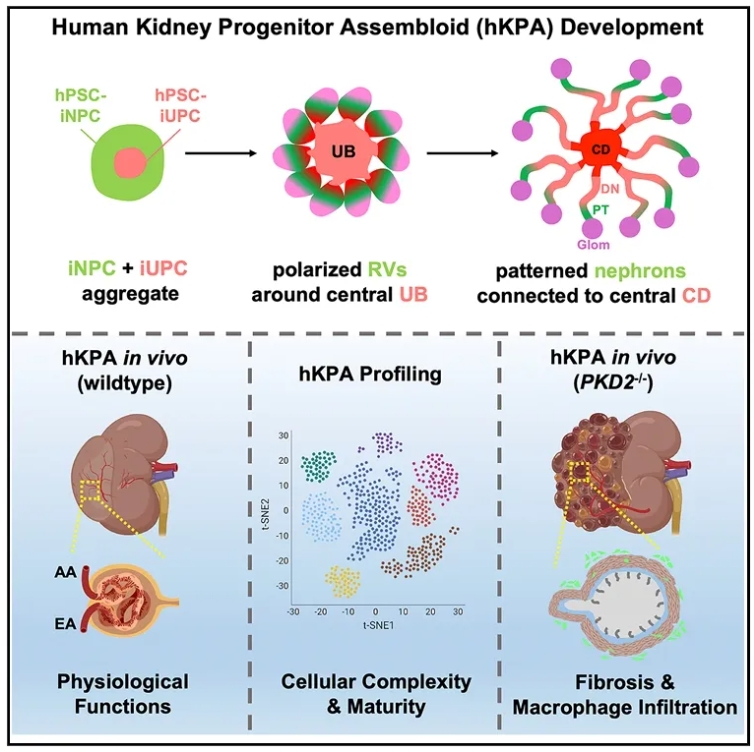
图形摘要:通过共培养两种肾脏祖细胞,构建出具有空间构型的肾脏组装体,并用于高保真疾病模拟。
文章亮点
1. 方法创新:从"混合"到"组装",重塑空间构型
传统肾脏类器官多由单一祖细胞分化而来,或将不同谱系的细胞简单混合,导致结构混乱。该研究的核心创新在于高保真模拟体内器官发生(organogenesis)的自组装原则,通过"自下而上"的组装策略构建KPA:
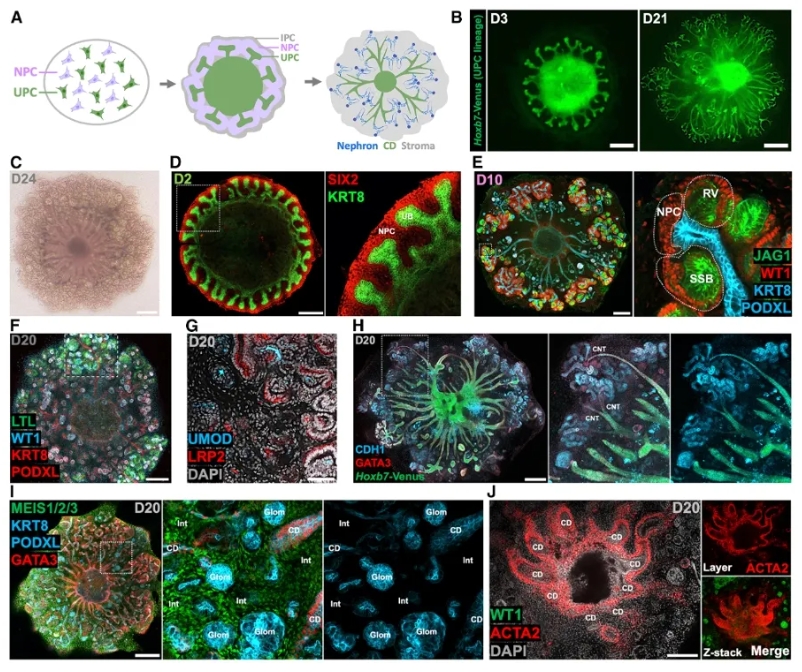
图1. 小鼠PKA的组装策略
A. iNPC/iUB祖细胞体系:利用团队先前建立的可扩增的诱导肾单位祖细胞(iNPCs)和诱导输尿管芽祖细胞(iUPCs),作为两个独立的"构建模块"。
B. 空间自组装:通过优化的三维培养系统(v2/v3 medium),引导iUPCs在中心形成聚集体,而iNPCs则在外周包裹并发生间充质-上皮转化(MET),形成围绕中央输尿管芽(UB)的极化肾小泡(polarized renal vesicles, RVs)。
C. 实现肾单位-集合管连接:这些RVs进一步发育成节段化的肾单位,其远端小管(distal nephron)最终与中央的集合管(collecting duct, CD)系统融合,形成连续的管状网络结构。
值得注意的是,研究发现维甲酸(Retinoic Acid, RA)信号(通过TTNPB激活)对于人源KPA中极化RV的形成至关重要,并揭示其可能通过上调WNT4来调控肾单位的发生,为优化分化方案提供了关键分子线索。
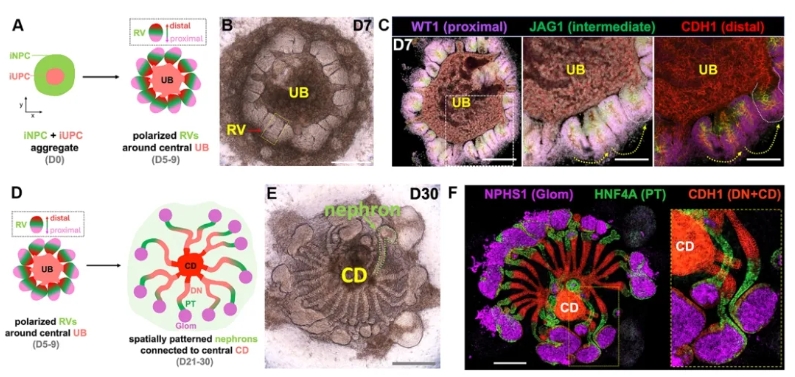
图2. hKPA发育过程示意图:iNPCs在中央iUPC周围形成极化的RV,并最终发育成与CD相连的肾单位
2. 功能完善:从结构模拟迈向生理功能再现
KPA模型在成熟度和功能性上均表现出显著提升,并通过严谨的体外与体内实验得到证实。单细胞多组学分析显示,mKPA的转录组特征接近出生后小鼠肾脏;而在体内存活1个月的hKPA,其成熟度相关基因集评分显著高于17周人类胎儿肾脏,并表达COL4A3/4/5、PLA2R1等成熟足细胞标志物以及SLC22A2(OCT2)、SLC22A6(OAT1)等重要转运蛋白。
体外培养的KPA已具备肾小管对葡聚糖、白蛋白的主动重吸收能力,以及对有机阴/阳离子的转运功能。此外,在特定诱导下,模型还能分泌肾素(Renin)和促红细胞生成素(EPO)。
进一步的,作者将早期hKPA移植到免疫缺陷小鼠肾包膜下,一个月后实现了高效血管化,其中包括由人类内皮细胞独立形成的肾小球毛细血管。并通过显微镜实时成像清晰地捕捉到肾小球的血液灌注和滤过过程。并于hKPA肾小管基底膜侧记录到了钾离子通道的电活动。
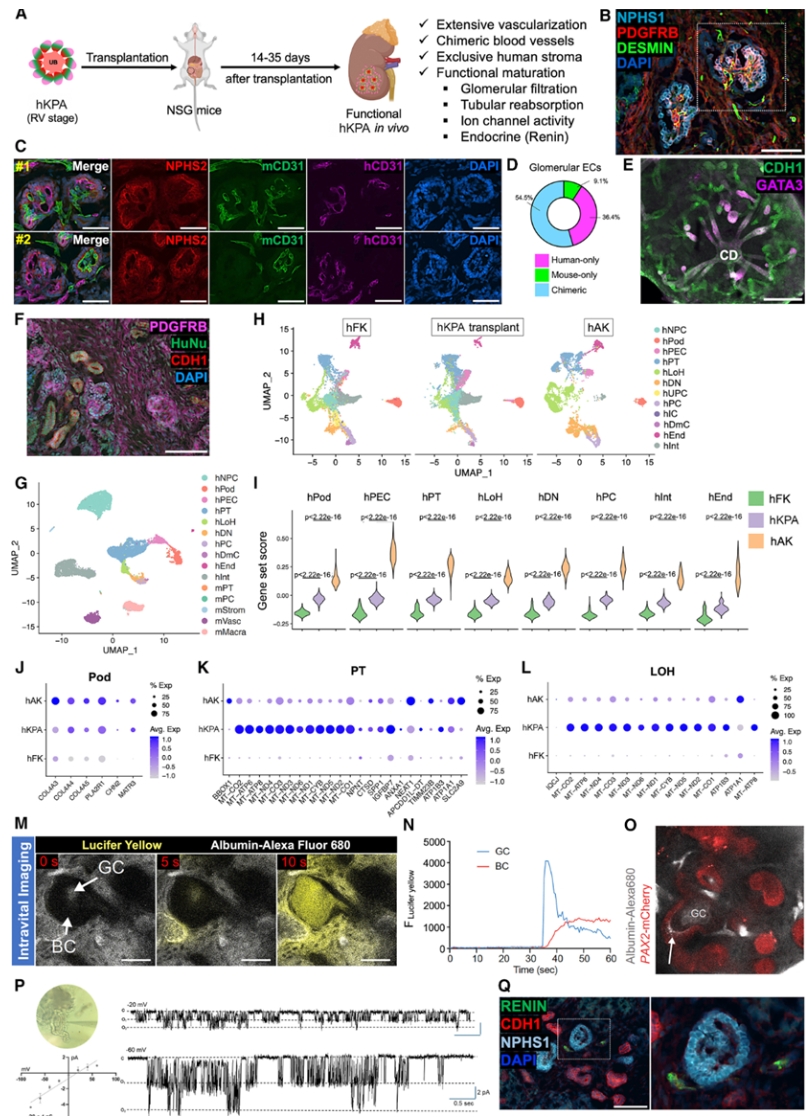
图3. hKPA移植小鼠内示意图,可见移植体内的hKPA肾小球实现血液灌注与滤过,并展示了其生理功能活性
3. 疾病建模:ADPKD复杂病理微环境的重现
该平台最令人振奋的应用,是其在疾病建模上的强大能力。研究团队利用CRISPR编辑的PKD2-/- iNPCs,构建了ADPKD hKPA模型,并在体内移植后观察到了传统体外模型难以重现的囊肿表型与细胞极性反转等病理现象。
PKD2-/- hKPA在体内形成了巨大的囊肿,并且初级纤毛(primary cilia)朝向囊腔,与ADPKD患者的病理特征一致。并发现在囊肿周围,形成了由人类细胞组成的、致密的PDGFRB+/COL1A1+/ACTA2+肌成纤维细胞层,这是肾脏纤维化的关键标志。此外,也发现了大量宿主来源的巨噬细胞被招募并聚集在囊肿上皮周围。
进一步的,通过CellChat分析,研究揭示了ADPKD模型中异常的细胞间串扰,如囊肿上皮(hPT)与间质(hInt)之间增强的TGF-β信号,以及与巨噬细胞之间激活的NOTCH信号,这些发现与ADPKD患者样本的分析结果高度一致,为探索早期致病机制和筛选干预靶点提供了宝贵资源。
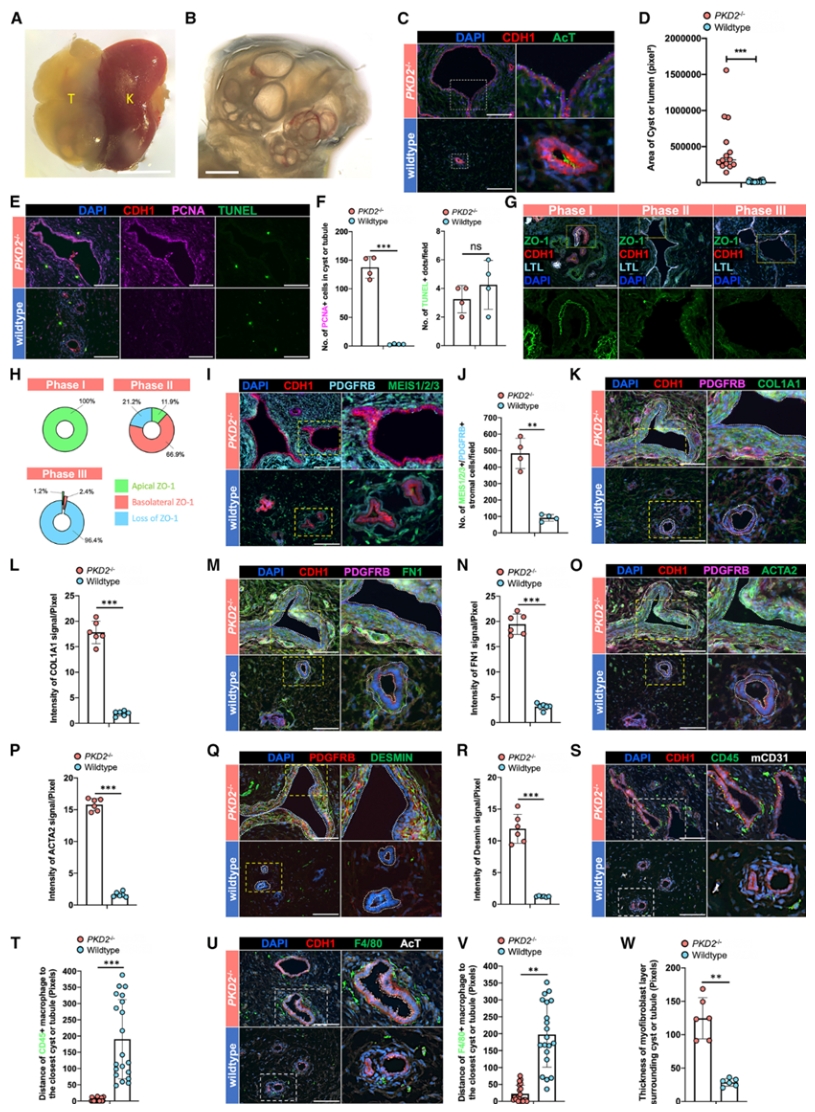
图4. PKD模型(底部)与野生型(顶部)对比,清晰显示囊肿周围的肌成纤维细胞和巨噬细胞浸润
总结
作者提出并验证了基于iNPC和iUPC双祖细胞系的"组装体"(KPA)策略,成功构建了具有中央集合管系统和外周连接性肾单位的空间有序结构。并通过多组学分析和严谨的体内外功能实验,证实KPA在细胞构成、转录组特征和生理功能(滤过、重吸收、内分泌)方面均达到了新的高度。
通过建立高保真ADPKD体内模型,首次在类器官模型中重现了纤维化和炎症浸润等关键的疾病微环境,并揭示了潜在的致病性细胞通讯网络。
该研究不仅为肾脏再生医学提供了结构和功能更优的基础组织单元,更重要的是,它为研究复杂的、涉及多细胞类型互作的肾脏疾病提供了一个前所未有的高保真、可追溯的实验平台。尽管模型仍存在持续肾单位生成和部分细胞类型缺失等局限,但其无疑为肾脏疾病的机制探索、药物开发和未来再生疗法开辟了全新的道路。
参考文献:
1. Huang, B., Medina, P., He, J., et al. (2025). Spatially patterned kidney assembloids recapitulate progenitor self-assembly and enable high-fidelity in vivo disease modeling. Cell Stem Cell, 32, 1–20.
2. Zeng, Z. et al. Generation of patterned kidney organoids that recapitulate the adult kidney collecting duct system from expandable ureteric bud progenitors. Nat. Commun. 12, 3641 (2021).
3. Huang, B. et al. Long-term expandable mouse and human-induced nephron progenitor cells enable kidney organoid maturation and modeling of plasticity and disease. Cell Stem Cell 31, 921-939.e17 (2024).

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

