肾脏的发生是一个精确而复杂的生物学过程,它涉及到三种主要的前体细胞群体的相互作用和分化。在哺乳动物中,这些群体包括上皮性的输尿管芽(ureteric bud, UB)细胞、表达Six2的肾单位组装前体细胞,以及表达Foxd1的间充质前体细胞。这些细胞群体共同协作,通过精细的信号传导和细胞间通讯,引导肾脏结构的形成和功能的发展。
肾脏提供了一个优秀的发育模型器官,因为体内早期的形态发生和细胞分化步骤在体外器官培养条件下可以重现,这使得科学家能够在控制的环境中研究肾脏发育的分子机制。尤为重要的是Wnt信号通路,在调控肾脏前体细胞的增殖、分化以及最终形成成熟的肾单位中发挥着核心作用。Wnt信号不仅引导肾脏前体细胞向特定细胞系分化,还维持它们的肾脏发生能力,确保肾脏的正常发育。这一过程中的任何失调都可能导致肾脏发育异常,影响个体的长期健康。
本文将深入探讨Wnt信号在肾脏发育中的作用机制,揭示其在肾脏形成中的关键作用,以及如何利用这些知识在体外模拟肾脏发育,为肾脏疾病治疗提供新的视角和策略。通过对肾脏前体细胞的深入研究,我们能够更好地理解肾脏发育的精细调控网络,为未来的再生医学和肾脏疾病治疗开辟新的道路。
来自芬兰奥卢大学的Sanna Junttila团队与来自瑞士苏黎世大学/苏黎世联邦理工学院的M. Rita Lecca团队及德国慕尼黑大学的André W. Brändli团队合作,通过一种创新的体外培养模型,深入探究了胚胎肾脏前体细胞的遗传靶向功能。该模型通过分离和重新聚集肾脏间质(MM)细胞,优化了在体外条件下模拟肾脏发育的能力,并利用这些细胞组装具有高度分化的肾单位。
虽然这些肾单位是在体外非生理条件下形成的,但是它们展现出了与体内相似的肾脏发生过程,精确地模拟了肾脏发育中的分子和细胞机制,体现了自然肾脏发育的强大调控能力。通过体外培养和分子标记物的分析,实验结果证实了模型的有效性,并观察到了与预期肾脏发育过程的高度一致性。这项研究不仅展示了在体外条件下对肾脏发育机制进行细胞和分子层面检查的潜力,还为肾脏疾病模型的建立和未来肾脏再生医学的发展提供了新的视角。相关研究成果以题为"Functional Genetic Targeting of Embryonic Kidney Progenitor Cells Ex Vivo"的文章发表在2015年的《Journal of the American Society of Nephrology》。

肾脏发育及体外培养模型示意图
1: 研究内容
实验系统概述:本文展示的实验系统如图1所示:首先描述了如何从E11.5的小鼠胚胎中机械分离出肾脏前体细胞——后肾间质(MM),这一步骤是实验的起点。随后,这些细胞被置于一个精心设计的体外培养系统中,模拟了它们在体内与输尿管芽(UB)的自然相互作用。
ABC1-A4模型:经典的肾小管诱导模型,将分离出的MM放置在1.0毫米孔径的Nuclepore滤器上,下方放置E11.5胚胎脊髓(eSC)的背侧片段,将结合物培养9天,模拟体内肾脏发育环境。
ABC1-B7模型:分散和重新聚集的肾脏前体细胞模型,将MM分散成单个细胞悬浮液(Dissociated Metanephric Mesenchyme,dMM)培养,在hrBMP7和hrFGF2的存在下,dMM细胞重新聚集后将诱导组织(eSC)放置在滤器对侧。
ABC1-C6模型:UB与drMM的重组模型,UB短暂暴露于Glial cell-derived neurotrophic factor (GDNF),处理后的UB与drMM培养,在没有生长因子的情况下培养,以评估肾脏器官形成的能力。
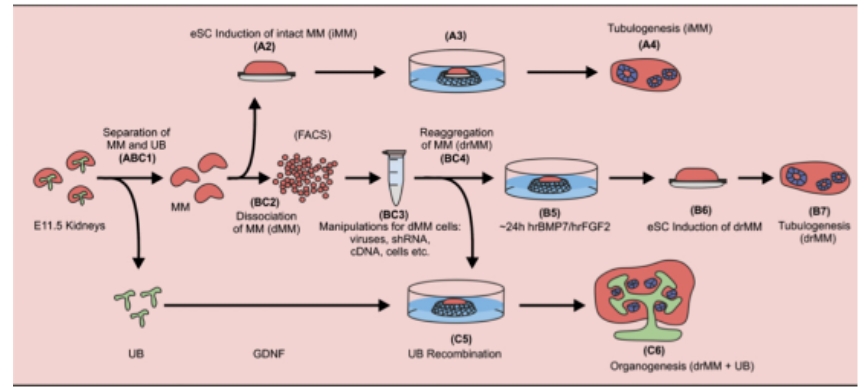
图1: 实验系统示意图
【小管诱导的后肾间质在体外能分化出成熟的肾单位】
本文通过研究体外条件下肾单位特异性标记物的诱导程度,来评估体外肾脏诱导模型的价值。作者通过将iMM和drMM与E11.5胚胎脊髓(eSC)结合,并培养9天,再利用RNA原位杂交技术来验证标记基因在相应肾单位段的表达(图2)。
结果显示:除了Henle环下降端标记物(图2-B表征的slc14a2)在iMM和drMM与eSC的结合体中表达有显著差异以外,其他标记物表达基本一致。因此,诱导的MM在体外也能组装分化良好的肾小管。
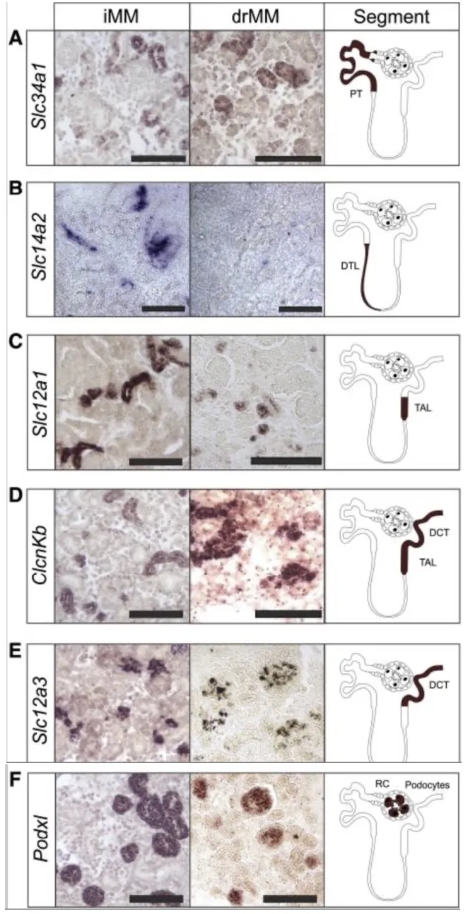
图2: iMM与drMM的区别
【BMP7/FGF2能维持drMM分化出肾小管的能力】
传统drMM技术的局限性在于,除非在MM解离步骤之前诱导小管生成,否则MM会退化。作者发现向分离并重新聚集的胚胎肾间充质前体细胞中补充hrFGF2和hrBMP7可以维持其肾发生能力。
如图3-A所示:如果不含hrBMP7和hrFGF2的情况下,将含有胚胎肾间充质的肾单位前体细胞分离并重新聚集(drMM),然后诱导分化,那么在培养后只会出现很少的管状结构。然而,在生成drMM时加入hrBMP7和hrFGF2,并在整个后续24小时的培养期间保持这些生长因子的存在,直到管状结构诱导步骤形成了大量的肾单位,通过Pax2免疫染色(绿色显示)可见(图3-B)。量化hrBMP和hrFGF2对维持drMM肾发生能力的积极影响(图3-C)。
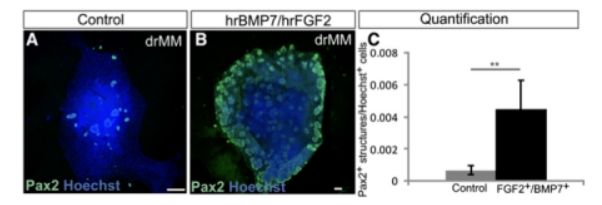
图3: 向分离并重新聚集的胚胎肾间充质前体细胞中补充hrFGF2和hrBMP7可以维持其肾发生能力
【生成嵌合性肾脏间质聚集体表明肾单位不是由单一前体细胞形成】
本文作者将带荧光的间质细胞和野生型间质细胞混合后用胚胎脊髓诱导后观察荧光信号来说明肾单位不是由单一前提细胞形成。
作者首先构建了CD-1GFP+小鼠模型,这里使用的是一个组成性活跃的β-actin/巨细胞病毒(CMV)启动子,这个启动子能够在多种细胞类型中驱动GFP的表达,然后将GFP+小鼠模型的MM细胞和野生型小鼠模型MM细胞按照1:6混合。培养的嵌合性外植体中的GFP+ MM细胞有能力整合到上皮小管(图4,A-D)和Foxd1+(间质细胞)、Aquaporin1+(AQ1,近端小管)、Slc12a1+(远端小管)和Nephrin+(足细胞)细胞中(图4,E-H)。因为未能找到完全由GFP+细胞组成的肾单位(图4),这表明肾囊泡具有非克隆性的细胞起源。
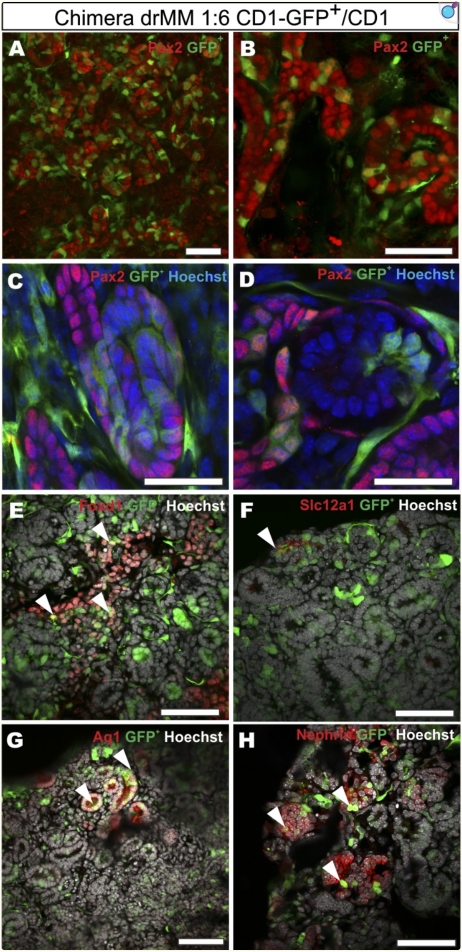
图4: 嵌合重组胚胎肾间充质前体细胞培养表明,肾单位不是由单一前体细胞形成
【Foxd1+ 肾脏间质前体细胞在肾脏间质中对于原始血管的扩张和肾脏发生的进展至关重要】
研究者进一步探索了Foxd1+ 间充质前体细胞在肾脏间质中的作用,特别是它们在原始血管扩张和肾脏发生进展中的关键作用。
利用(Foxd1cre+; floxed Rosa26tdTomato+)小鼠模型和流式细胞排序(FACS)技术,研究者分离出Foxd1+ 细胞,并在体外培养条件下观察这些细胞的行为。在器官培养条件下,Foxd1+ 细胞与Pax2+ 肾单位前体细胞保持区分(图5,A-D)。当这些Foxd1+ 细胞单独培养成为细胞聚集体后,再与eSC诱导,结果显示,Foxd1+ 细胞存活,但Pax2和Pecam1标记表达较弱(图5,E-H)。然而,当这些细胞与其余MM细胞结合并按照上述方法处理时,观察到这些标记的强烈表达(图5,I-L)。实验结果强调了Foxd1+ 间充质前体细胞在肾脏发育中的重要性,以及它们与其他肾脏间质细胞相互作用的必要性。
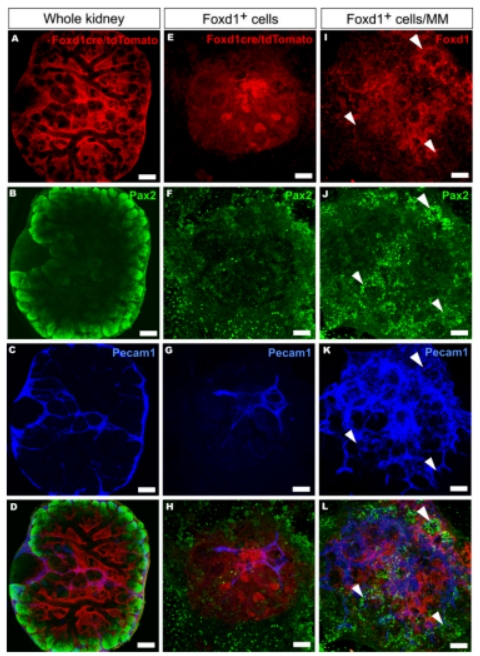
图5: Foxd1+间充质前体细胞与肾脏间质前体细胞的相互作用对于内皮网络和肾单位发展中的作用
【drMM与UB结合可以重建肾脏的发育能力】
鉴于诱导的drMM能够重建肾单位的分化,研究者决定研究与UB的相互和顺序组织相互作用是否也能在共轭物中恢复。
新鲜分离的UB在与MM重组前暴露于Glial cell-derived neurotrophic factor (GDNF)(图1,步骤C5),并培养9天以评估肾脏器官形成的能力。有趣的是,与GDNF处理过的UB结合的drMM恢复了肾脏器官形成,这基于形成的UB分支程度(图6,A和B)。UB也恢复了小管诱导的潜力,因为早期肾单位标记Pax2表达的MM细胞围绕UB尖端存在(图6,C和D,绿色)。Pax2+ 肾囊泡样结构和一些UB连接小管也已形成(图6,E-H,箭头)。一个类似髓质的区域也表达Pax2(图6,I-L),并且肾脏小球结构表达足细胞标记Nephrin(图6,M-P)。因此,诱导的drMM在一定程度上恢复了与UB的相互信号。
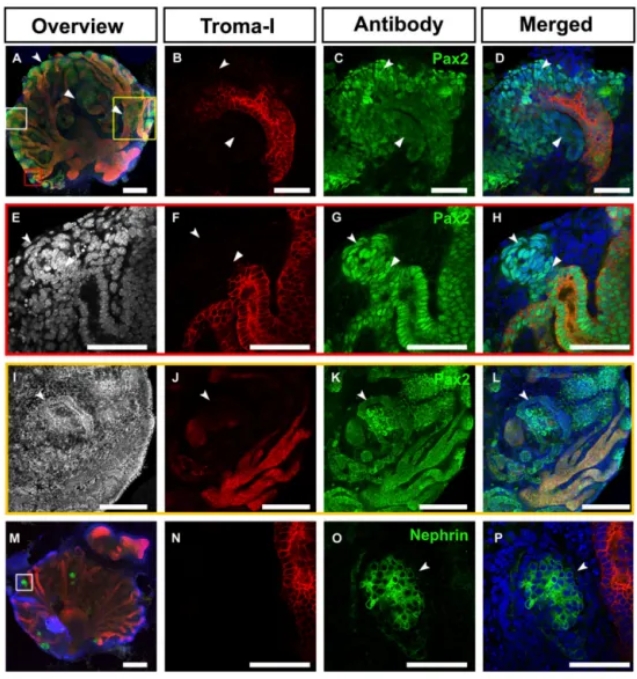
图6: drMM与UB结合可以重建肾脏的发育能力
【dMM可以高效转导逆转录病毒】
尽管重组病毒在细胞培养中靶向分子机制非常关键,但它们在组织渗透方面的局限性限制了其在器官形成研究中的应用。
胚胎肾脏间充质前体细胞的分散显著提高了它们被含GFP cDNA的重组逆转录病毒高效转导的能力,这些细胞在重新聚集和诱导后仍保持肾脏发生潜力。相比之下,未分散的iMM细胞(图7A-B)只有少数表层细胞被GFP+病毒转导,而分散的MM细胞(drMM)则显示出显著的GFP表达,表明高效转导(图7C-F)。值得注意的是,病毒转导并未影响肾单位前体细胞从间充质到上皮的转变,这是肾单位组装过程的关键,如上皮小管中E-钙粘蛋白的表达和GFP阳性细胞的存在所证实。
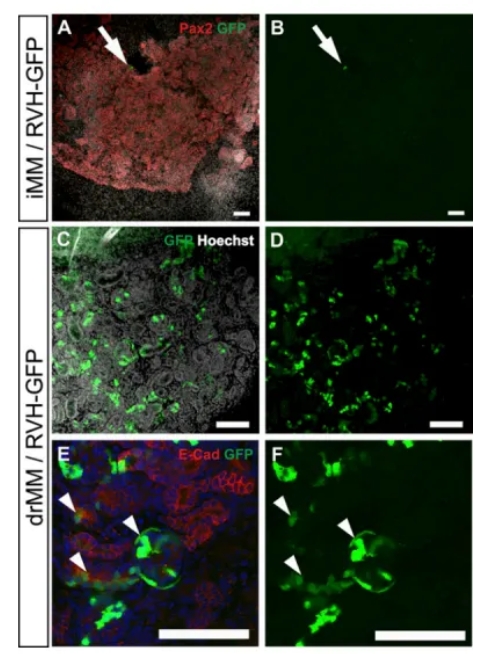
图7: dMM可以被高效的转导逆转录病毒
【被病毒转录后的肾间质细胞依然可以保持肾脏发生的潜力,从而能够靶向调控基因】
本文进一步探讨了体外模型是否可以用来靶向肾脏发生控制基因的功能。
研究者选择了Lhx1作为一个概念验证基因,因为Lhx1缺乏的肾单位前体细胞开始分化但后来退化。分散的MM细胞被转导与GFP-Lhx1-shRNA(GFP-Lhx1KD)病毒,这些病毒在模型细胞中使Lhx1表达沉默了69%至68.2%。这些病毒被引入到hrBMP7/hrFGF2存在下的dMM细胞中。MM细胞被重新聚集并培养了24小时,之后按照上述描述诱导小管生成。与对照GFP+病毒感染的相比,GFP-Lhx1KD病毒感染和重新聚集的GFP阳性Lhx1-KD细胞未能整合到主要由GFP阴性细胞组成的上皮化肾单位中。尽管肾单位管状发育没有GFP-Lhx1KD+细胞,但一些GFP+细胞足以整合到类似肾小球的结构中,与体内数据一致。被GFP+逆转录病毒转导的肾单位前体细胞仍然具备肾脏发生的能力,但shRNA介导的关键基因沉默可能会影响这一点。基于病毒载体的shRNA或cDNA方法应提供新的机会来探索体外重建的胚胎肾脏中MM前体细胞中候选肾脏发生控制基因的功能。
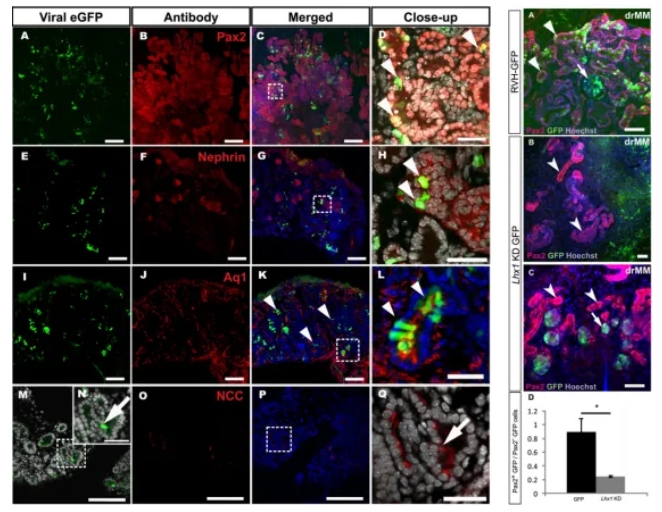
图8: 病毒介导的胚胎肾脏间质前体细胞(drMM)的转基因操作对其分化成不同肾小管段的能力的影响
2: 总结与展望
总结:本文通过体外培养和遗传操作技术,研究了胚胎期肾脏前体细胞(metanephric mesenchyme, MM)的肾发生能力。研究发现,通过分离和重新聚集MM细胞,并在特定生长因子存在下培养,可以恢复其形成肾单位的能力。
技术突破:利用病毒载体介导的基因转导技术,实现了对MM细胞的有效遗传操作,为研究肾单位的形成和肾脏器官发生提供了新的工具。这些技术不仅允许对肾脏发育的分子机制进行更深入的探索,也为未来肾脏疾病的基因治疗提供了可能。
展望:这些技术的发展和应用将极大地推动肾脏发育生物学和再生医学的研究。通过精确控制基因表达,科学家可以更详细地解析肾脏发育过程中的关键分子事件,为肾脏疾病的发病机制提供新的见解。此外,这些技术可能有助于开发新的治疗策略,如通过体外培养和遗传操作生成功能性肾脏组织,用于肾脏疾病的治疗。
文章来源
https://doi.org/10.1681/ASN.2013060584
Junttila, S., et al. (2015). Functional Genetic Targeting of Embryonic Kidney Progenitor Cells Ex Vivo. Journal of the American Society of Nephrology.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

