
近日,荷兰伊拉斯姆斯医学中心(Erasmus MC)移植研究所、肾脏科与病理科的Quincy Nlandu与Martin J. Hoogduijn教授团队,联合德国亚琛大学医院肾脏科与临床免疫学科的研究人员在《干细胞研究与治疗》上发表研究,利用人源iPSC肾类器官,成功构建了一个能同步模拟肾脏纤维化损伤与肾小管再生的关键模型。
研究团队通过联合应用缺氧(1% O₂) 与促炎因子IL-1β,在类器官中精准模拟了临床常见的缺血再灌注损伤。该处理最强效地诱导了纤维连接蛋白(FN1) 与I型胶原的沉积,并造成肾单位损伤。
研究揭示,损伤后,肾小管与肾小球走向截然不同的修复命运。在数周的持续培养中,肾小管标志物得以恢复,并伴随出现具有再生潜能的CD133+/CD24+祖细胞样细胞群。然而,足细胞标志物表达持续低下,肾小球结构未能有效修复,这精准复现了临床上足细胞损伤后难以再生的核心困境。
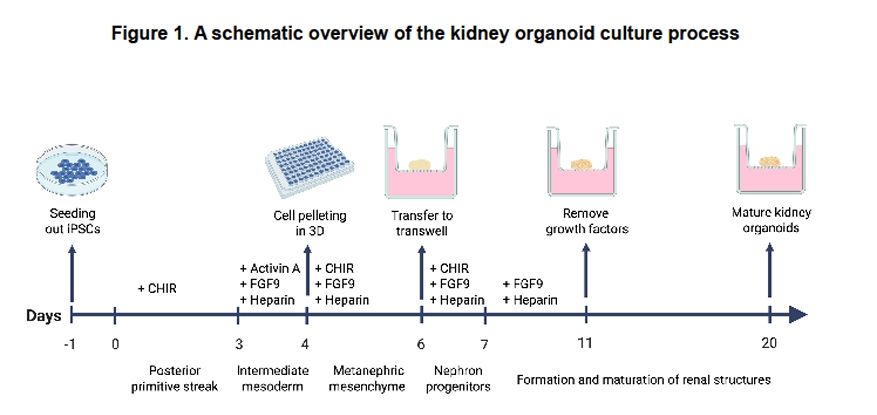
图1. 从诱导多能干细胞(iPSC)分化为成熟肾类器官的完整培养流程与时间线,涵盖了从后原条期、中间中胚层、后肾间充质到肾单位祖细胞的逐步诱导分化,以及肾结构最终形成与成熟的全过程。图中以时间轴形式清晰标明了关键生长因子(如CHIR99021、FGF9、Activin A)的添加与撤除节点,以及三维聚集和Transwell转移等关键操作步骤,为实验提供了标准化的技术路线图。
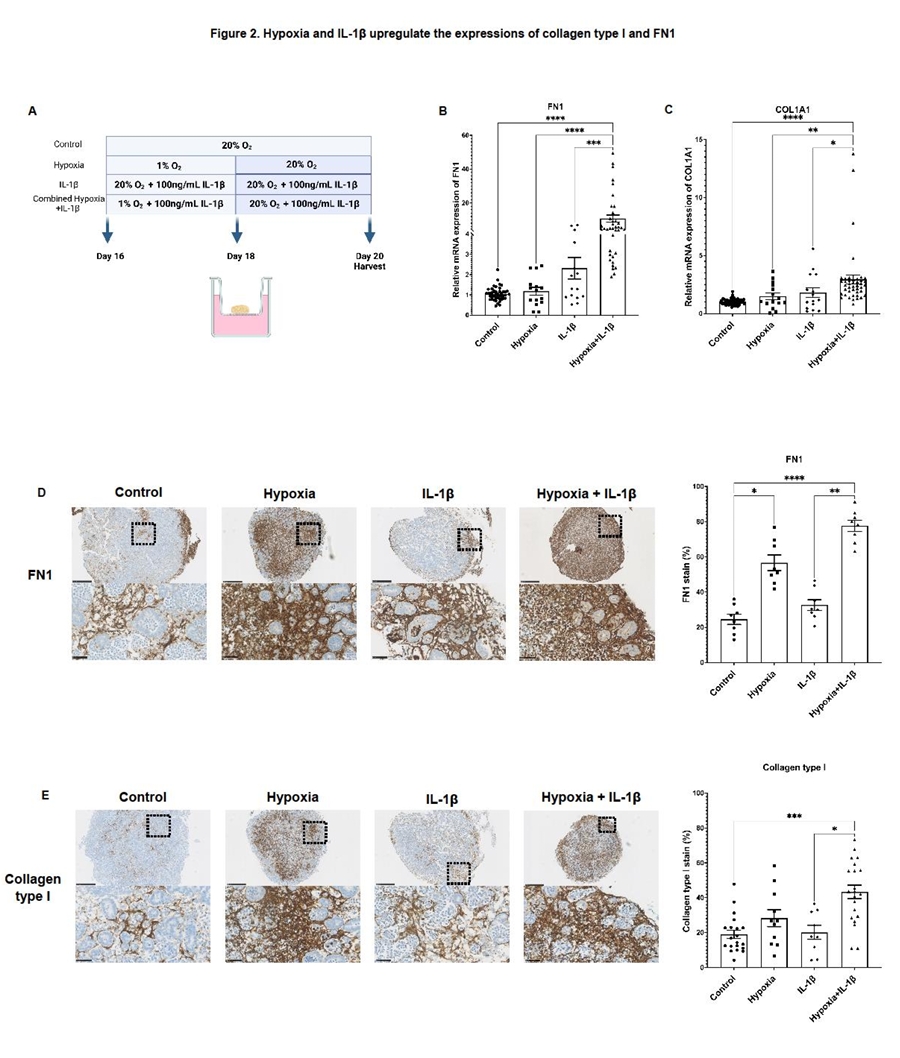
图2. 通过对比不同损伤诱导条件(单独缺氧、单独IL-1β、缺氧联合IL-1β)对肾类器官的影响,证实了联合刺激能最强效地上调纤维化标志物FN1与I型胶原的表达,表明缺氧与炎症的协同作用是诱导类器官发生显著纤维化重塑的关键机制。
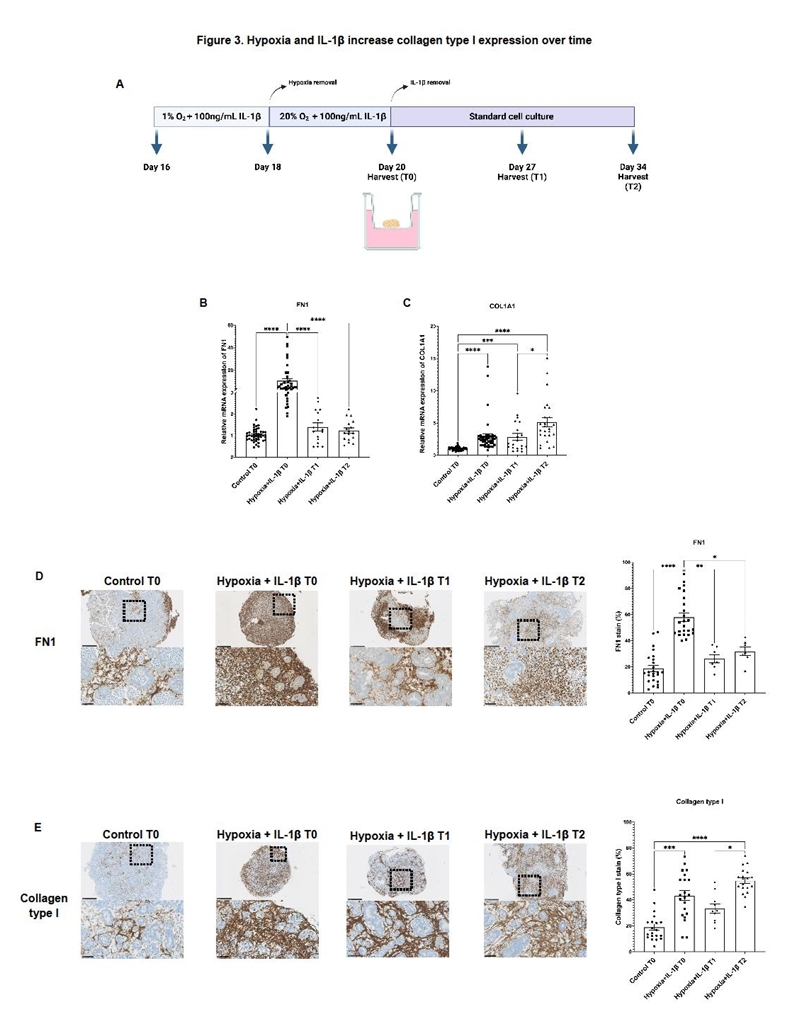
图3. 通过时序分析揭示了肾类器官在缺氧联合IL-1β损伤后不同时间点的纤维化动态变化:FN1的表达在损伤初期显著升高后逐渐恢复至基线,而I型胶原的表达则持续保持高水平,表明损伤诱导的纤维化中不同基质成分具有差异性的沉积与降解模式。
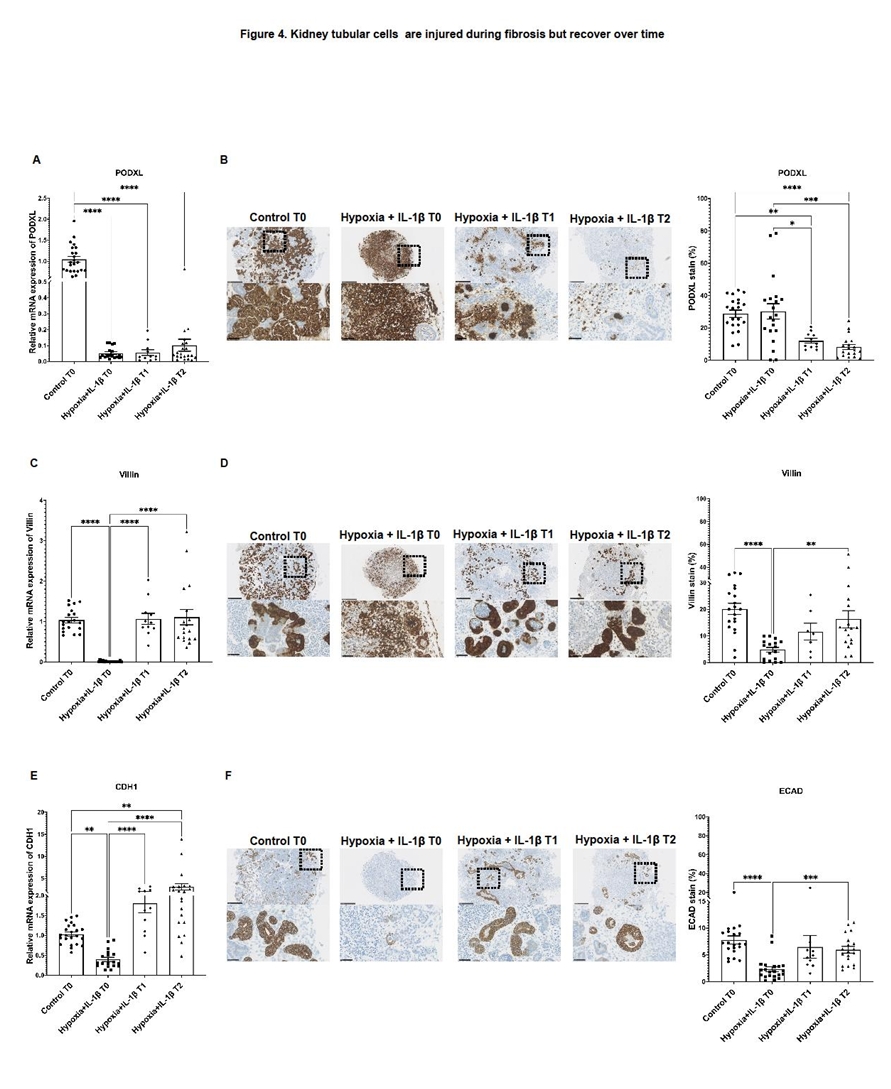
图4. 比较肾类器官在纤维化损伤后肾小球与肾小管结构的差异性修复过程:足细胞标志物PODXL持续低下且肾小球结构未恢复,而肾小管标志物Villin和ECAD则在损伤后逐渐恢复至近正常水平,表明肾小管具有较强的内源性再生能力而肾小球修复能力有限。
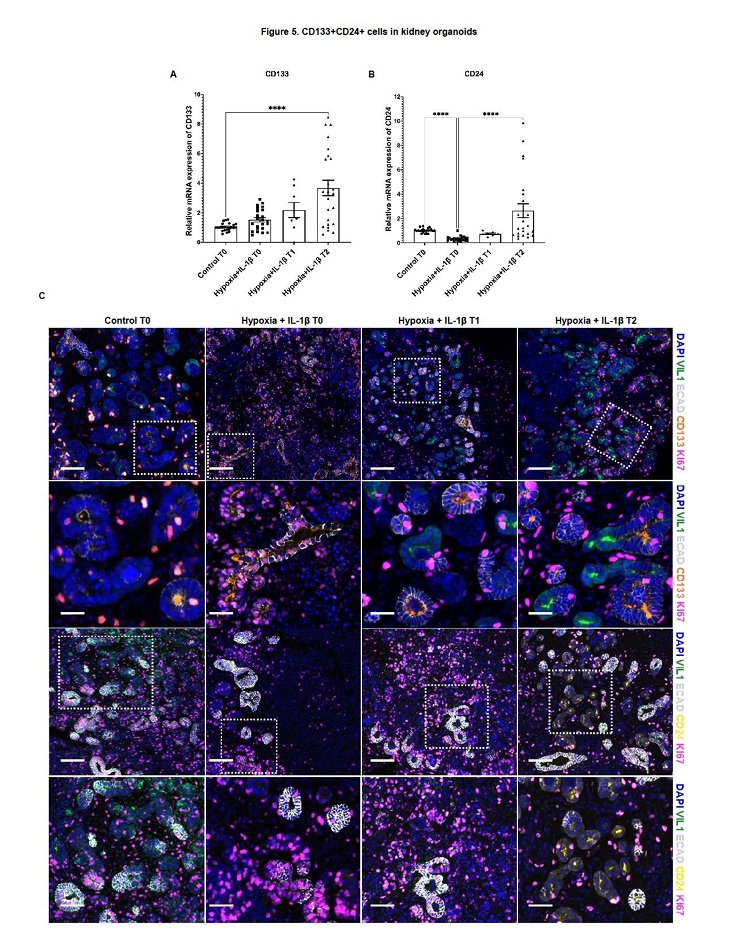
图5. 肾类器官在缺氧联合IL-1β损伤后出现的CD133+和CD24+细胞群体,这些细胞在损伤后随时间的延长而逐渐增多,并与Ki67阳性细胞共定位,提示其可能具有增殖活性和参与肾小管再生的祖细胞样特征。
该模型在一个人源化三维系统中,清晰地再现了损伤后纤维化瘢痕持续存在与肾小管内在再生程序被激活的并存现象,为在统一且高度相关的临床前平台上,并行筛选抗纤维化与促再生疗法提供了强大的新型工具。
参考文献
Li, Shengbing et al. “Modeling kidney fibrosis and tubular regeneration in iPSC-derived kidney organoids.” Stem cell research & therapy, 10.1186/s13287-025-04866-6. 18 Dec. 2025

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

