
常染色体显性多囊肾病(ADPKD)是最常见的遗传性肾脏疾病,也是导致肾衰竭的主要单基因病因。长期以来,托伐普坦作为唯一的疾病修饰疗法,虽验证了cAMP抑制的治疗思路,但其使用受限于多尿副作用和肝毒性风险,且仅能延缓疾病进展,无法根治。
近期发表于Kidney360的综述《Emerging Therapies in Autosomal Dominant Polycystic Kidney Disease》系统梳理了ADPKD治疗领域正在快速兴起的多维度策略,标志着该病管理正从单一通路干预迈向多机制、分层式、个体化治疗的新时代。
ADPKD的根源在于多囊蛋白功能缺失,导致纤毛钙信号紊乱、cAMP水平升高、细胞代谢重编程(转向糖酵解),进而驱动囊泡增殖与扩张。最新综述将新兴治疗策略归纳为以下几个关键方向,并已有多项疗法进入临床试验阶段:
1. 恢复多囊蛋白表达:基因剂量疗法
抗miR-17寡核苷酸(Farabursen):miR-17过表达会抑制*PKD1/PKD2*翻译,降低多囊蛋白水平。新型ASO药物通过抑制miR-17,恢复多囊蛋白表达,在临床前模型中显著减少囊肿负荷。
PC1折叠纠正剂(VX-407):针对约30%的PKD1错义突变导致蛋白错误折叠、滞留于内质网的问题,小分子药物VX-407作为药理性分子伴侣,帮助突变蛋白正确折叠并运输至纤毛膜,已进入基因型选择的II期临床试验。
2. 阻断局部生长信号:靶向IGF-1通路
抗PAPP-A单克隆抗体(ABBV-CLS-628):PAPP-A是一种金属蛋白酶,在囊肿微环境中切割IGFBP-4,释放活性IGF-1,促进囊肿上皮增殖。单抗药物通过抑制PAPP-A,局部降低IGF-1活性,显著减缓囊肿生长,目前已进入全球II期试验。
3. 代谢重编程治疗:调整能量与合成代谢
二甲双胍:作为AMPK激活剂,抑制mTORC1信号、降低cAMP-CFTR介导的氯离子分泌,其大规模III期试验(IMPEDE-PKD)正在进行中。
贝派度酸(Bempedoic acid):ATP柠檬酸裂解酶抑制剂,抑制脂肪合成,临床前研究显示与托伐普坦联用具有协同效应。
GLP-1受体激动剂:除减重、改善胰岛素敏感性外,还具有抗炎、抗纤维化及线粒体支持作用,其ADPKD专用试验已启动。
饮食干预:热量限制、限时进食、生酮饮食等可抑制mTORC1、增加酮体、促进脂肪酸氧化,在早期试点研究中显示出减缓疾病进展的潜力。
4. 新型cAMP调控:PDE4激活剂
作为cAMP水解的关键酶,长型PDE4亚型在囊肿上皮中高表达。其变构激活剂可局部增强cAMP水解,降低PKA活性,抑制囊肿生长,且不引起多尿副作用,目前正迈向首次人体试验。
5. 基因疗法与编辑:迈向功能性治愈
最令人振奋的进展之一是动物模型显示,在囊肿形成后重新表达Pkd1或Pkd2,不仅可阻止疾病进展,甚至可使囊肿消退、肾小管结构恢复正常。这证明ADPKD在适当条件下是可逆的。当前研发重点包括:
递送载体优化:通过定向进化开发肾趋向性AAV载体,或使用脂质纳米颗粒等非病毒平台。
编辑策略多样化:包括CRISPRa上调基因表达、碱基编辑纠正点突变、反式剪接实现大片段基因插入等。
微型PC1构建体:全长PKD1编码区过大(~13 kb),目前正在开发保留功能的截短型转基因作为过渡策略。
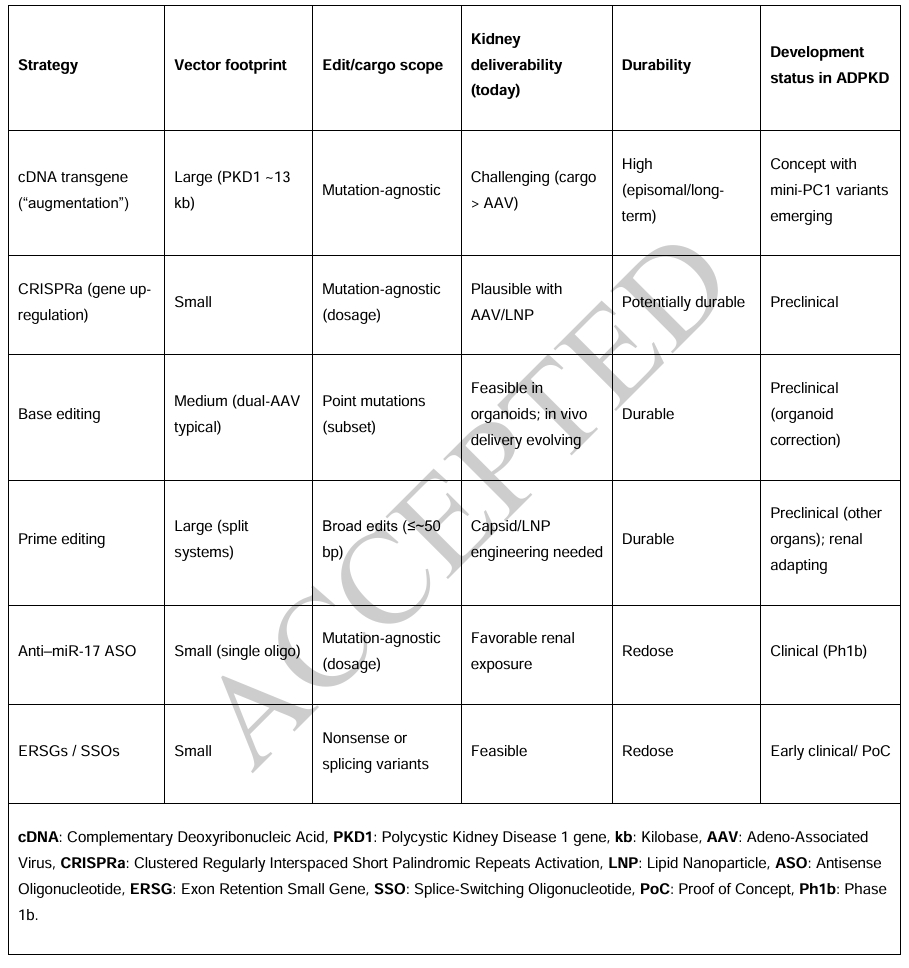
表4. 系统梳理并比较了当前处于不同研发阶段的ADPKD基因治疗策略,包括cDNA转导、CRISPR激活(CRISPRa)、碱基编辑、先导编辑、反义寡核苷酸以及翻译通读/剪接调控等六大技术方向。该表从载体装载需求、基因编辑范围、肾脏递送可行性、作用持久性和当前临床开发状态五个维度进行了横向对比,为评估不同基因治疗路径的技术特点与转化潜力提供了框架性参考。
多项临床试验因疗效不足或安全性问题终止,包括:
Venglustat(葡萄糖神经酰胺合酶抑制剂):II/III期试验因无效而停止。
GLPG2737(CFTR抑制剂):II期试验未显示疗效。
Lixivaptan(选择性V2受体拮抗剂):因一例显著转氨酶升高病例,开发暂停。
这些经验强调了临床前模型的预测价值、可靠生物标志物的必要性以及长期用药安全性筛查的重要性。
综述指出,未来ADPKD治疗将呈现分层化、组合化趋势:
近期:托伐普坦联合代谢调节剂(如二甲双胍、GLP-1激动剂)及信号通路抑制剂(如抗PAPP-A单抗)。
中期:引入基因型特异性疗法(如PC1折叠纠正剂)和无多尿副作用的cAMP调节剂(如PDE4激活剂)。
远期:基因编辑或基因增强疗法,旨在持久提升多囊蛋白水平至高于致病阈值,实现功能性治愈。
ADPKD治疗领域正处于从症状管理向疾病修饰乃至潜在治愈转变的关键时期。多囊蛋白功能恢复、局部信号通路调控、代谢重编程及基因治疗等策略的并行发展,标志着该领域已进入多靶点、多机制的精准治疗新时代。随着基因编辑技术、人工智能药物发现平台及人类肾脏类器官模型的深度融合,未来有望实现基于个体遗传背景和疾病分子特征的完全个性化治疗,最终改善ADPKD患者的长期预后。
参考文献:
Chen CY, Hadla M, Khambati I, Kashyap S, Westerfield V, Fedeles S, Besse W, Hopp K, Harris PC, Patel V, Chini E, Salih M, Barry MA, Chebib FT. Emerging Therapies in Autosomal Dominant Polycystic Kidney Disease. Kidney360. 2025 Dec 12

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

