慢性肾脏病(CKD)作为一种发病率高、病程进展性强、治疗手段较为有限的慢性疾病,在临床治疗中面临一定挑战。传统药物常因肾脏靶向性不足、全身性副作用明显,其应用受到一定限制。
近年来,纳米药物凭借其独特的理化性质和递送潜力,在肾脏疾病治疗研究中显示出一定的应用前景,但其向临床转化仍需更贴近人体生理的研究模型支持。本文结合近年相关研究,梳理纳米药物在肾脏疾病中的研究进展,并探讨肾脏类器官技术在该领域中的意义。
靶向ECM产生细胞的CAR-T疗法
缓解CKD纤维化
文献名称:Targeting ECM-producing cells with CAR-T therapy alleviates fibrosis in chronic kidney disease
发表期刊:Cell Stem Cell(IF 20.4)
发表日期:2025年9月4日
研究团队:山东大学易凡、唐伟、孙金鹏团队
研究概要:
研究首次发现靶向细胞外基质(ECM)产生细胞表面抗原PDGFRβ的嵌合抗原受体T细胞(CAR-T)疗法在多种小鼠CKD模型中可显著改善肾脏及多器官纤维化,且无明显毒性。研究中的CAR-T细胞可通过两种方式生成,其中之一是利用CD5-脂质纳米颗粒(LNP)在体内原位递送并生成,展现出纳米递送技术的治疗潜力。更重要的是,该疗法的抗纤维化效果在人源肾脏类器官构建的CKD模型中也得到了验证,为其临床应用提供了关键的支持性证据。
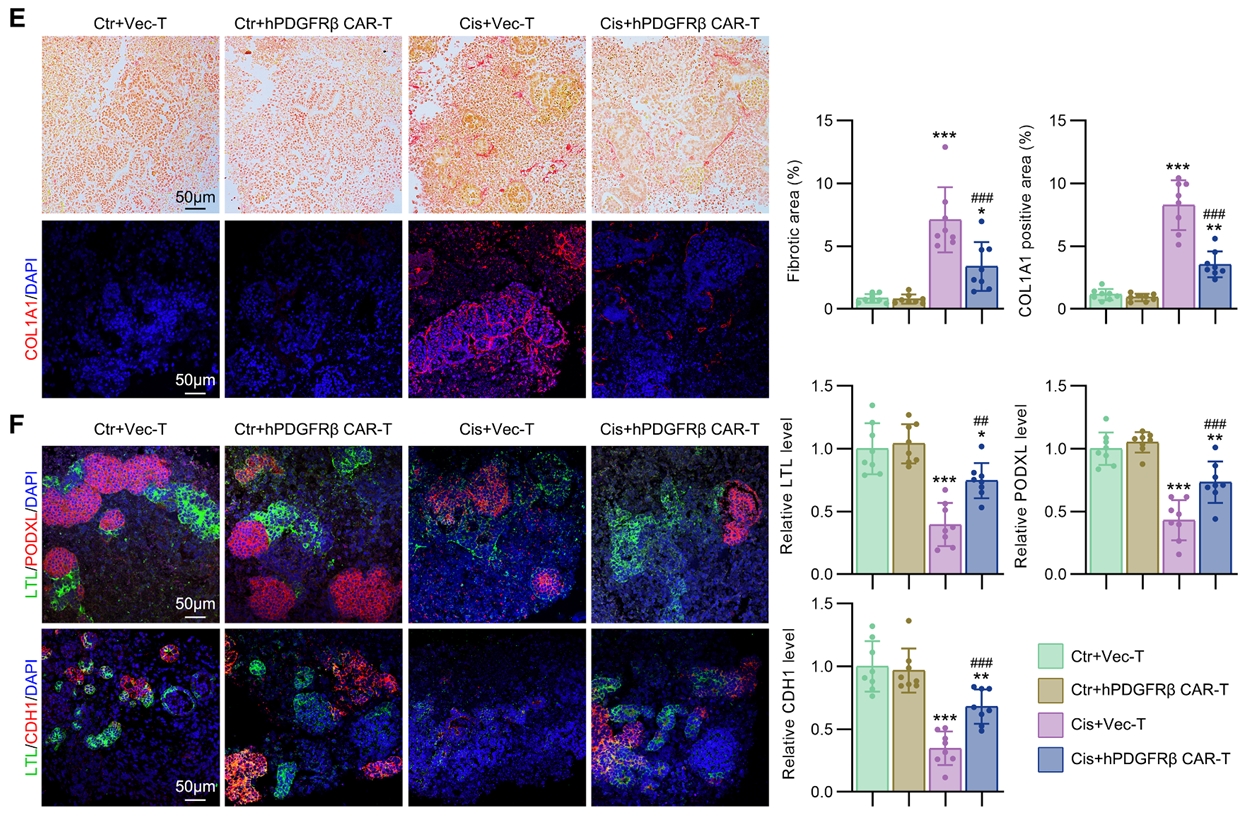
图1. hPDGFRβ CAR-T细胞减轻肾脏类器官CKD模型中的肾小管间质纤维化:
E) CAR-T治疗显著减轻顺铂诱导的肾脏类器官纤维化;
F) CAR-T治疗可改善肾小管、足细胞等标志物的表达水平。
(点击图片可放大)
吸入性纳米塑料通过激活特定信号通路
诱导肾损伤
文献名称:Toxicological effects and mechanisms of renal injury induced by inhalation exposure to airborne nanoplastics
发表期刊:Journal of Hazardous Materials(IF 11.3)
发表日期:2025年5月5日
研究团队:天津医科大学第二医院陈岳、浙江大学医学院附属儿童医院胡丽丹、天津医科大学第二医院齐士勇团队
研究概要:
本研究首次将人源肾脏类器官应用于吸入性纳米塑料的肾毒性评估。结果表明,相比于永生化肾小管上皮细胞(HK-2),肾脏类器官对纳米塑料表现出更高的敏感性,揭示了纳米塑料通过激活NR4A1/CASP3和TF/F12信号通路诱导氧化应激、炎症和肾损伤的分子机制。
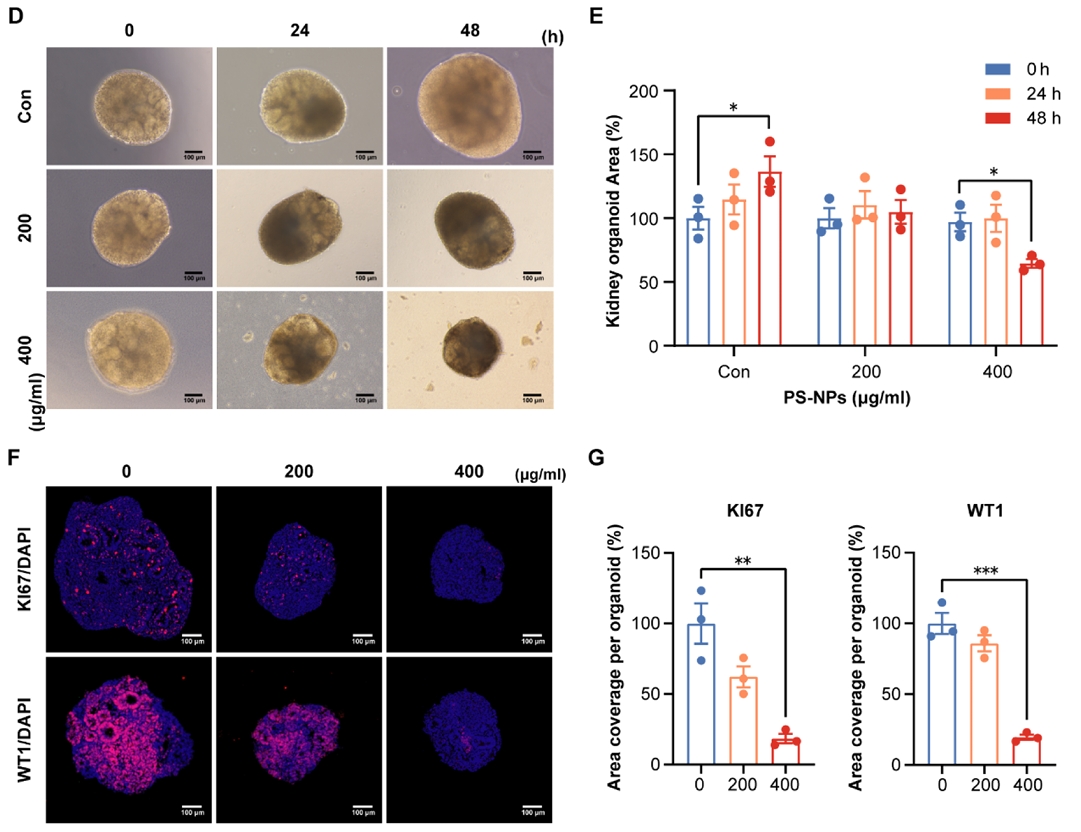
图2. 人肾脏类器官的培养及纳米塑料暴露对其的影响:D) 纳米塑料暴露导致类器官形态变化;E) 类器官面积随纳米塑料浓度增加而减小;F) 增殖与足细胞标志物染色;G) 纳米塑料抑制增殖并影响足细胞标志。
(点击图片可放大)
单线态双自由基纳米颗粒
诱导肾脏代谢重编程
文献名称:Induction of Metabolic Reprogramming in Kidney by Singlet Diradical Nanoparticles
发表期刊:Advanced Materials(IF 26.8)
发表日期:2023年9月刊
研究团队:清华大学深圳国际研究生院马岚、天津大学分子+研究院孙哲团队
研究概要:
研究设计了一种新型单线态双自由基纳米材料(BO-Ph),并在人源肾脏类器官中验证了其生物安全性及功能。BO-Ph能通过刺激谷胱甘肽合成、促进脂肪酸降解和增强三羧酸循环,诱导有益的代谢重编程,从而提升肾脏细胞的抗氧化能力和线粒体功能。
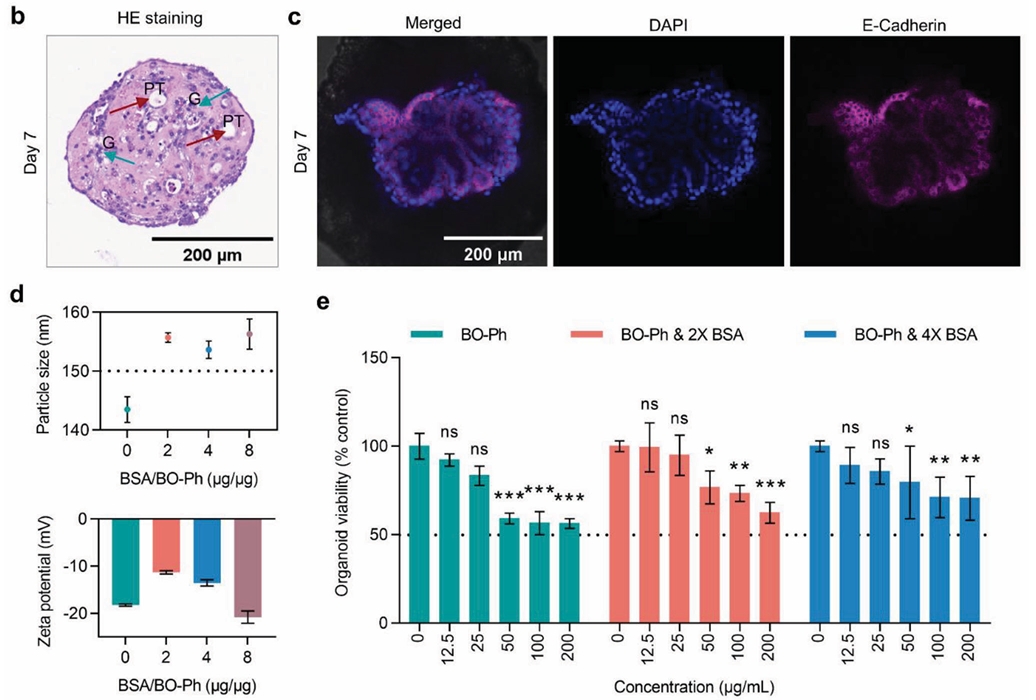
图3. BO-Ph在体外肾脏类器官中诱导的细胞毒性:b) 第7天肾脏类器官的肾小球和近端小管结构;c) 类器官上皮标志物E-钙黏蛋白表达情况;d) BO-Ph纳米颗粒的粒径和电位数据及BSA包被影响;e) BO-Ph及其BSA包被版本对类器官存活率的影响。
(点击图片可放大)
组织工程策略构建罕见肾病活体模型
并测试纳米疗法
文献名称:A tissue-bioengineering strategy for modeling rare human kidney diseases in vivo
发表期刊:Nature Communications(IF 15.7)
发表日期:2021年11月11日
研究团队:美国波士顿Brigham and Women’s Hospital的D. R. Lemos团队
研究概要:
本研究创新性地利用结节性硬化症患者来源的iPSC构建了人源肾脏类器官,成功模拟了肾血管平滑肌脂肪瘤与上皮囊肿等病变,并将其移植至免疫缺陷大鼠肾内,构建出可用于机制研究与药物测试的活体肿瘤模型。在此模型中,研究验证了负载雷帕霉素的纳米颗粒能有效抑制肿瘤生长。
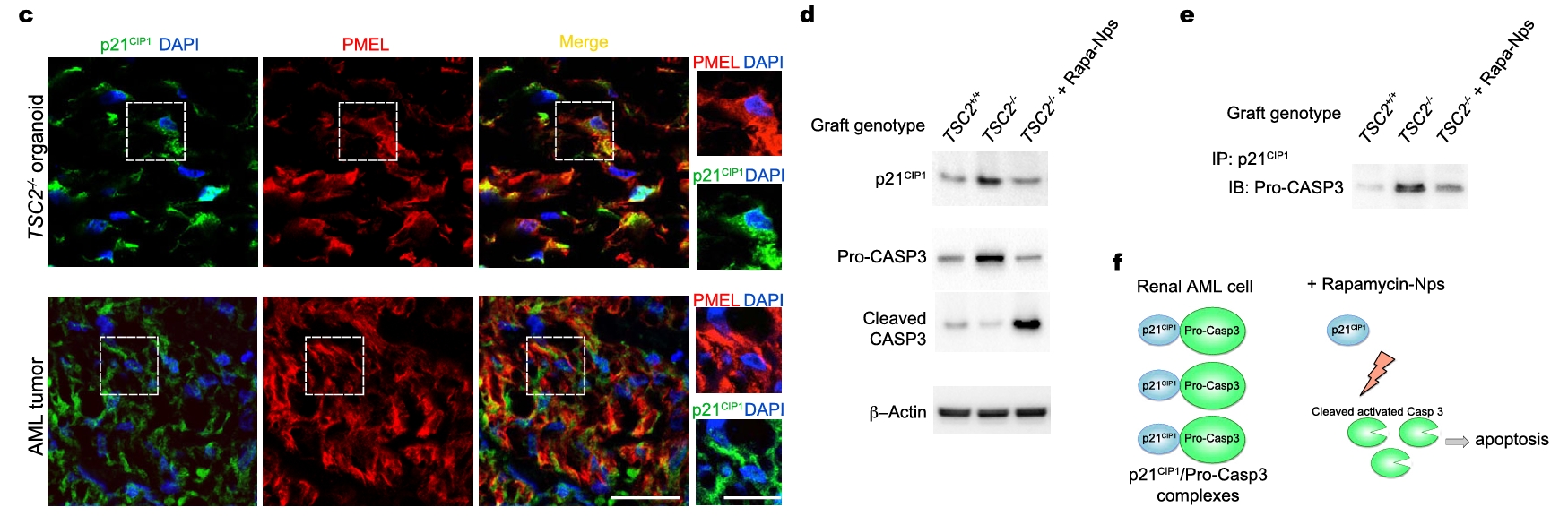
图4. 雷帕霉素纳米颗粒在体内破坏TSC2−/−类器官AML细胞中p21CIP1与pro-CASP3的相互作用:c) 类器官与肿瘤样本均检测到p21CIP1蛋白表达;d) TSC2−/−类器官中p21CIP1和pro-CASP3蛋白水平升高;e) 雷帕霉素纳米颗粒破坏p21CIP1与pro-CASP3蛋白结合。
(点击图片可放大)
黑磷量子点通过IRE1α信号通路
在肾脏类器官中引发肾毒性
文献名称:Black Phosphorus Quantum Dots Cause Nephrotoxicity in Organoids, Mice, and Human Cells
发表期刊:Small(IF 12.1)
发表日期:2020年6月刊
研究团队:厦门大学生命科学学院左正宏、清华-伯克利深圳学院马少华、厦门大学生命科学学院何承勇团队
研究概要:
研究建立了一种基于微流控的均质化肾脏类器官高通量筛选平台。利用该平台,发现黑磷量子点(BP-QDs)在肾脏类器官中引起显著毒性,其敏感性高于2D培养细胞系。进一步机制研究表明,BP-QDs通过激活IRE1α介导的内质网应激通路,导致胰岛素抵抗和细胞损伤。
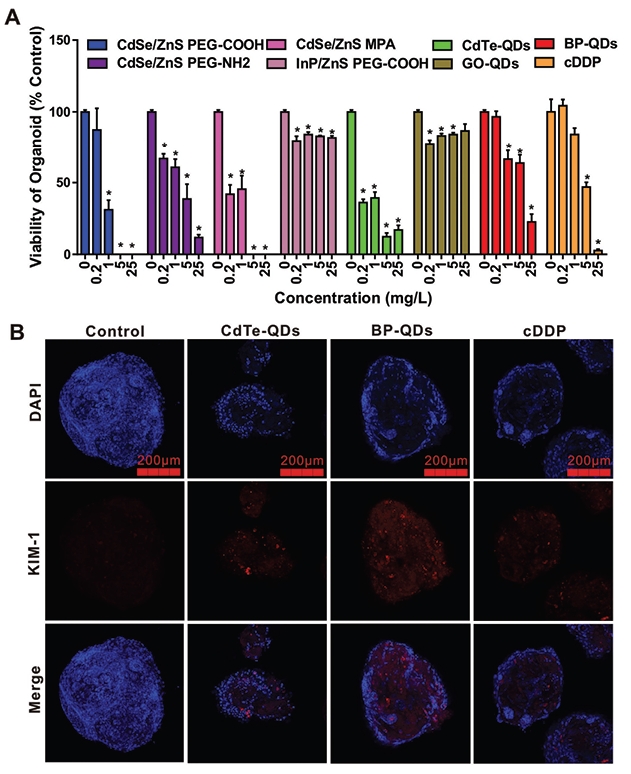
图5. 肾脏类器官量子点毒性检测:A) 量子点处理后细胞存活情况(顺铂对照);B) 毒性标志物KIM-1表达检测。
(点击图片可放大)
肾脏类器官在纳米药物研究中
的应用价值
在纳米药物的研发过程中,传统细胞模型和动物模型存在一定局限性。肾脏类器官作为一种三维培养的人源微组织,可部分模拟肾脏的结构与功能,为相关研究提供补充性的实验平台。
如前述五项研究所示,肾脏类器官在以下方面有参考价值:
在人源组织环境中观察纳米药物或纳米材料的效应。
为纳米药物的初步疗效或安全性评估提供实验条件。
用于研究纳米材料与肾脏细胞的相互作用及相关机制。
研究支持与服务
在相关研究过程中,华津生物基于自主研发的Kidnioid®人源肾脏类器官平台,可提供肾脏类器官培养、疾病模型构建及体外药物测试等技术服务,为研究人员开展纳米药物相关研究提供实验条件支持。
华津Kidnioid®肾脏类器官技术平台
肾脏类器官模型
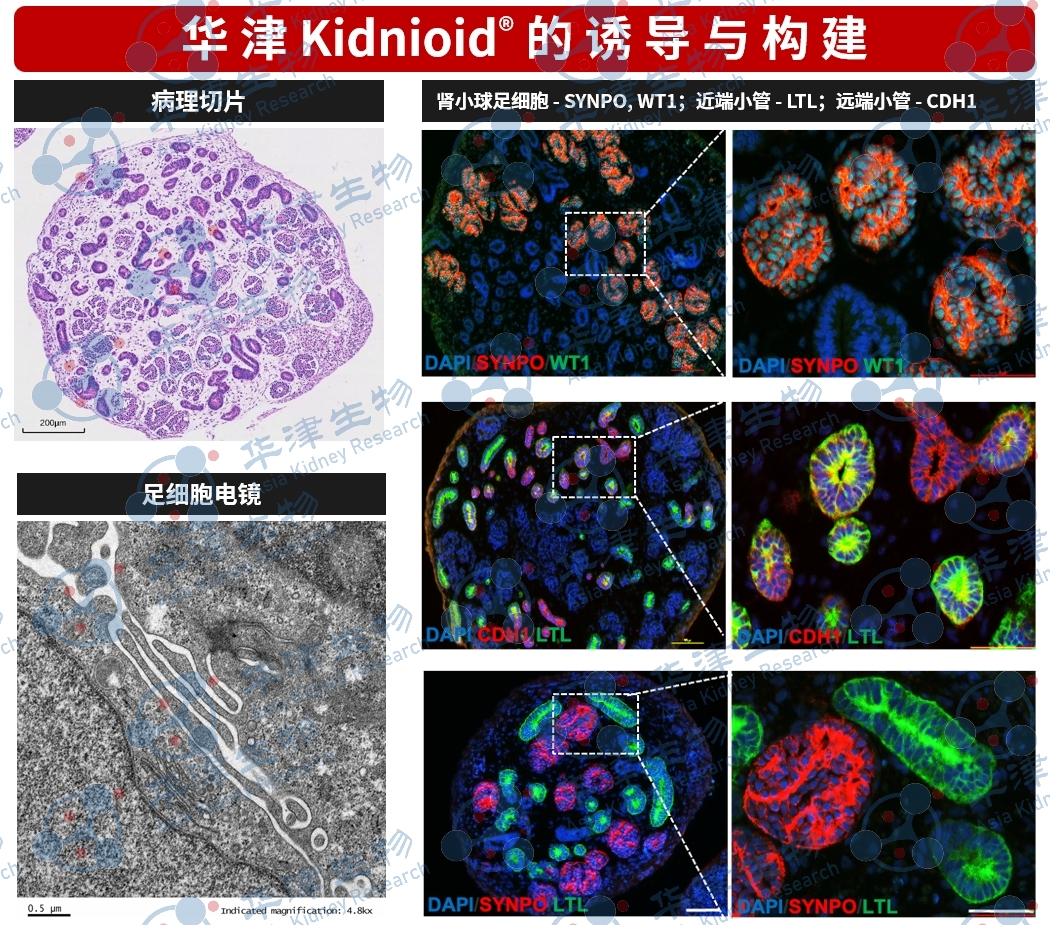
图1. 经病理切片、电镜及免疫荧光鉴定,该肾脏类器官可观察到肾小球与肾小管结构,电镜下可见足细胞足突形态,免疫荧光染色显示足细胞、近端小管及远端小管的定位特征。
基于人源肾脏类器官构建,包含近端小管、足细胞等功能结构,能够模拟疾病相关的病理变化。
该模型可支持:
药物作用机制的系统研究
多信号通路的协同分析
细胞-药物相互作用评估
适用于药物筛选、毒性评估、疾病机制研究及个性化医疗等多个方向。
周期较短:相比部分动物实验,模型构建与评估时间有所缩短。
可重复性较好:在标准化培养条件下,模型稳定性较高。
灵活性较强:可根据研究需求进行定制化调整。
检测体系适配性高:与常规分子生物学/细胞生物学方法高度兼容,可直接开展qPCR、Western blot、免疫荧光等检测,便于机制研究与多指标评价。
感谢您对本文的浏览。肾脏类器官作为前沿生物技术,不仅在疾病模拟、药物筛选和再生医学研究中展现出巨大潜力,也为精准医疗和新药研发提供了更可靠的平台。目前全球多家监管机构已将其纳入药物评价体系,标志着该技术正逐步走向标准化与应用化。如果您希望进一步了解肾脏类器官的技术细节、合作研究或商业应用,欢迎随时联系咨询:
商务支持 - 李老师 17276665437
技术支持 - 田老师 18843183823
我们期待为您提供专业服务与合作支持。

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

