慢性肾脏病及遗传性肾脏疾病因其病因复杂、病理机制多样,长期以来缺乏精准有效的治疗手段。传统研究多依赖动物模型或二维细胞培养,但这些模型在模拟人类肾脏生理和病理特征方面存在局限。
近年来,CRISPR基因编辑技术的突破性发展为肾脏疾病研究开辟了全新路径。通过在人诱导多能干细胞(iPSCs)中精确引入或修复致病突变,并结合肾脏类器官三维培养技术,研究者能够在体外重现患者特异性病理表型,深入探究疾病机制,并开展药物筛选与评估。本文梳理了近年利用CRISPR-Cas9及碱基编辑技术构建肾脏类器官疾病模型的研究进展,展现了这一技术平台在遗传性肾小管病、足细胞病变及多囊肾病等领域的应用前景。
构建Gitelman综合征细胞模型
文献名称:CRISPR/Cas9-based SLC12A3 gene knock in: a model for cellular feature analysis in Gitelman syndrome
发表期刊:Kidney Research and Clinical Practice
发表日期:2026年2月6日在线发表
研究团队:韩国天主教大学医学院首尔圣玛丽医院Byung Ha Chung团队
研究概要:
本研究利用CRISPR/Cas9基因编辑技术,将SLC12A3基因成功敲入人类诱导多能干细胞(hiPSCs),建立了WTC-11SLC12A3-KI细胞系。通过绿色荧光蛋白(GFP)报告基因及多种分子生物学技术验证了SLC12A3的成功表达。将该细胞系分化形成的肾脏类器官中,SLC12A3表达及其下游WNK-SPAK/OSR1信号通路均显著增强。功能分析显示,血管紧张素II可刺激类器官细胞内钠离子流,而噻嗪类利尿剂则可减弱这一反应。该研究表明,SLC12A3基因敲入策略可作为Gitelman综合征的潜在治疗方向,并为研究该疾病的细胞特征和药物反应提供了有效的体外模型。
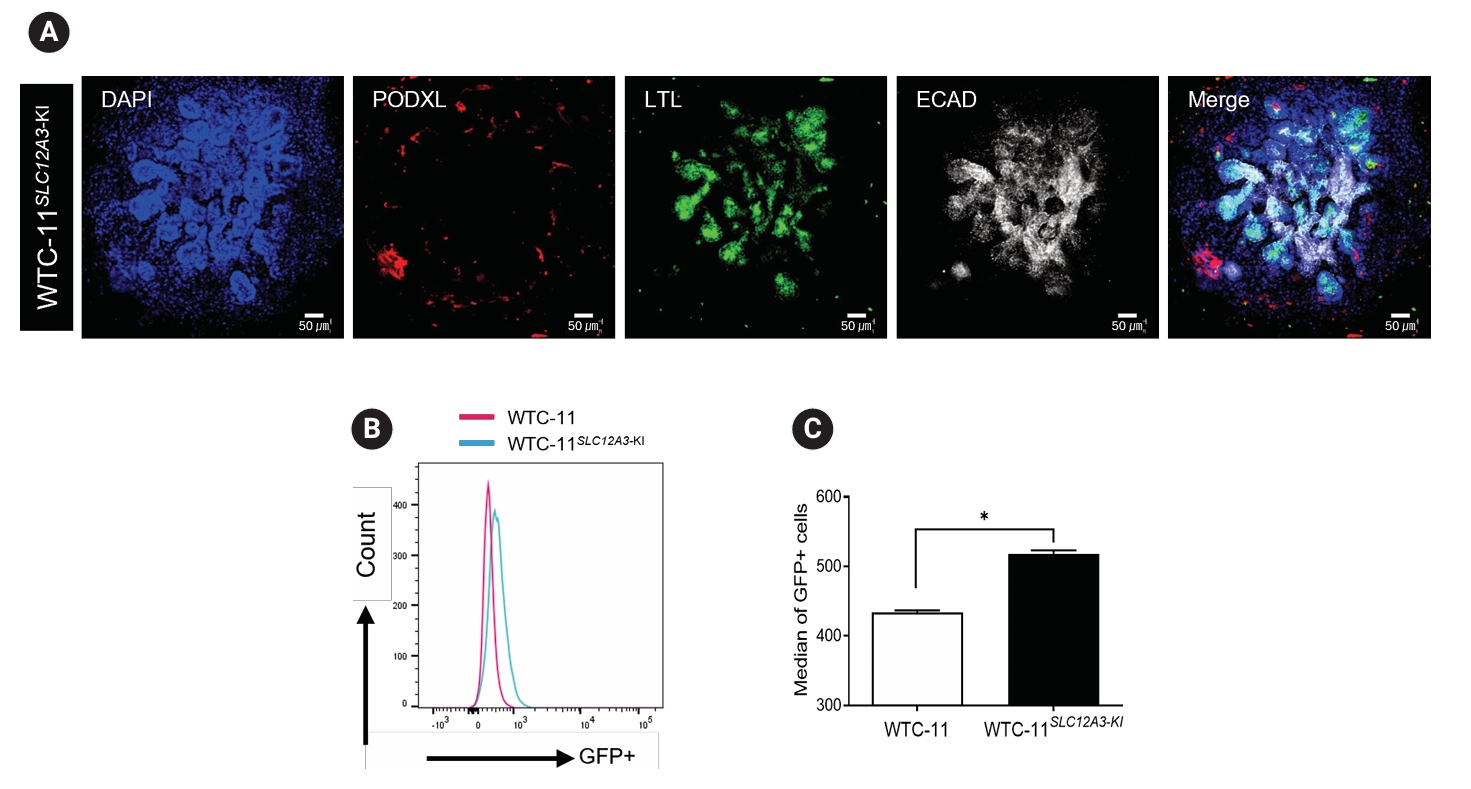
(点击图片可放大)
他汀类药物展现治疗潜力
文献名称:KCNJ16-depleted kidney organoids recapitulate tubulopathy and lipid recovery upon statins treatment
发表期刊:Stem Cell Research & Therapy
发表日期:2024年8月26日
研究团队:荷兰乌得勒支大学药学院A M van Genderen团队
研究概要:
本研究利用CRISPR/Cas9技术在健康人诱导多能干细胞(iPSC)中构建了KCNJ16基因杂合(+/-)和纯合(-/-)突变的细胞系,并分化获得气液界面培养的成熟肾脏类器官。KCNJ16基因敲除的类器官重现了肾小管病变的关键病理特征,包括囊肿形成、脂滴积聚和纤维化,并表现出电压依赖性电解质和水通道转运体的转录组及功能损伤。通过大规模谷氨酰胺示踪代谢组学分析发现,KCNJ16-/-类器官存在三羧酸循环和脂质代谢障碍。药物筛选结果显示,他汀类药物(特别是辛伐他汀与C75联合使用)可有效阻止脂滴积聚和胶原蛋白I沉积。该研究为KCNJ16相关遗传性肾小管病的机制研究提供了新见解,并揭示他汀类药物作为潜在治疗策略的可能性。
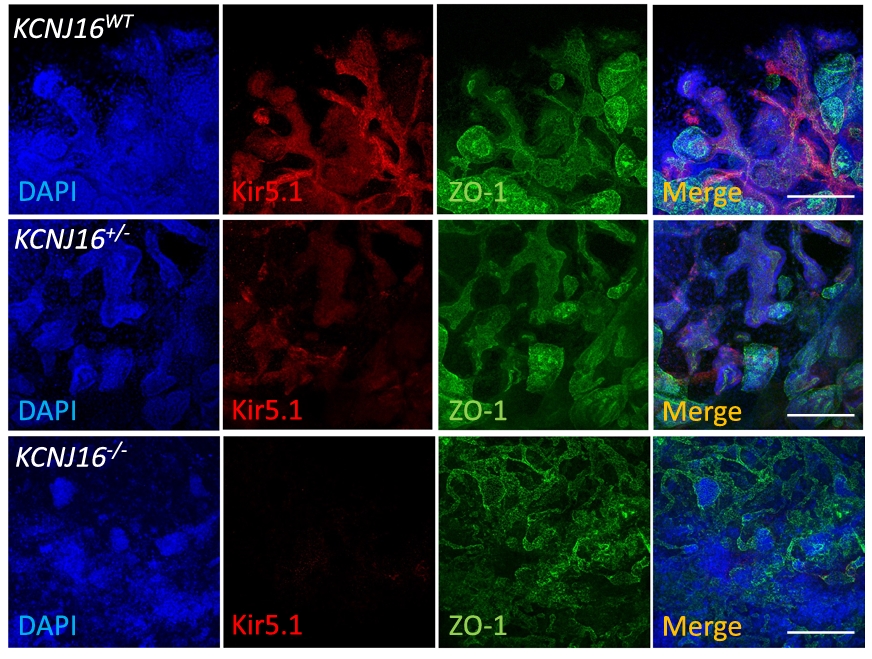
(点击图片可放大)
足细胞发育关键调控通路
文献名称:Kidney Organoid Modeling of WT1 Mutations Reveals Key Regulatory Paths Underlying Podocyte Development
发表期刊:Advanced Science(IF 14.1)
发表日期:2024年8月刊
研究团队:南京大学医学院附属金陵医院刘志红院士团队
研究概要:
本研究通过单细胞染色质可及性测序(scATAC-seq)和单细胞RNA测序(scRNA-seq)绘制了胎儿肾脏和肾脏类器官的表观遗传图谱,揭示了WT1调控足细胞发育的关键下游靶基因,包括调控WNT信号通路的BMPER/PAX2/MAGI2、维持肌动蛋白细胞骨架的MYH9以及调节细胞连接组装的NPHS1。研究利用携带WT1杂合错义突变的患者iPSC分化获得肾脏类器官,发现该突变导致WT1无法激活其靶基因MAGI2、MYH9和NPHS1,进而引起足细胞发育延迟和细胞结构损伤。更重要的是,利用CRISPR-Cas9技术纠正患者iPSC中的WT1突变后,足细胞表型得到显著恢复。该研究阐明了WT1相关的人类足细胞发育表观遗传调控网络,并验证了WT1突变的致病机制。
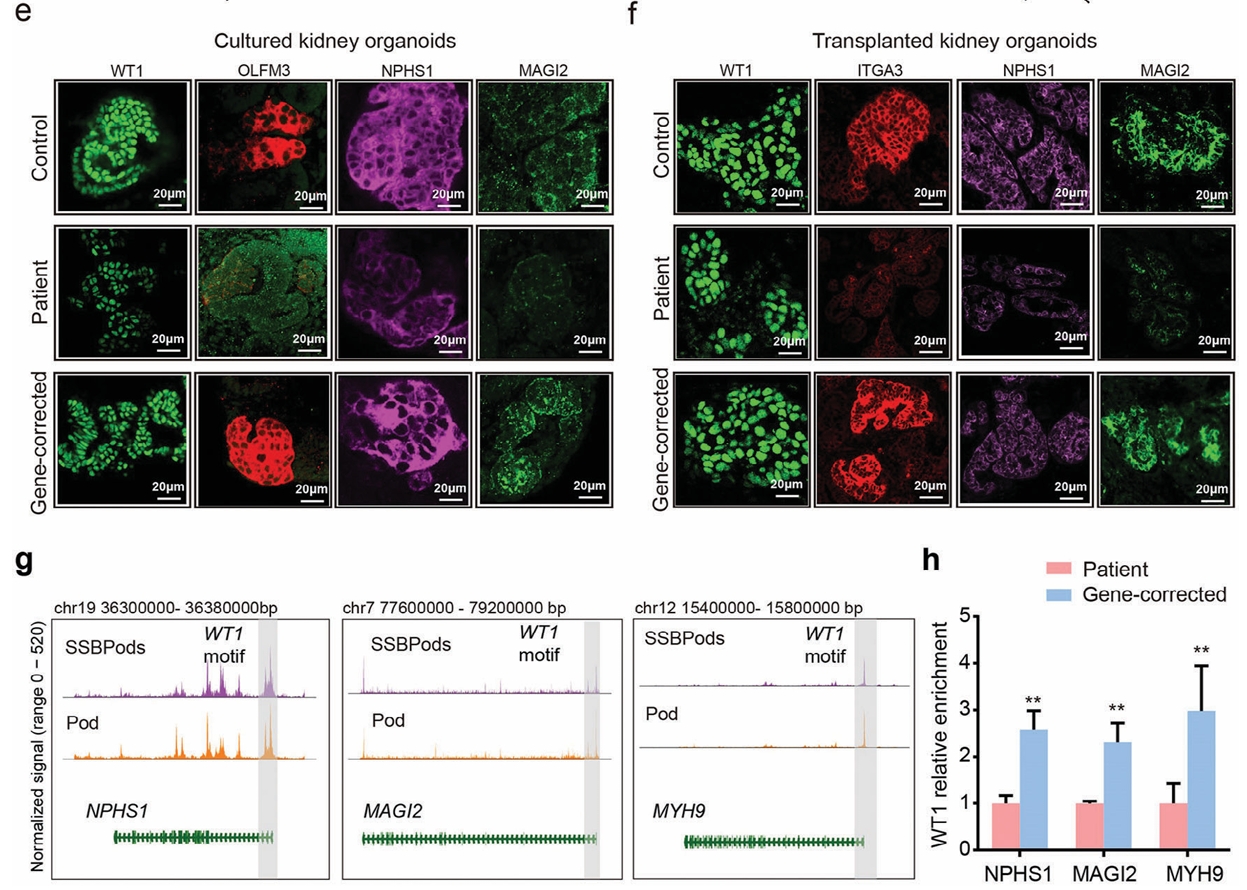
(点击图片可放大)
及疾病模型构建
文献名称:Long-term expandable mouse and human-induced nephron progenitor cells enable kidney organoid maturation and modeling of plasticity and disease
发表期刊:Cell stem cell(IF 20.4)
发表日期:2024年6月刊
研究团队:美国南加州大学凯克医学院李中伟教授团队
研究概要:
本研究通过调控p38和YAP信号通路活性,成功实现了原代小鼠和人类肾祖细胞(NPCs)以及来源于人类多能干细胞(hPSCs)的诱导肾祖细胞(iNPCs)的长期克隆性扩增。分子分析表明,培养的iNPCs在转录特征上高度接近原代人类肾祖细胞。利用iNPCs生成的肾脏类器官具有更少的非靶细胞类型和更高的足细胞成熟度。值得注意的是,该培养体系还揭示了足细胞的可塑性,使其能够重编程为类肾祖细胞状态。借助该平台的可扩展性和易于基因编辑的特点,研究进行了全基因组CRISPR筛选,鉴定了多个与肾脏发育和疾病相关的新基因。此外,利用该平台构建的常染色体显性多囊肾病(ADPKD)模型成功筛选出一种能够抑制囊肿形成的小分子化合物。该研究为肾脏发育、疾病机制、细胞可塑性和再生医学研究提供了广泛应用前景的新平台。
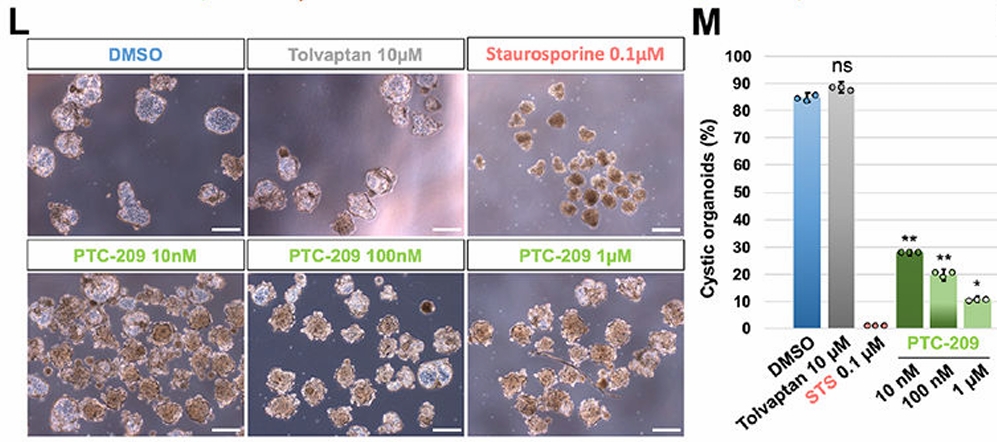
(点击图片可放大)
遗传学及多囊肾病治疗策略
文献名称:Genetics of cystogenesis in base-edited human organoids reveal therapeutic strategies for polycystic kidney disease
发表期刊:Cell stem cell(IF 20.4)
发表日期:2024年4月4日
研究团队:美国华盛顿大学医学院Benjamin S Freedman团队
研究概要:
本研究利用CRISPR碱基编辑技术在人类多能干细胞中构建了四种常见无义突变的等位基因系列。分化形成的肾脏类器官中,纯合突变体自发形成囊肿,而杂合突变体(无论是原始突变株还是碱基修复株)均无囊肿表型。基于该模型,研究鉴定出真核核糖体选择性糖苷(ERSGs)作为多囊肾病的潜在治疗药物,这类药物通过促进核糖体通读无义突变,部分恢复多囊蛋白表达,不仅能预防囊肿形成,还能限制已形成囊肿的生长。此外,糖苷类药物在类器官和小鼠模型中均富集于囊肿上皮细胞。该研究明确了人类多囊蛋白的阈值效应可作为药物或基因治疗的可干预靶点,为理解疾病机制和未来临床试验提供了重要依据。
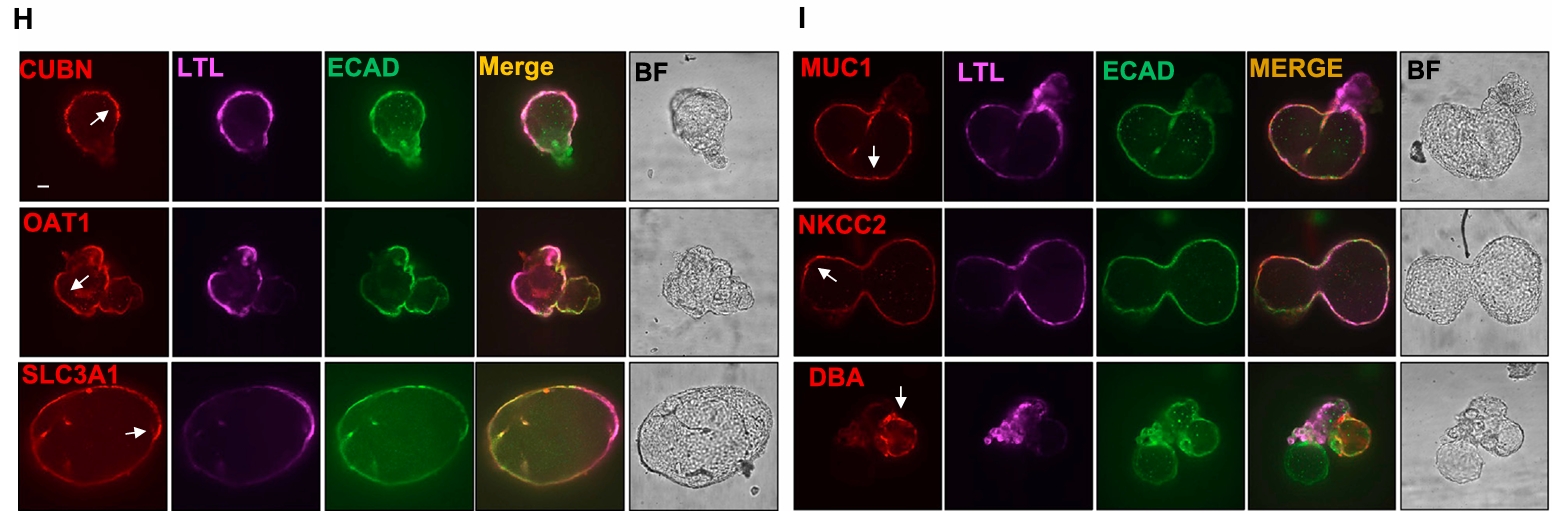
(点击图片可放大)
传统模型难以完全模拟人类肾脏病理特征。肾脏类器官作为三维人源微组织,为遗传性肾脏疾病研究提供了更具生理相关性的实验平台。前述五项研究展示了CRISPR联合类器官技术的应用价值:
如前述五项研究所示,肾脏类器官在以下方面有参考价值:
机制解析:在人类iPSCs中引入致病突变,观察基因变异对肾脏细胞的影响,如WT1突变导致足细胞发育延迟、KCNJ16缺陷重现肾小管病变。
药物评估:利用疾病类器官筛选候选药物,如他汀类药物逆转脂质积聚、ERSGs抑制囊肿形成,为相关疾病治疗提供新方向。
基因治疗验证:类器官平台验证基因修复可行性,如碱基编辑修复杂合突变逆转囊肿、CRISPR纠正WT1突变恢复足细胞表型。
功能筛选:结合全基因组CRISPR筛选,高效鉴定肾脏发育和疾病相关新基因,为发现治疗靶点提供技术支持。
将具备关键肾脏结构与细胞特征的类器官,与精准基因编辑技术相结合,为机制研究提供了可设计、可验证的创新平台。
华津肾脏类器官Kidnioid®平台在此领域提供专业支持:
▸ 方案咨询:针对类器官构建与基因编辑策略提供专业建议
▸ 实验实施:承接基因编辑、类器官培养
▸ 数据支持:提供规范的实验流程与可验证的数据结果
基于华津Kidnioid®平台在肾脏类器官培养和基因编辑领域的技术积累,华津Kidnioid®平台能够确保模型构建的规范性和实验结果的可靠性。
肾脏类器官模型
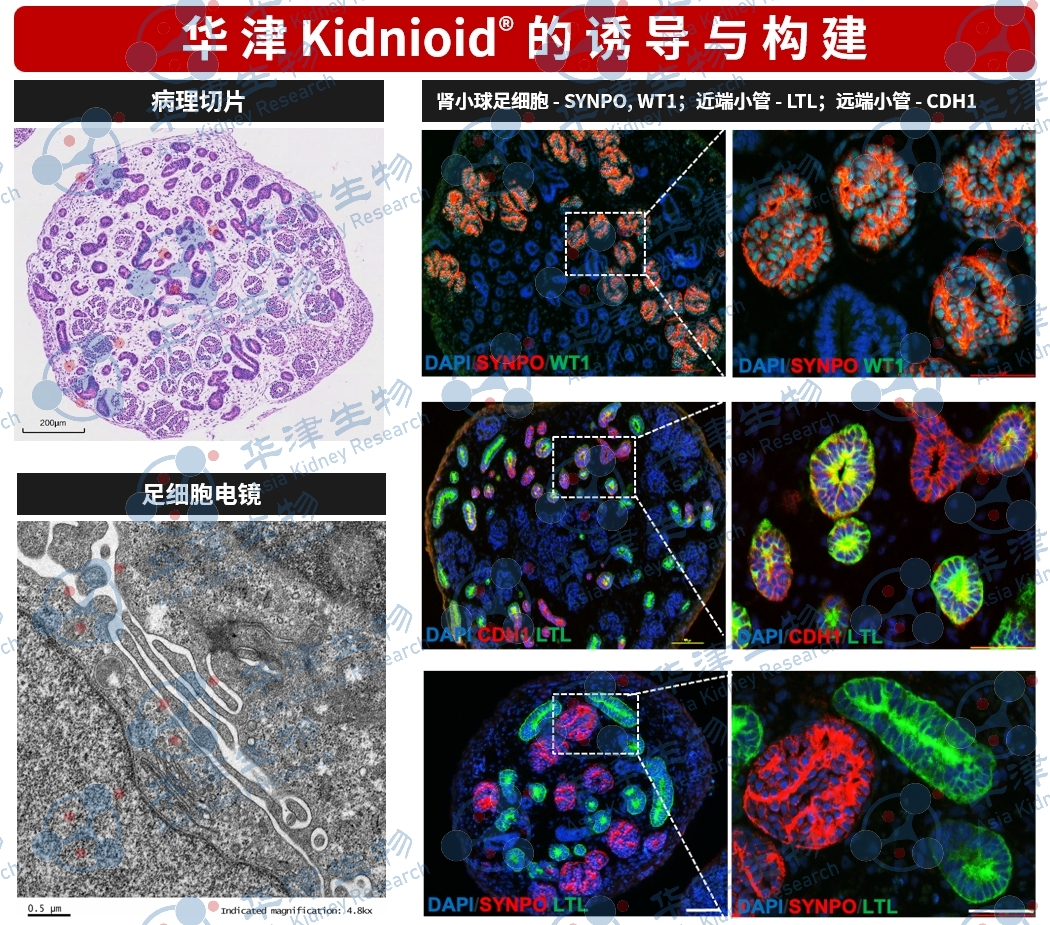
基于人源肾脏类器官构建,包含近端小管、足细胞等功能结构,能够模拟疾病相关的病理变化。
该模型可支持:
药物作用机制的系统研究
多信号通路的协同分析
细胞-药物相互作用评估
适用于药物筛选、毒性评估、疾病机制研究及个性化医疗等多个方向。
周期较短:相比部分动物实验,模型构建与评估时间有所缩短。
可重复性较好:在标准化培养条件下,模型稳定性较高。
灵活性较强:可根据研究需求进行定制化调整。
检测体系适配性高:与常规分子生物学/细胞生物学方法高度兼容,可直接开展qPCR、Western blot、免疫荧光等检测,便于机制研究与多指标评价。
感谢您对本文的浏览。肾脏类器官作为前沿生物技术,不仅在疾病模拟、药物筛选和再生医学研究中展现出巨大潜力,也为精准医疗和新药研发提供了更可靠的平台。目前全球多家监管机构已将其纳入药物评价体系,标志着该技术正逐步走向标准化与应用化。如果您希望进一步了解肾脏类器官的技术细节、合作研究或商业应用,欢迎随时联系咨询:
商务支持 - 李老师 17276665437
技术支持 - 田老师 18843183823
我们期待为您提供专业服务与合作支持。


