
慢性肾脏病影响着全球超过10%的人口,而现有治疗手段——透析与肾移植——分别面临着长期并发症和供体短缺的严峻挑战。近年来,人诱导多能干细胞来源的肾脏类器官技术为这一困境带来了新的希望。然而,类器官的血管化不足和功能不成熟,正成为其临床转化的主要瓶颈。
2026年2月发表于Journal of Artificial Organs的综述文章《Vascularization and maturation of kidney organoids: a comprehensive review of technological trends and challenges》,由Nishimura教授团队完成,系统梳理了肾脏类器官血管化与成熟化的技术进展、比较了不同策略的优势与局限,并对未来发展方向进行了深入展望。本文将为读者解读这篇综述的核心观点。
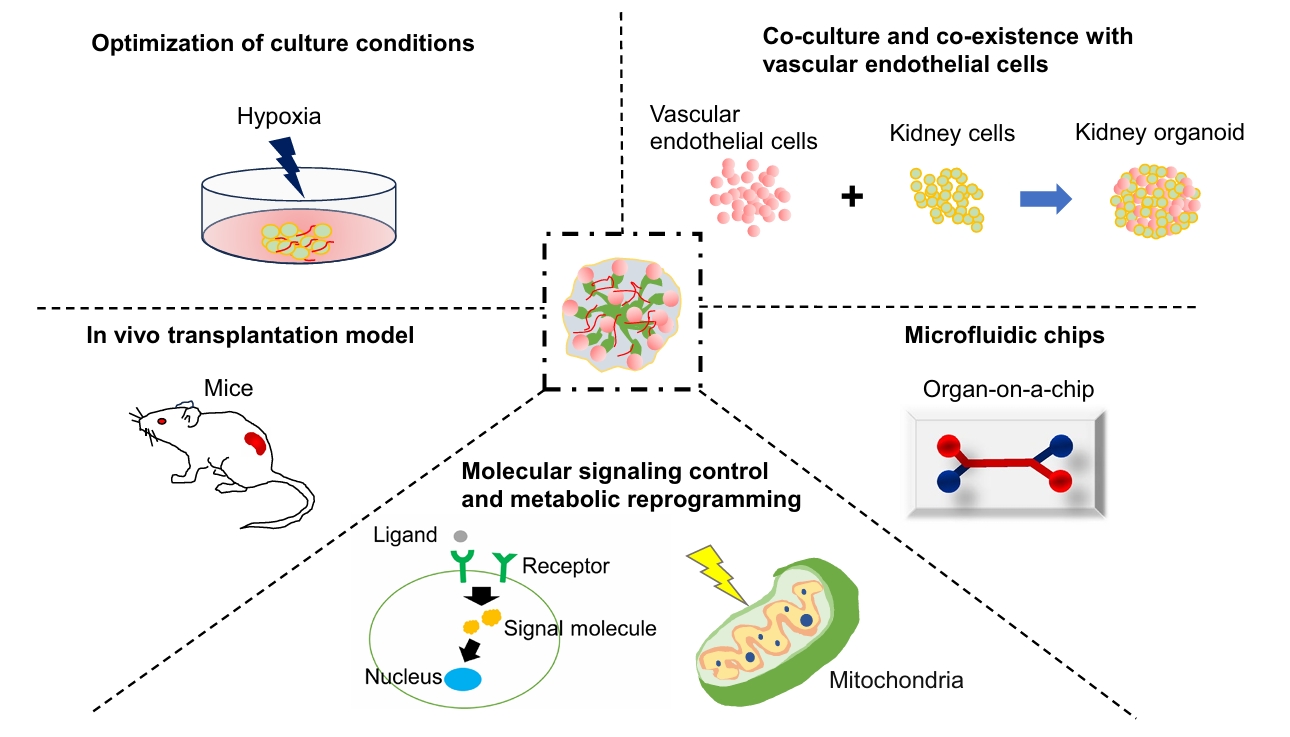
肾脏类器官的血管化是模拟肾小球滤过功能和肾小管重吸收功能的前提。当前主流策略包括低氧培养、体内移植、生物材料与微流控系统、以及基因调控等,各具特色,也各有局限。
低氧培养是一种相对简便可控的策略。研究表明,在约7%氧浓度的生理性低氧条件下培养类器官,可上调VEGF-A等血管生成因子的表达,促进内皮细胞形成管状结构,进而构建更为复杂的血管网络。这一方法的优势在于完全在体外完成,无需依赖动物模型。然而,所形成的血管结构是否具备功能性灌注能力、是否影响间质细胞和免疫细胞的成熟、以及长期培养的安全性,仍有待验证。
体内移植模型则通过将类器官植入免疫缺陷小鼠肾包膜下,借助宿主血管的浸润实现生理性血管网络的形成。该方法在促进肾小球成熟方面表现出色,但也面临样本量小、个体差异大、人源与鼠源血管难以区分、功能评估标准不统一等问题。
生物材料与微流控技术为血管化提供了空间精确控制和流体力学刺激的可能。3D生物打印可精确构建血管通道结构,微流控芯片可施加流体剪切力,二者结合已在促进肾小管成熟方面取得进展。但这类系统成本高、操作复杂、培养周期短,且难以完全复现肾脏特异性血管网络的复杂性,技术标准化尚待推进。
基因调控策略则追求更精准的分子层面控制。例如,通过ETV2诱导表达构建可调控的内皮微环境,不仅促进了多谱系细胞成熟,还成功诱导了肾素表达细胞的出现。然而,过度激活血管生成信号可能导致异常血管形成和细胞增殖失控,其致瘤风险和安全评估尚不充分。
下表总结了当前主要血管化策略的比较:
| 策略 | 优势 | 挑战/局限 |
| 低氧培养 | 简单可控, 完全体外完成 | 缺乏功能灌注评估; 长期效应未知 |
| 体内移植 | 可形成生理性 血管网络 | 个体差异大; 人源与宿主血管 难以区分 |
| 生物材料+微流控 | 空间精确控制, 可施加流体力学 刺激 | 成本高;周期短; 标准化难 |
| 基因调控 | 分子层面精准调控 | 致瘤风险; 安全性验证不足 |
血管化与成熟化是相互依存的两个过程。只有形成功能性血管网络,类器官才能获得充足的营养和信号支持,进而实现细胞分化和功能成熟。当前促进成熟化的策略主要围绕以下几个方面展开:
培养条件优化是基础性策略。通过模拟胎儿肾脏的低氧微环境(1-5%氧浓度),可减少氧化应激,促进成熟标志物表达。同时,调整培养基中葡萄糖和脂质代谢相关成分,有助于细胞能量代谢的正常化。然而,长期培养往往伴随结构退化和未分化细胞扩增,需要开发适宜的3D基质和支撑材料。
与血管化的协同推进是核心路径。内皮细胞不仅提供营养,还通过分泌生长因子和信号分子,为邻近肾脏细胞提供诱导分化的“血管生态位”。研究表明,血管化程度更高的类器官,其肾小球成熟标志物(如Wt1、nephrin)表达水平和肾小管极性均显著提升。
分子信号调控是精准干预手段。Wnt和Notch信号通路在肾脏发育中决定细胞分化方向,通过瞬时激活Wnt或添加Notch配体,可促进肾小管细胞分化和肾小球细胞成熟。代谢重编程则是新兴方向,通过激活线粒体功能、促进脂肪酸氧化,可显著改善类器官的结构与功能成熟,但需警惕过度代谢刺激带来的细胞损伤。
生物反应器与力学刺激关注物理环境对细胞成熟的影响。微流控芯片中施加流体剪切力和压力刺激,可增强细胞骨架结构、细胞间连接和极性功能。将肾小管类器官整合至流速可控的芯片系统,已观察到重吸收能力和膜转运蛋白表达的提升。但肾脏复杂的压力和流型仍难以完全复现。
下表总结了成熟化策略的比较:
| 策略 | 优势 | 挑战/局限 |
| 培养条件 优化 | 模拟生理环境, 促进成熟 | 长期培养结构 易崩解 |
| 与血管化 协同 | 增强极性和 功能结构 | 依赖血管质量 |
| 分子信号 +代谢调控 | 精准促进 特定细胞成熟 | 过度刺激风险; 安全性评估不足 |
| 生物反应器+力学刺激 | 改善转运功能 和极性 | 难以复现 肾脏特异性流场 |
综述对不同技术路径进行了横向比较,明确指出:单一策略难以同时满足血管化与成熟化的多维需求,未来发展方向应是多因素、多层次的整合策略。
以内皮细胞共培养为例,该方法在体外可控性强、可诱导内皮腔形成,但形成的血管功能不完善,且难以诱导和维持血管支持细胞(如间质细胞、周细胞)。相比之下,体内移植虽能形成生理性血管网络,但无法评估人源特异性特征,且存在伦理争议和规模化难题。
生物材料和微流控技术虽可实现空间精确控制,但技术要求高、成本高、标准化程度低。分子调控策略可直接作用于细胞内成熟开关,但安全性和长期效应尚不明确。
因此,构建整合多种细胞类型(包括神经和免疫细胞)的共培养系统、发展高精度3D生物打印与微流控技术、建立统一的成熟度评估标准、验证长期功能与安全性,成为未来研究的核心方向。
肾脏类器官血管化与成熟化技术正处于从结构模拟向功能重建乃至临床转化的关键时期。低氧培养、体内移植、微流控芯片、基因调控等多策略的并行发展,标志着该领域已进入多技术融合、多维度整合的新阶段。随着诱导多能干细胞技术、3D生物打印平台及微流控芯片系统的深度融合,未来有望构建出血管网络完整、功能成熟的肾脏类器官,最终为慢性肾病患者带来真正意义上的再生医学治疗新希望。
参考文献:
Nishimura Y. Vascularization and maturation of kidney organoids: a comprehensive review of technological trends and challenges. J Artif Organs. 2026 Feb 5;29(1):18.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

