慢性肾脏病(CKD)的进展与细胞衰老密切相关。衰老的肾细胞会获得稳定的细胞周期停滞,并分泌促炎及促纤维化因子(SASP),进而驱动肾脏纤维化和功能丧失。然而,传统模型在模拟人类肾脏衰老过程方面存在局限。例如,动物模型与人类存在种属差异,而二维培养的细胞难以维持长期培养以模拟慢性衰老过程,且缺乏细胞间及细胞与基质的复杂相互作用。
近年来,肾脏类器官技术的发展,在一定程度上弥补了这些不足,为研究肾脏细胞衰老机制及开展药物筛选提供了新的平台。本文从模型选择、机制发现及干预策略三个角度,对相关研究进展进行梳理。
类肾小管模型:模拟反复损伤诱导的细胞衰老与纤维化
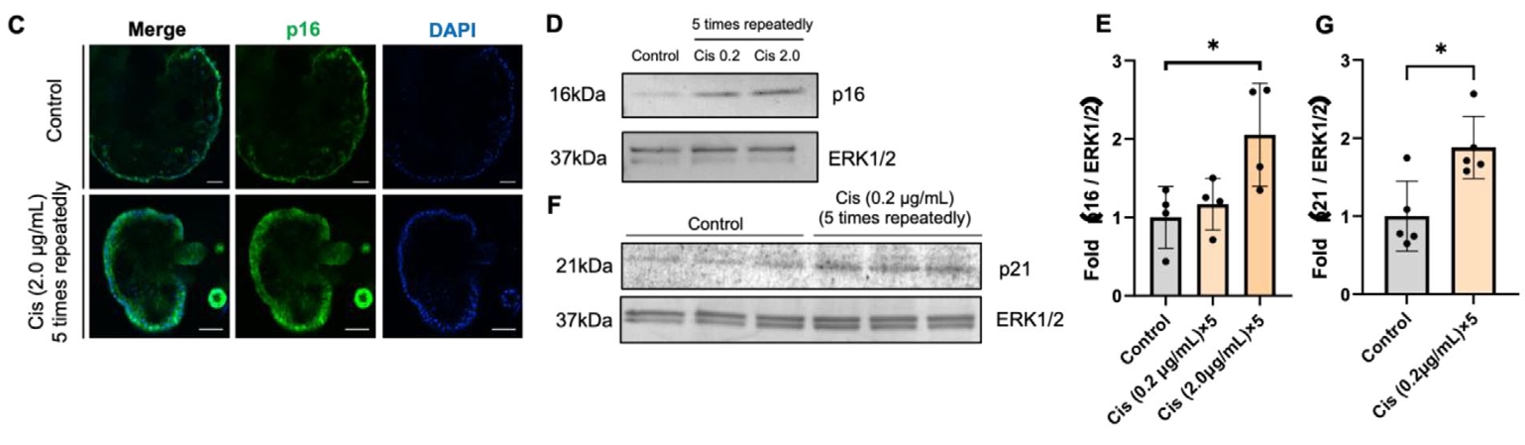
研究概要:本研究利用原代肾小管上皮细胞构建了类肾小管(Tubuloid)模型。通过反复给予顺铂处理,模拟了慢性肾损伤。结果显示,反复损伤导致类器官中衰老标志物(p16, p21)上调,并分泌SASP因子。这些衰老类器官的上清液能够激活成纤维细胞,提示其促进了早期纤维化改变。该模型可用于研究肾小管上皮细胞在重复性应激下的衰老反应及筛选抗衰老药物。
靶向NNMT:抑制肾小管衰老与纤维化的新策略
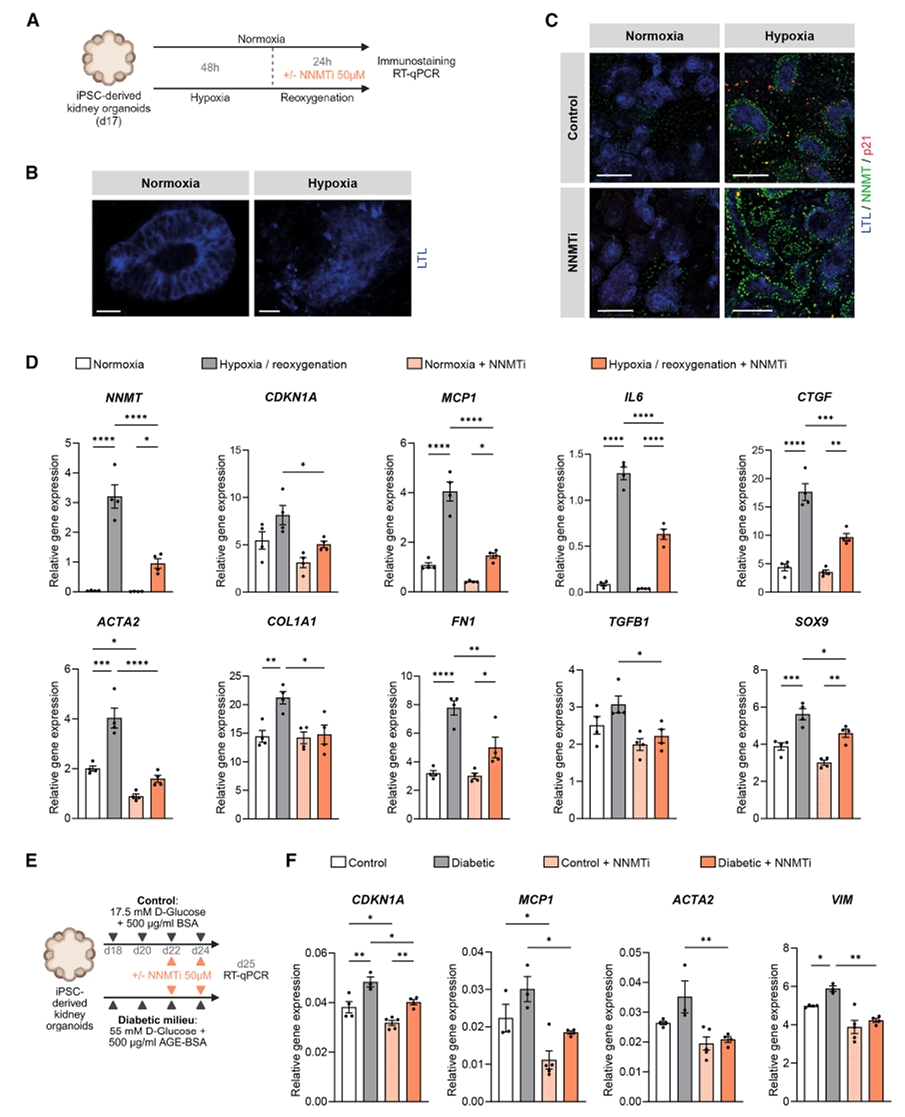
研究概要:该研究通过分析人类CKD数据,发现NNMT是驱动肾小管衰老和纤维化的关键介质。在糖尿病肾病患者活检组织及肾脏类器官中,NNMT表达与衰老标志物p21及纤维化相关。空间转录组学显示,NNMT阳性肾小管周围存在促炎微环境。选择性抑制NNMT,在衰老肾细胞、肾脏类器官和小鼠体内均能减轻衰老和纤维化。该研究将NNMT作为早期CKD治疗的潜在靶点。
血小板通过TGF-β信号通路诱导细胞周期停滞与纤维化
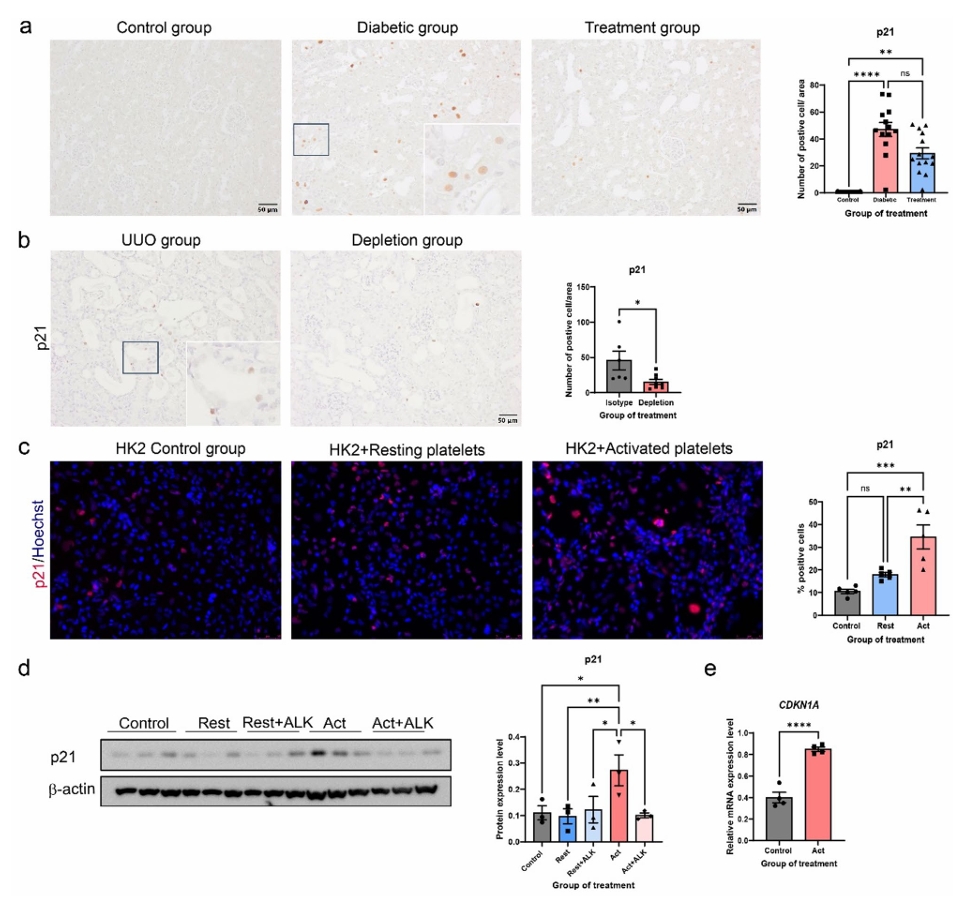
研究概要:本研究通过小鼠模型和肾脏类器官共培养体系,发现活化的血小板通过释放TGF-β1,诱导肾小管上皮细胞表达细胞周期停滞标志物p21,并促进其发生部分EMT和纤维化。使用TGF-β受体抑制剂可逆转这些表型。该研究提示血小板-TGF-β1轴在诱导肾小管细胞周期停滞和纤维化中具有一定作用。
肾脏类器官与类肾小管模型的比较分析:为衰老研究提供模型选择依据
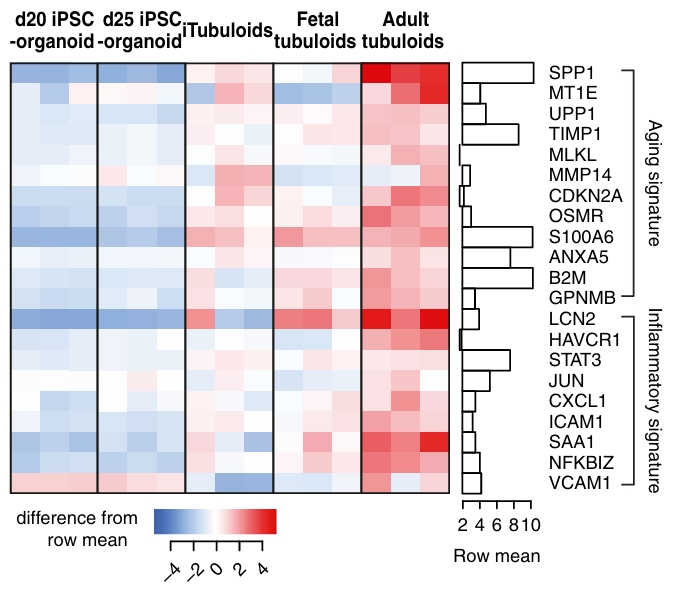
研究概要:本研究对不同来源的肾脏类器官模型进行了转录组比较。结果显示,源自成人肾脏的类肾小管富集了较强的衰老和炎症相关基因表达特征,而iPSC来源的肾脏类器官则高表达近端小管标志物。功能验证显示,iPSC来源的类肾小管在经历重复性低氧损伤后,表现出适应不良性修复特征。该比较为模型选择提供了参考。
内皮自噬缺陷通过铁死亡和NLRP3炎症小体加速肾脏衰老
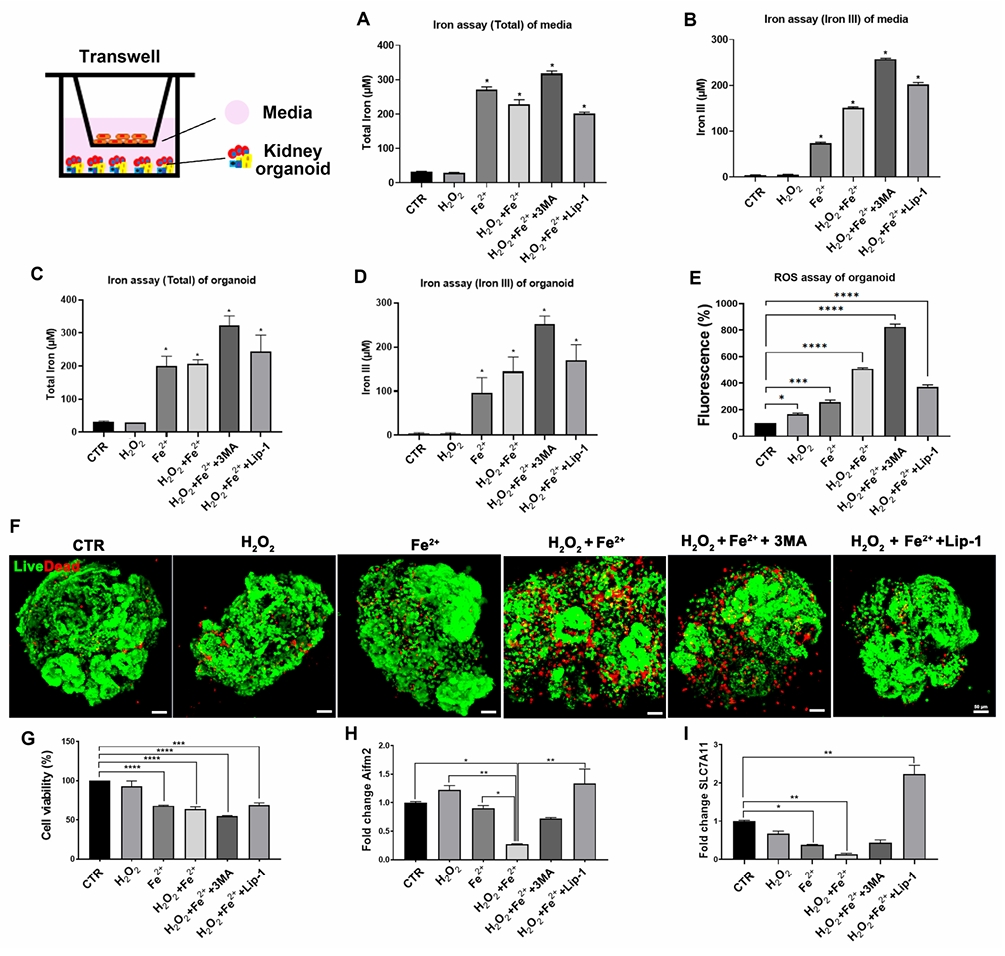
研究概要:本研究利用内皮特异性Atg7敲除小鼠和肾脏类器官-内皮细胞共培养系统,发现内皮自噬缺陷破坏了内皮屏障,导致铁离子泄漏至肾脏类器官,引发类器官细胞发生铁死亡,并激活NLRP3炎症小体信号通路,加速了肾脏衰老相关病变。使用铁死亡抑制剂liproxstatin-1可部分逆转这些损伤。
早年足细胞损伤诱导早熟衰老并加剧肾小球老化
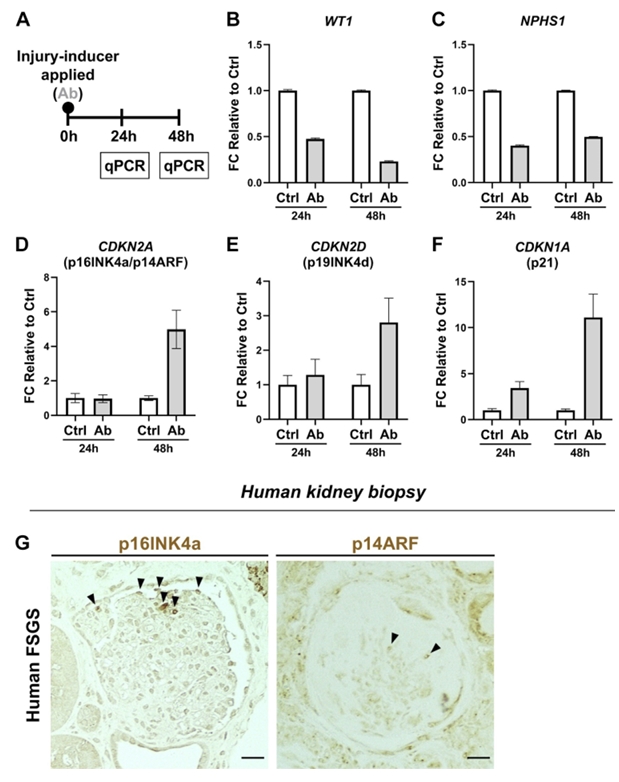
研究概要:该研究在足细胞和iPSC来源的肾脏类器官中证实,药物诱导的损伤可直接上调衰老相关基因(p16, p21)。在年轻时诱导FSGS的小鼠模型中,损伤引发了足细胞衰老。长期追踪显示,年轻时受过损伤的小鼠在中年期表现出更明显的足细胞衰老、密度降低和肾小球硬化。
应用肾脏类器官研究细胞衰老的研究价值
肾脏类器官来源于人源细胞(如iPSC或原代肾上皮细胞),包含肾小管、足细胞等功能结构,可在体外模拟衰老相关的细胞周期停滞、SASP分泌等变化。与动物模型相比,其遗传背景更接近人类;与二维培养相比,其三维结构更接近体内组织环境。
类器官可支持长期培养和反复应激处理(如多次顺铂或低氧暴露),适用于模拟慢性肾脏病中损伤累积和修复过程。通过共培养体系,还可观察不同细胞类型(如内皮细胞与上皮细胞)在衰老过程中的相互作用。
在类器官水平可检测衰老相关标志物(如p16、p21)及铁死亡、炎症通路的变化。结合基因编辑或药物干预,可用于筛选和评估潜在抗衰老策略的效应。
肾脏类器官在一定程度上有别于传统模型:与动物模型相比,其更接近人类细胞背景;与二维培养相比,其结构更完整。可作为现有研究体系的补充工具。
将肾脏类器官与细胞衰老研究相结合,为探索肾小管上皮细胞衰老及纤维化机制提供体外验证平台。
▸ 模型构建:提供人源iPSC来源肾脏类器官模型
▸ 方案咨询:针对衰老研究需求提供模型选择与实验设计建议
▸ 实验实施:承接损伤建模、基因编辑及药物干预实验
▸ 数据支持:提供规范的实验流程与可验证的数据结果
基于华津Kidnioid®平台在肾脏类器官培养和细胞衰老研究领域的技术积累,能够确保衰老模型构建的规范性和实验结果的可靠性。
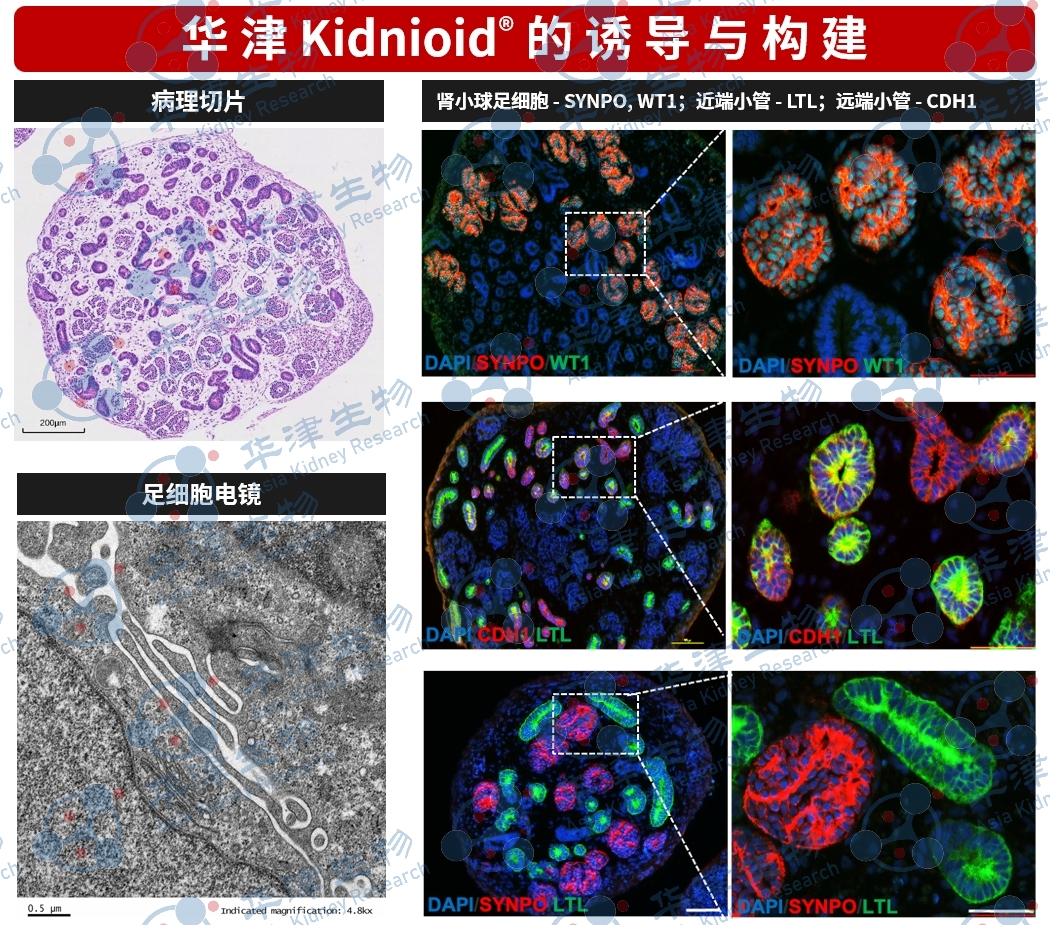
图1. 经病理切片、电镜及免疫荧光鉴定,该肾脏类器官可观察到肾小球与肾小管结构,电镜下可见足细胞足突形态,免疫荧光染色显示足细胞、近端小管及远端小管的定位特征。
基于人源肾脏类器官构建,包含近端小管、足细胞等功能结构,能够模拟疾病相关的病理变化。
该模型可用于对药物作用机理进行系统分析,研究多信号通路间的相互作用,并评估细胞与药物之间的相互影响。
该模型主要应用于药物筛选、毒性评估及疾病机制研究等方向。
周期较短:相比部分动物实验,模型构建与评估时间有所缩短。
模型稳定性较好:在标准化培养条件下,模型稳定性较高。
灵活性较强:可根据研究需求进行定制化调整。
检测体系适配性高:与常规分子生物学/细胞生物学方法高度兼容,可直接开展qPCR、Western blot、免疫荧光等检测,便于机制研究与多指标评价。

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

