近日,美国哈佛大学医学院附属麻省总医院的研究团队在NPJ Biomedical Innovations上发表研究,成功开发出可规模化生产的血管化肾类器官平台,生产效率提升超50倍,并在活体小鼠中证实其具备功能性滤过能力。
慢性肾脏病患者数量持续攀升,对肾脏替代疗法的需求日益迫切。尽管人多能干细胞来源的肾类器官为疾病研究和治疗带来希望,但传统静态培养体系劳动密集、成本高昂且缺乏功能性血管化,严重限制了其大规模应用。
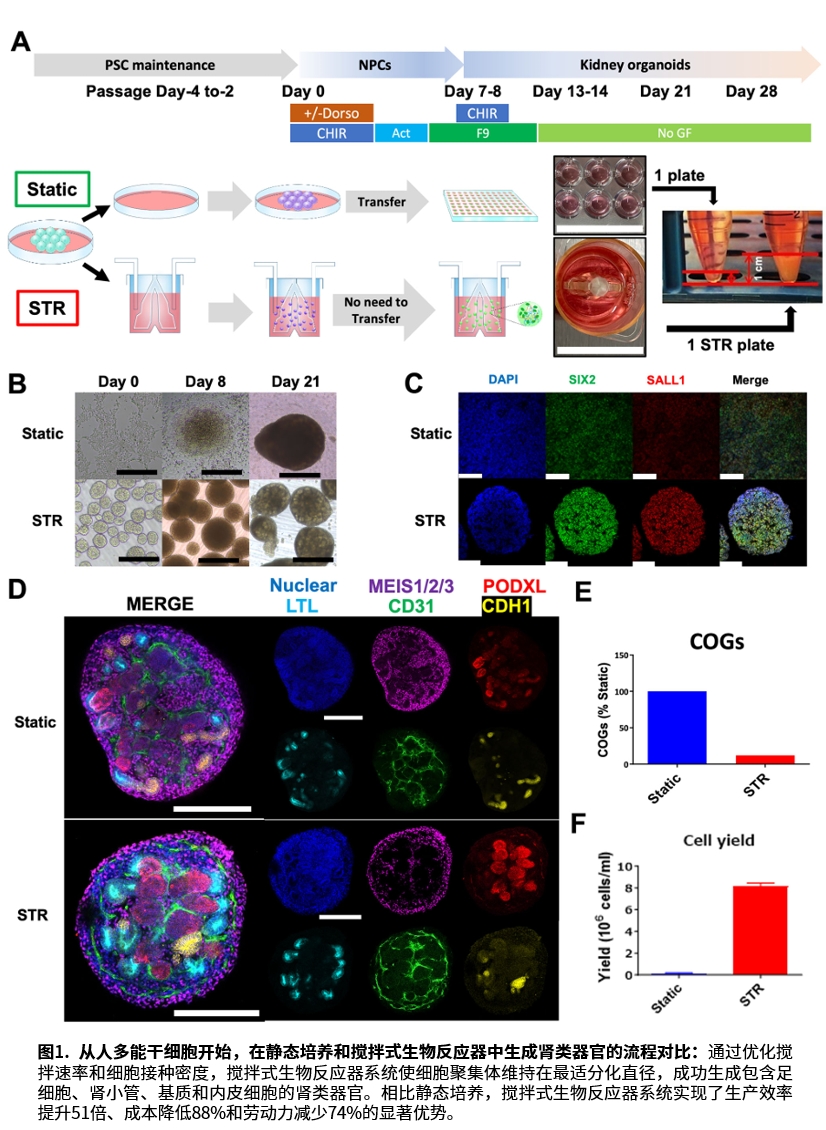
研究团队采用三角翼搅拌式生物反应器,通过精确调控搅拌速率,使细胞聚集体维持在最佳分化直径,实现了生产效率提升51倍、成本降低88%、劳动力减少74%的重大突破。
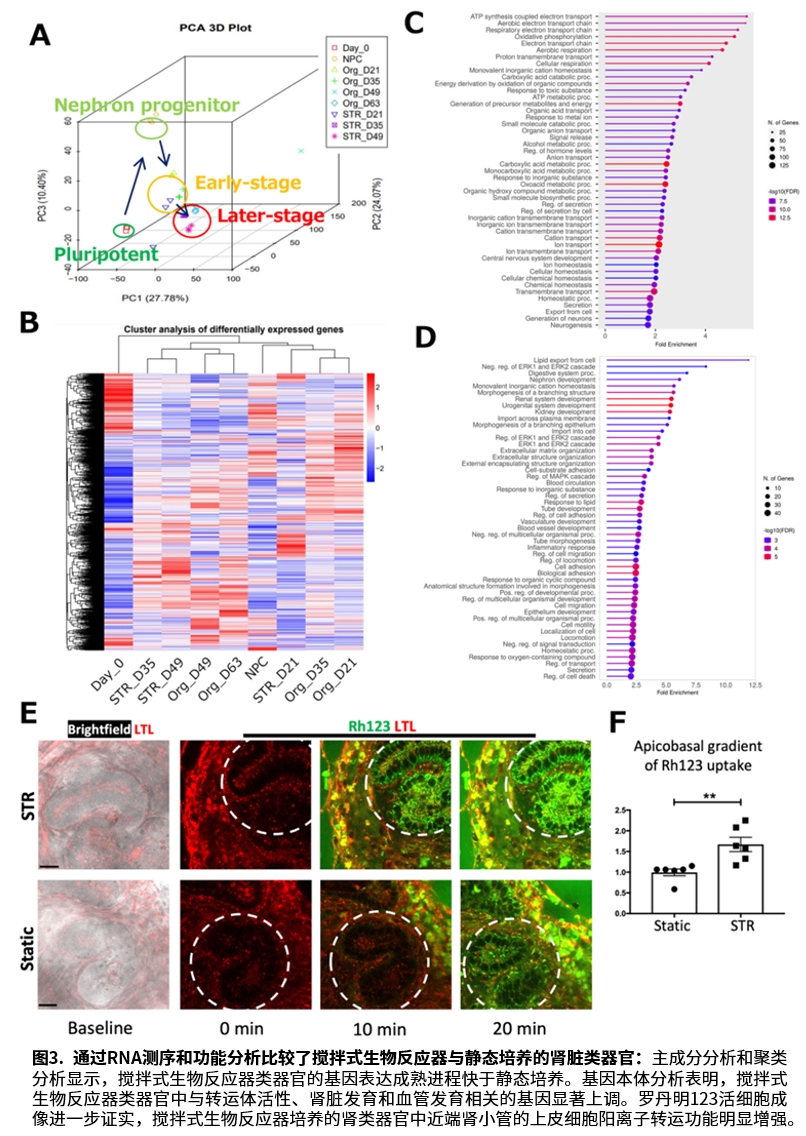
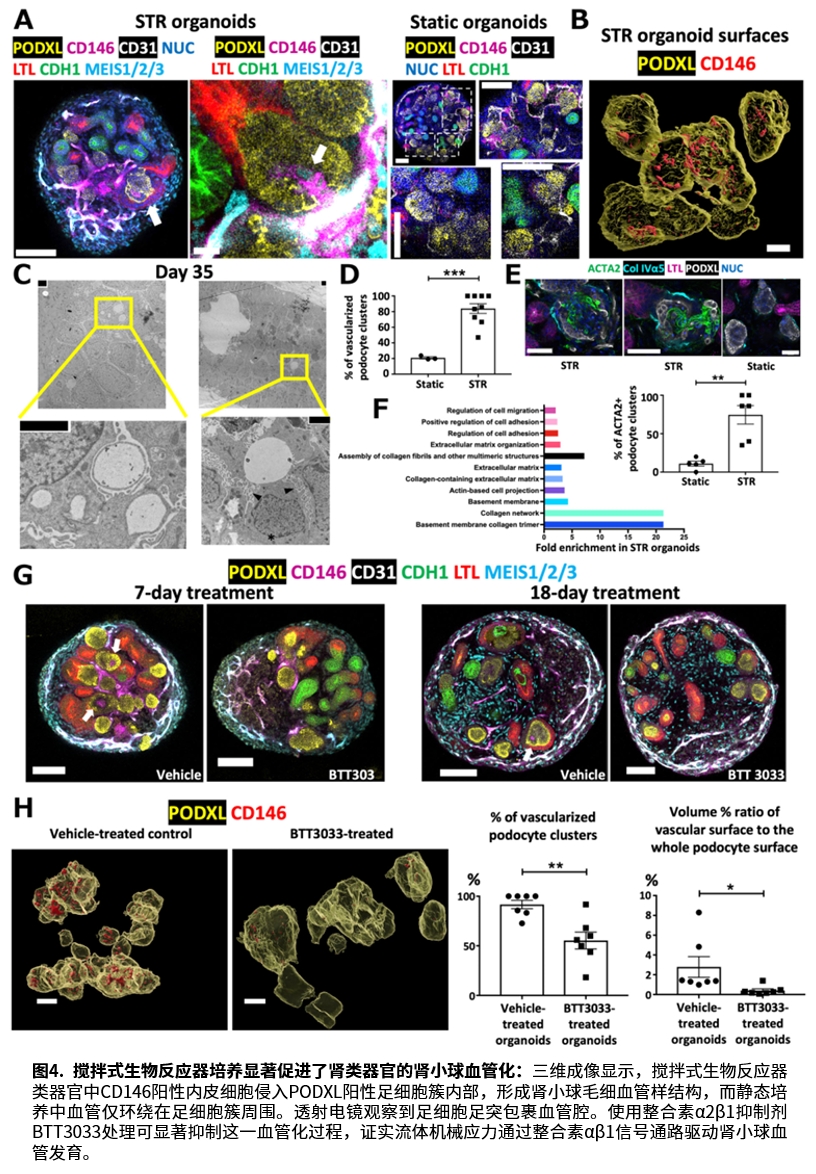
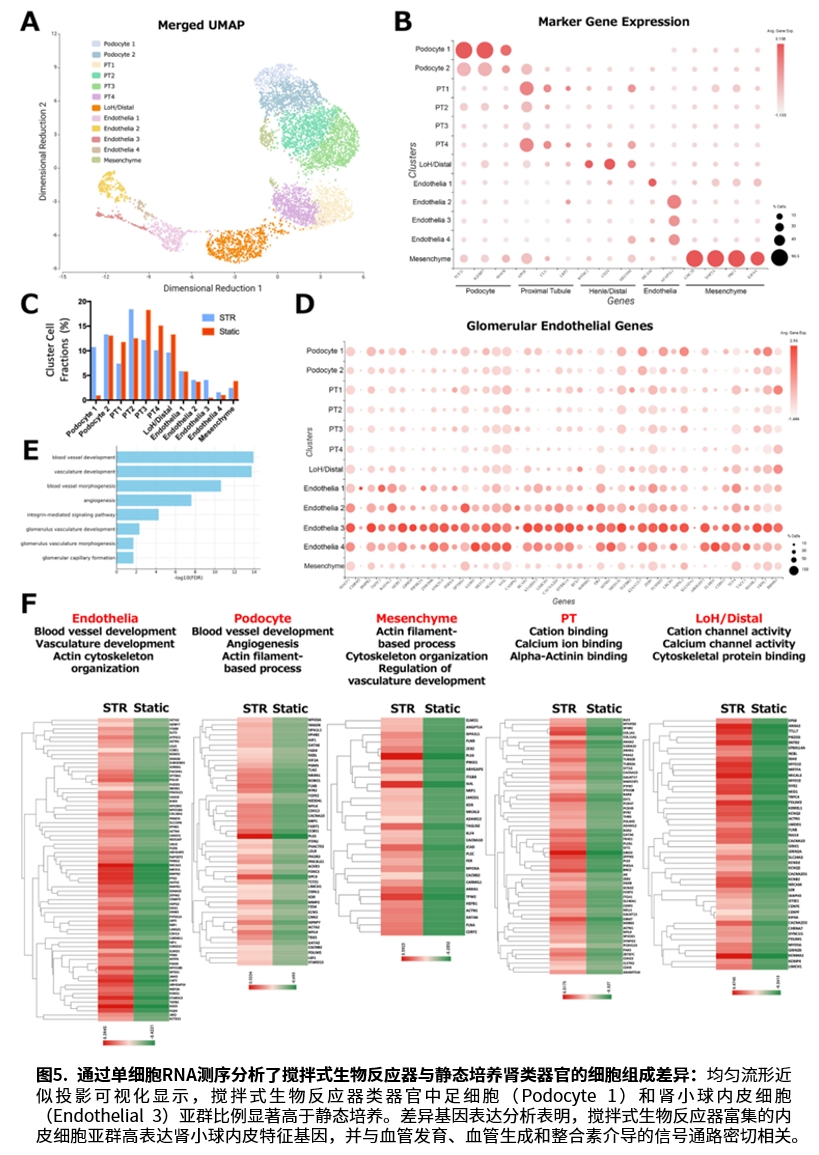
研究发现,流体机械应力通过整合素αβ1信号通路显著促进肾小球血管化。单细胞测序显示,生物反应器培养的类器官中肾小球内皮细胞和足细胞比例明显升高。透射电镜更在类器官肾小球内观察到带足突的足细胞包裹人内皮细胞形成血管腔,这一结构是滤过功能的基础。
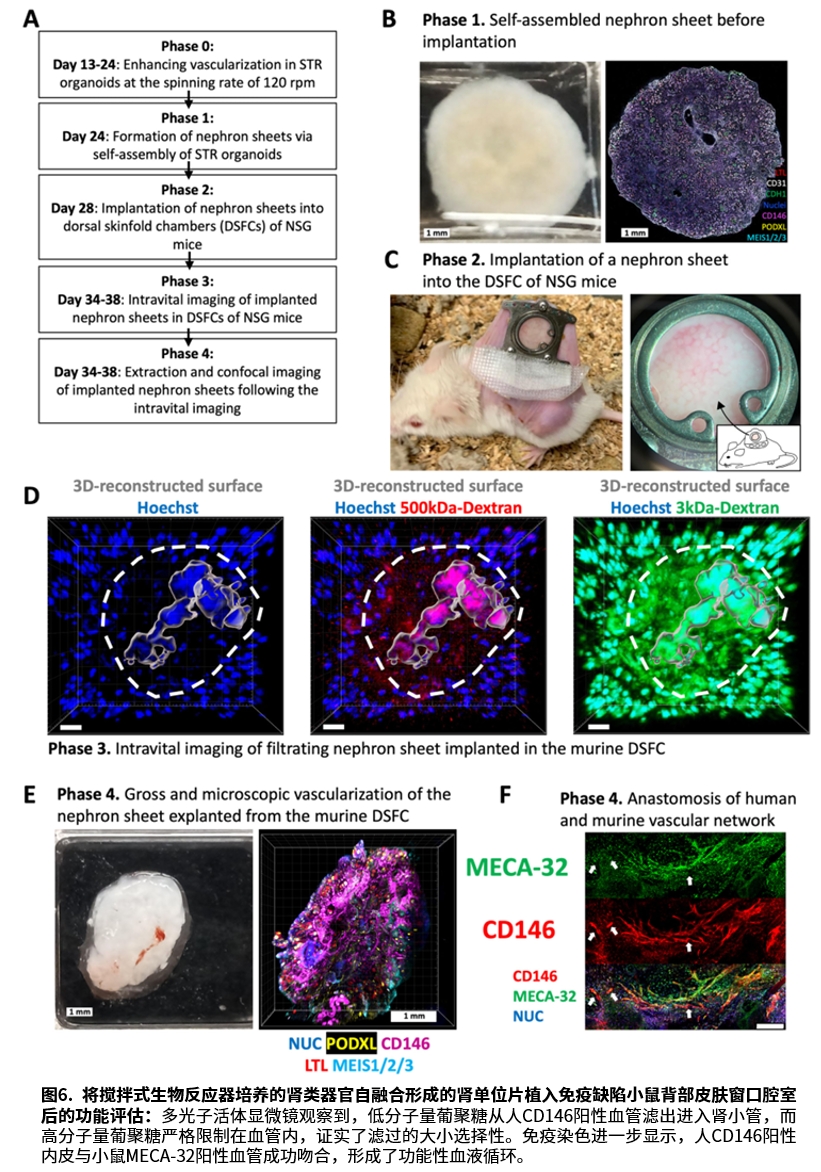
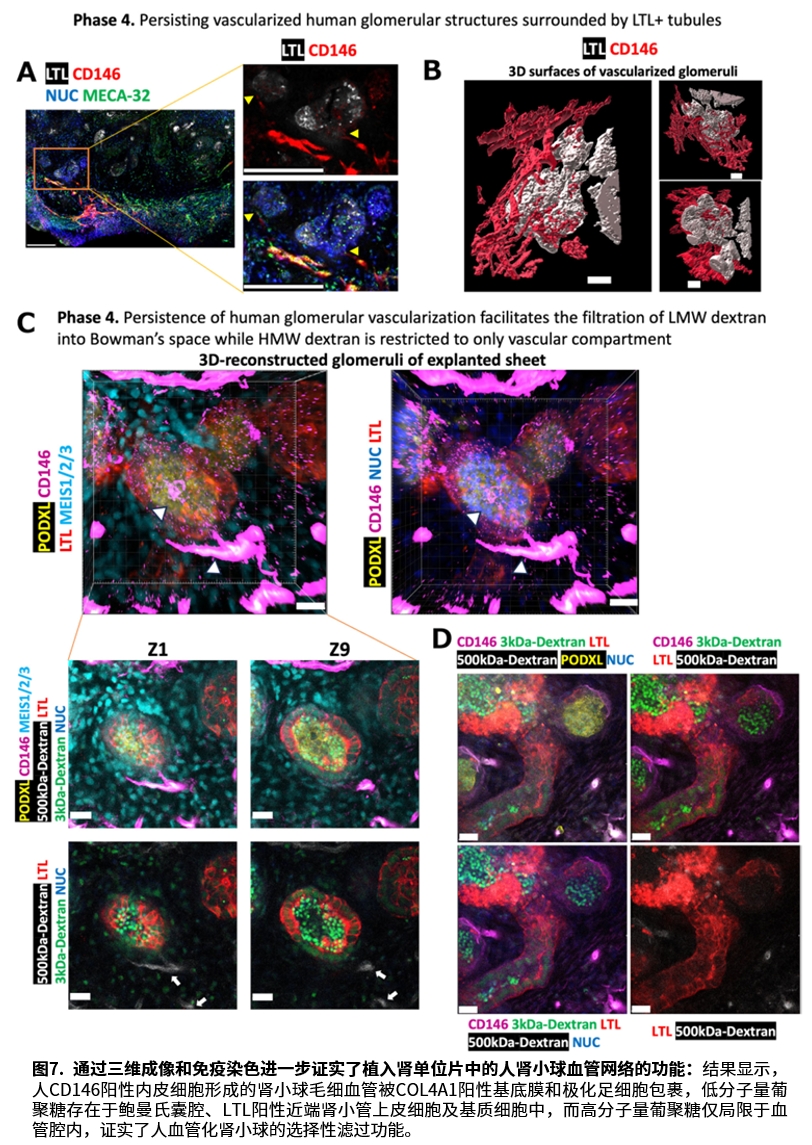
团队将约1533个肾类器官自融合成一张肾单位片,内含约4.6万个肾单位,相当于两个大鼠肾脏的肾单位数量。植入小鼠背部后观察到,低分子量葡聚糖从人CD146+血管滤出进入肾小管,而高分子量葡聚糖严格限制在血管内,证实了滤过的大小选择性。同时,人源内皮与小鼠血管成功吻合,形成了功能性血液循环。
该研究提供了一个成本低、可规模化、符合cGMP转化潜力的肾类器官平台,为药物筛选、疾病建模及最终实现生物人工肾迈出了关键一步。

参考文献:
Tekguc M, Matsumoto T, Altenburger LM, Kobayashi K, Hiratsuka K, Higashi Y, Rizki-Safitri A, Miyoshi T, El-Jouni W, Arnaout MA, Mempel TR, Morizane R. Engineering scalable vascularized kidney organoids for in vivo glomerular filtration with human endothelial integration. NPJ Biomed Innov. 2026;3(1):10.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

