近年来,糖尿病肾病(DKD)是糖尿病最常见的微血管并发症之一,也是终末期肾病的主要病因,其病理机制涉及代谢紊乱、炎症反应、细胞衰老与纤维化等多种因素的复杂交互作用。传统动物模型和二维细胞培养难以充分模拟人类肾脏的三维结构与疾病微环境,限制了机制研究和药物开发的进展。
人诱导多能干细胞来源的肾脏类器官可在体外重现肾脏的复杂结构与细胞多样性,为DKD研究开辟了新路径。本文梳理了近年利用肾脏类器官构建糖尿病损伤模型的研究进展,从高糖诱导的代谢重编程、组织固有炎症激活、上皮细胞脱落机制,到糖尿病环境对病毒感染易感性的影响等维度,展现该平台在模拟早期DKD病理特征、探索关键分子机制及筛选治疗靶点中的应用前景。
利用人诱导多能干细胞来源的肾脏类器官分析高糖损伤
文献名称:Analysis of high glucose injury using human induced pluripotent stem cell-derived kidney organoids
发表期刊:BMC Nephrology 发表日期:2026年1月8日 IF:-
研究团队:贵州省人民医院查艳团队
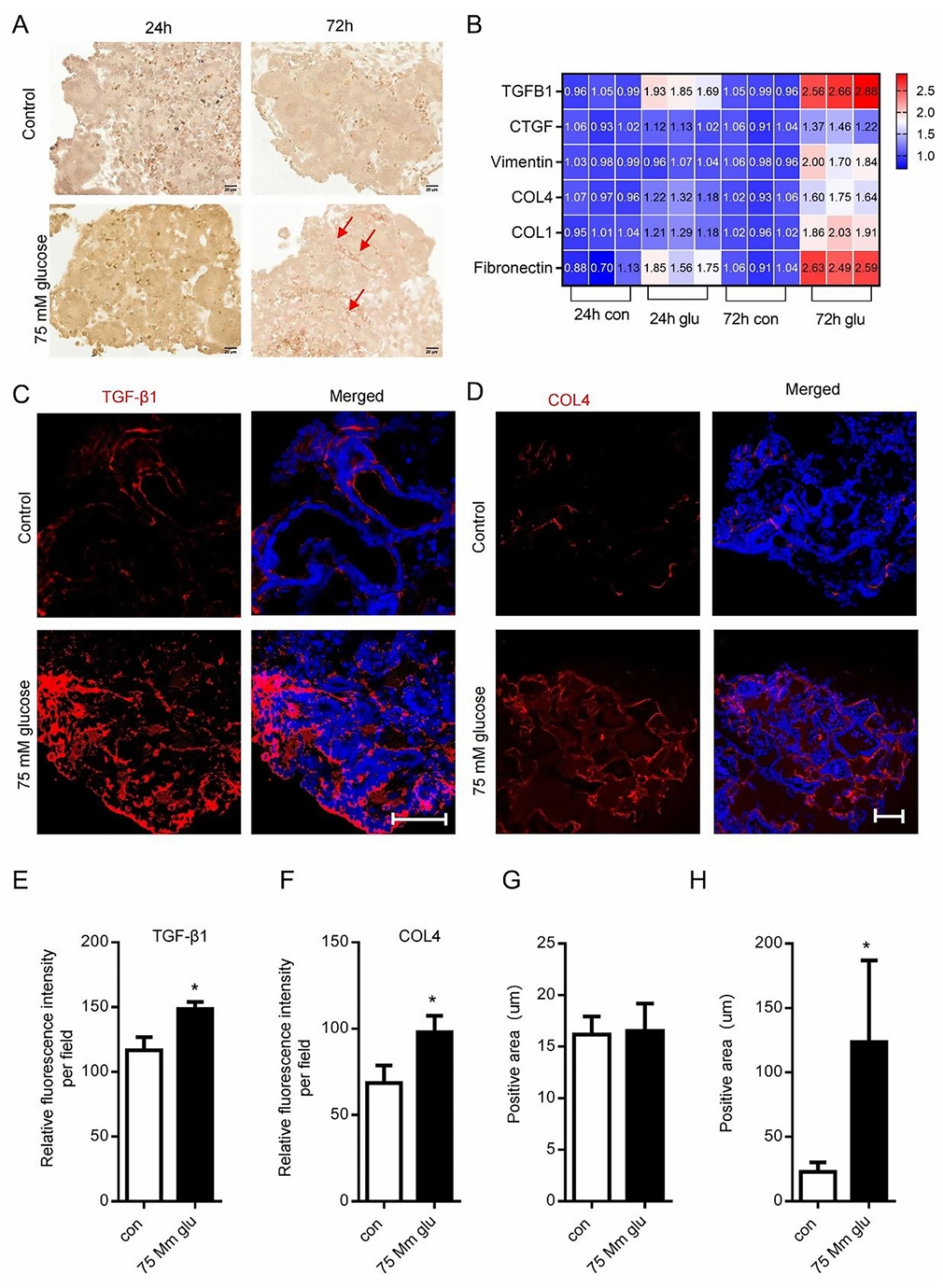
研究概要:本研究利用人多能干细胞来源的肾脏类器官建立糖尿病肾病(DKD)损伤模型,通过高糖干预24和72小时模拟DKD早期事件。结果显示:高糖干预后糖脂代谢相关基因(LDH、HK2、SGLT2等)表达上调;促炎细胞因子(IL6、IL1B、TNFA等)表达增加;肾损伤标志物KIM1上调,TUNEL实验证实凋亡细胞增加;纤维化相关分子TGF-β1和COL4表达增加。该研究成功建立了复现DKD关键特征(代谢紊乱、炎症、损伤、纤维化启动)的体外模型,为DKD机制研究和药物筛选提供了有价值平台。
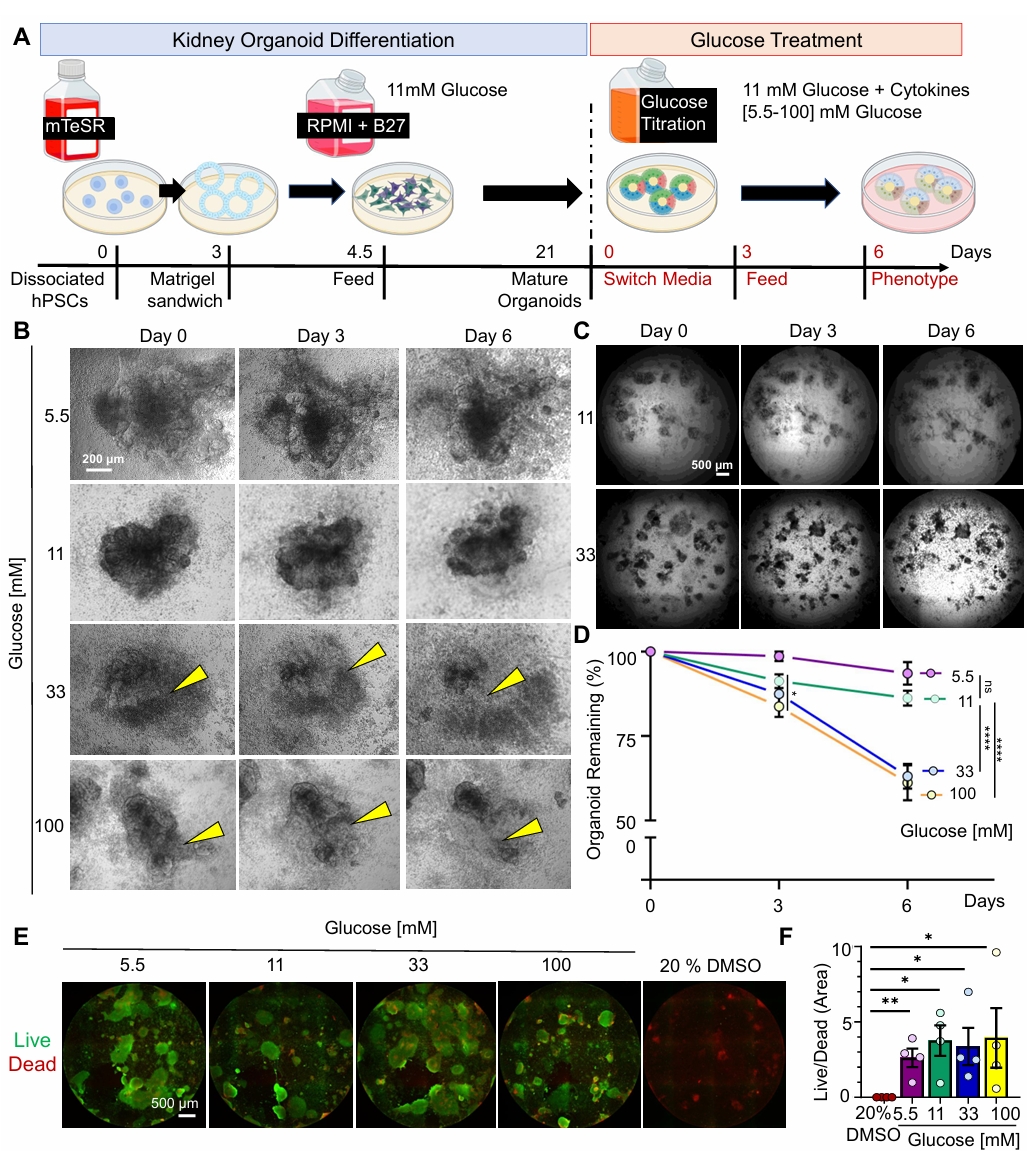
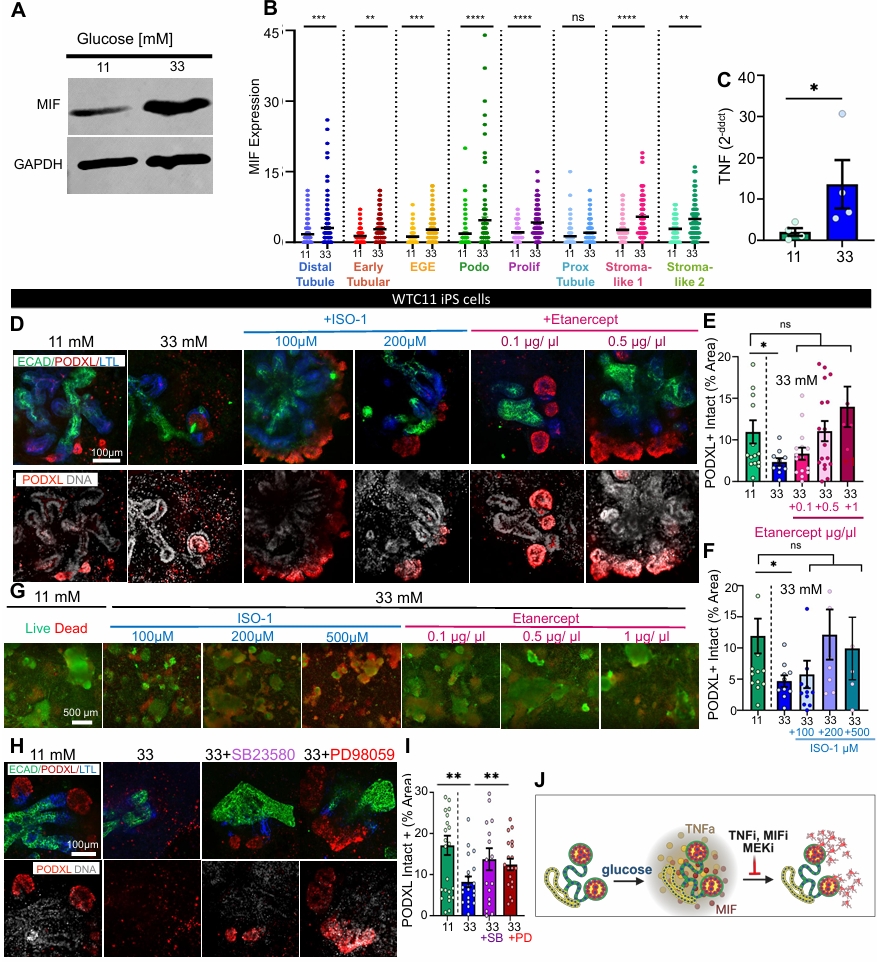
肾脏类器官中高糖诱导组织固有炎症驱动上皮细胞脱落
文献名称:Elevated glucose in kidney organoids induces tissue-intrinsic inflammation driving epithelial detachment
发表期刊:bioRxiv (预印本) 发表日期:2025年9月8日
研究团队:华盛顿大学Benjamin S Freedman团队
研究概要:本研究揭示了高糖导致糖尿病肾病中细胞脱落的新机制。人肾脏类器官经高糖处理后出现足细胞和肾小管细胞脱落表型,但无细胞毒性。转录组分析显示,高糖激活类器官内部炎症、信号传导和细胞粘附通路,与人类糖尿病肾脏变化高度相似。添加细胞因子使类器官对中等浓度高糖敏感,而炎症因子或信号通路抑制剂可挽救高糖表型。研究提出“组织固有炎症”新概念:高糖直接触发肾脏组织内部炎症级联反应,导致细胞粘附丧失和脱落,为靶向局部炎症治疗DKD提供了新思路。
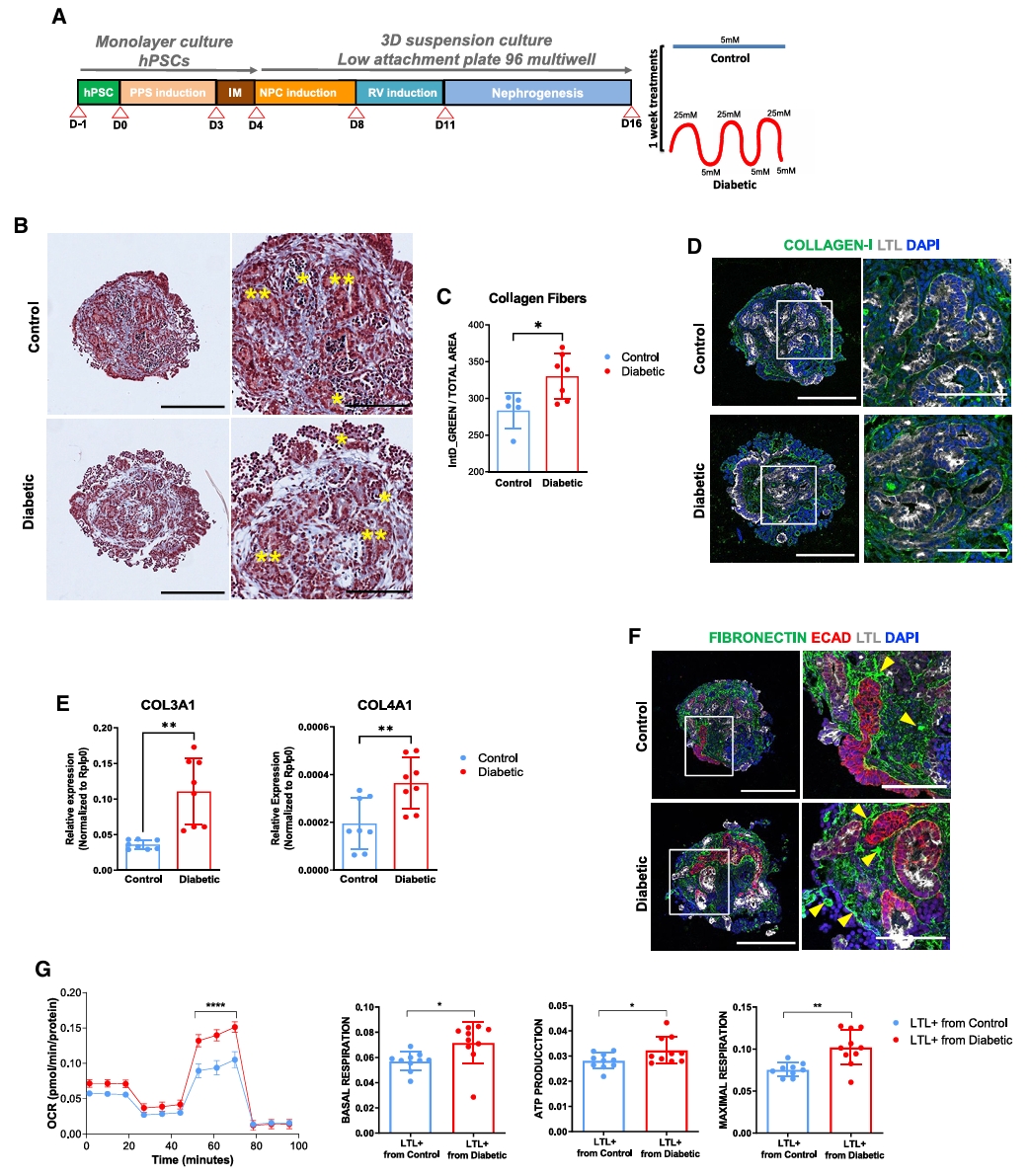
糖尿病环境增加ACE2表达和细胞对SARS-CoV-2感染的易感性
文献名称:A diabetic milieu increases ACE2 expression and cellular susceptibility to SARS-CoV-2 infections in human kidney organoids and patient cells
发表期刊:Cell Metabolism (IF 30.9) 发表日期:2022年6月7日
研究团队:西班牙加泰罗尼亚生物工程研究所Nuria Montserrat、奥地利科学院分子生物技术研究所Josef M Penninger等团队
研究概要:本研究揭示了糖尿病患者易感重症COVID-19的机制。通过建立具有早期糖尿病肾病特征的人肾脏类器官模型,发现SARS-CoV-2感染后糖尿病样类器官病毒载量显著高于对照组,这种易感性增加依赖于ACE2表达上调。从糖尿病患者肾活检组织分离的细胞表现出线粒体呼吸改变和糖酵解增强,导致更高的病毒感染率。使用有氧糖酵解抑制剂二氯乙酸处理可降低病毒感染。该研究首次揭示糖尿病诱导的肾脏代谢重编程是增加SARS-CoV-2感染易感性的关键事件,为靶向能量代谢的COVID-19干预提供了新思路。
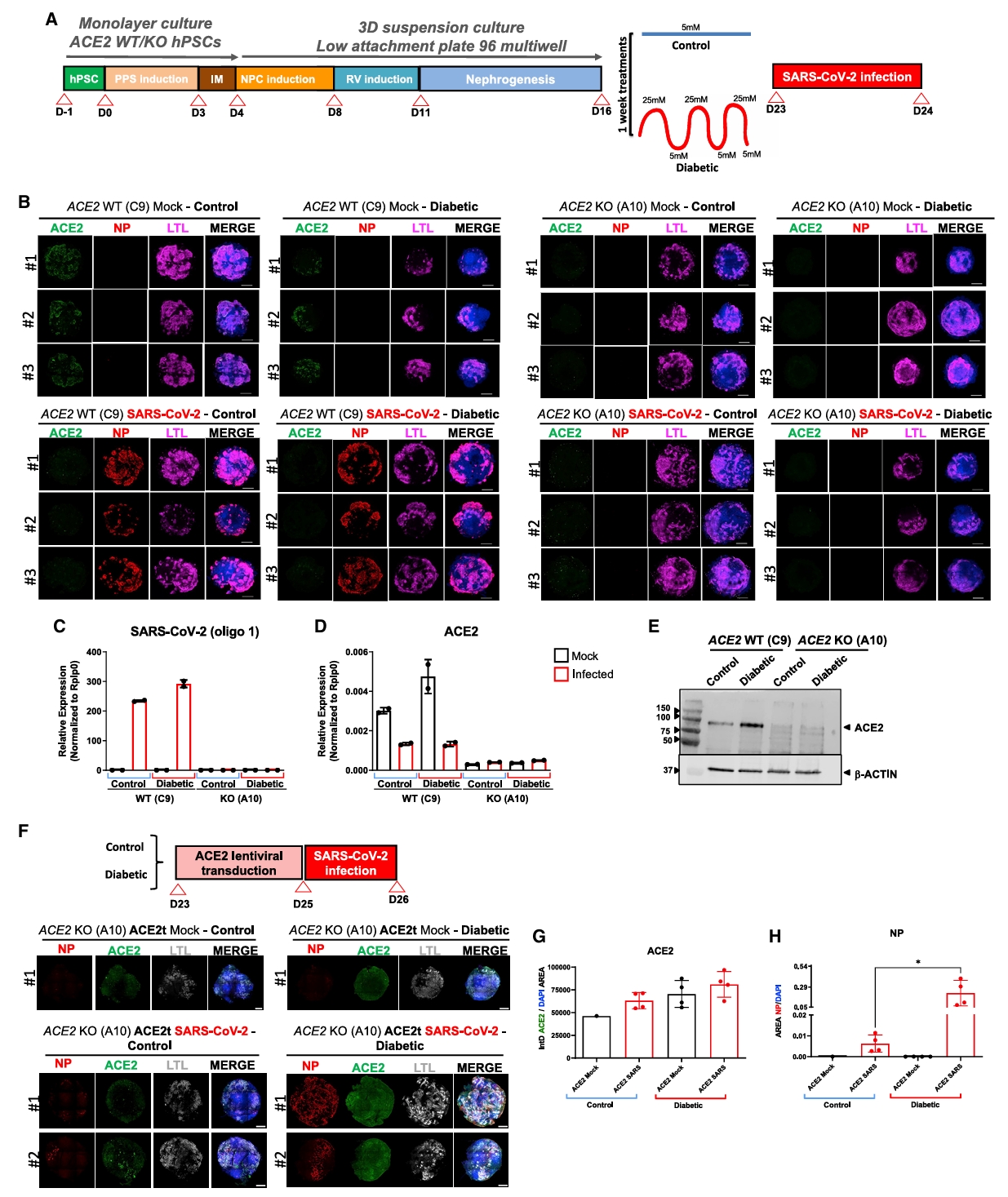
糖尿病相关肾损伤类器官模型的应用价值
传统模型在模拟人类肾脏对高糖环境的复杂应答方面存在局限。人诱导多能干细胞来源的肾脏类器官为糖尿病肾病研究提供了可体外操作的细胞模型。前述三项研究展示了该模型在糖尿病损伤研究中的应用:
机制观察:在高糖条件下培养肾脏类器官,可观察到代谢相关基因表达变化、炎症因子上调及细胞结构改变等糖尿病肾病早期特征性表现。
靶点识别:基于类器官模型的分析有助于发现参与高糖损伤的关键分子,如MIF和TNF-α在介导上皮细胞脱落中的作用,以及ACE2在糖尿病环境下表达水平的变化。
干预评估:该类器官平台可用于测试候选干预手段的效果,如MIF抑制剂、TNF-α抑制剂对细胞结构的保护作用,以及代谢调节剂对病毒感染易感性的影响。
交叉研究应用:糖尿病样肾脏类器官还可用于探讨糖尿病与其他病理因素(如病毒感染)之间的相互关系,拓展应用范围。
研究支持与服务
将肾脏类器官与糖尿病损伤模型相结合,为相关机制研究和干预评估提供了可操作的实验平台。
华津肾脏类器官Kidnioid®平台在此领域提供专业支持:
方案咨询:针对糖尿病肾病类器官模型构建与实验设计提供专业建议。
实验实施:承接类器官培养、高糖损伤建模、药物干预等实验服务。
数据支持:提供实验流程记录与可验证的检测数据。
平台优势
基于华津Kidnioid®平台在肾脏类器官培养和疾病建模领域的技术积累,可为糖尿病肾病相关研究提供标准化的实验模型和技术支持。
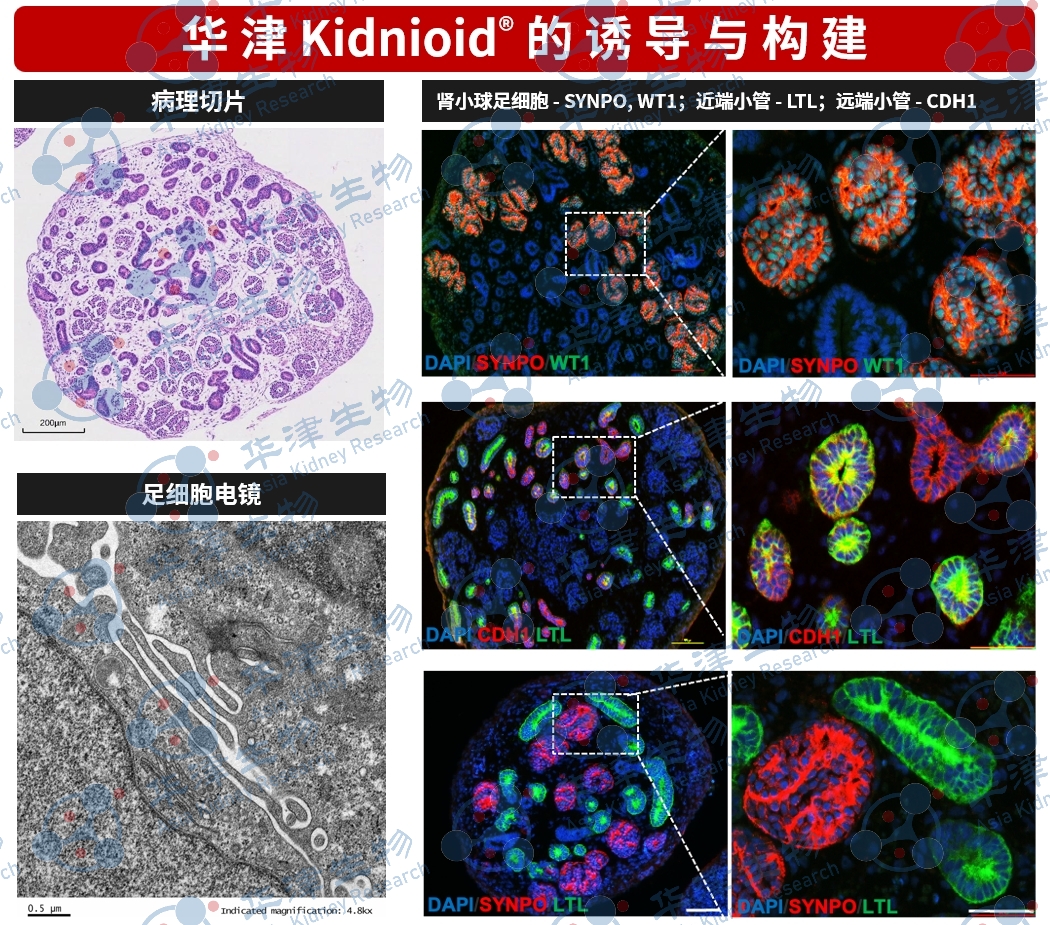
基于人源细胞构建的肾脏类器官包含足细胞、近端小管和远端小管等细胞类型,可在一定程度上反映人肾脏的结构特征。
该模型可用于高糖诱导的细胞应答观察、相关信号通路的初步分析以及候选干预手段的效果评估。
可用于糖尿病肾病机制探索、化合物筛选、干预策略验证等研究场景。
技术优势
周期较短:相比部分动物实验,模型构建与评估时间有所缩短。
模型稳定性较好:在标准化培养条件下,模型稳定性较高。
灵活性较强:可根据研究需求进行定制化调整。
检测体系适配性高:与常规分子生物学/细胞生物学方法高度兼容,便于机制研究与多指标评价。
感谢您对本文的浏览。肾脏类器官作为前沿生物技术,不仅在疾病模拟、药物筛选和再生医学研究中展现出巨大潜力,也为精准医疗和新药研发提供了更可靠的平台。目前全球多家监管机构已将其纳入药物评价体系,标志着该技术正逐步走向标准化与应用化。如果您希望进一步了解肾脏类器官的技术细节、合作研究或商业应用,欢迎随时联系咨询:
📞 商务支持 - 李老师 17276665437
📞 技术支持 - 田老师 18843183823
我们期待为您提供专业服务与合作支持。

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

