基于肾脏类器官的肾祖细胞移植策略研究
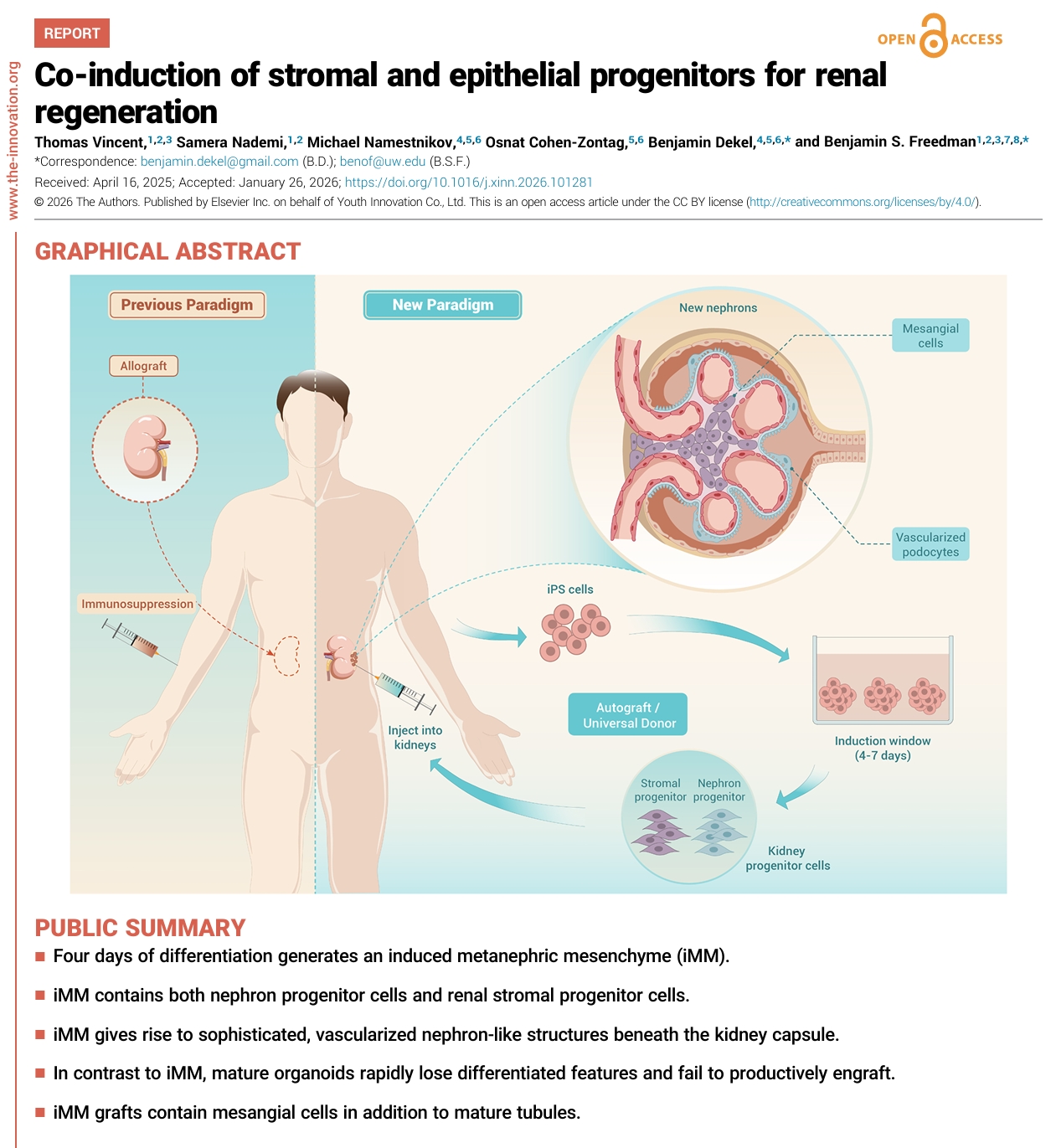
本研究比较了iPSC不同分化阶段细胞的体内成肾能力。研究发现,分化仅4天、同时表达肾单位与间质祖细胞标志的“诱导后生间充质”(iMM)移植后,能在小鼠体内形成包含多种肾小管节段的肾单位,并成功招募宿主内皮细胞形成具有潜在滤过功能的嵌合性肾小球。该策略简化了细胞制备流程,为基于iPSC的肾脏再生研究提供了新依据。
近日,以色列示巴医疗中心(Sheba Medical Center)与特拉维夫大学(Tel Aviv University)的Benjamin Dekel教授团队,联合华盛顿大学(University of Washington)医学院肾脏科、生物工程系的Benjamin S. Freedman教授团队,在 The Innovation 期刊(IF 25.7)上发表研究,系统比较了不同分化阶段的诱导多能干细胞(iPSC)在体内形成肾组织的能力。研究发现,仅分化4天的细胞群体——即“诱导后生间充质”(iMM)——在移植至免疫缺陷小鼠肾被膜下后,能够形成包含足细胞、系膜细胞及多种肾小管节段的肾单位结构,并招募宿主血管形成嵌合性肾小球。
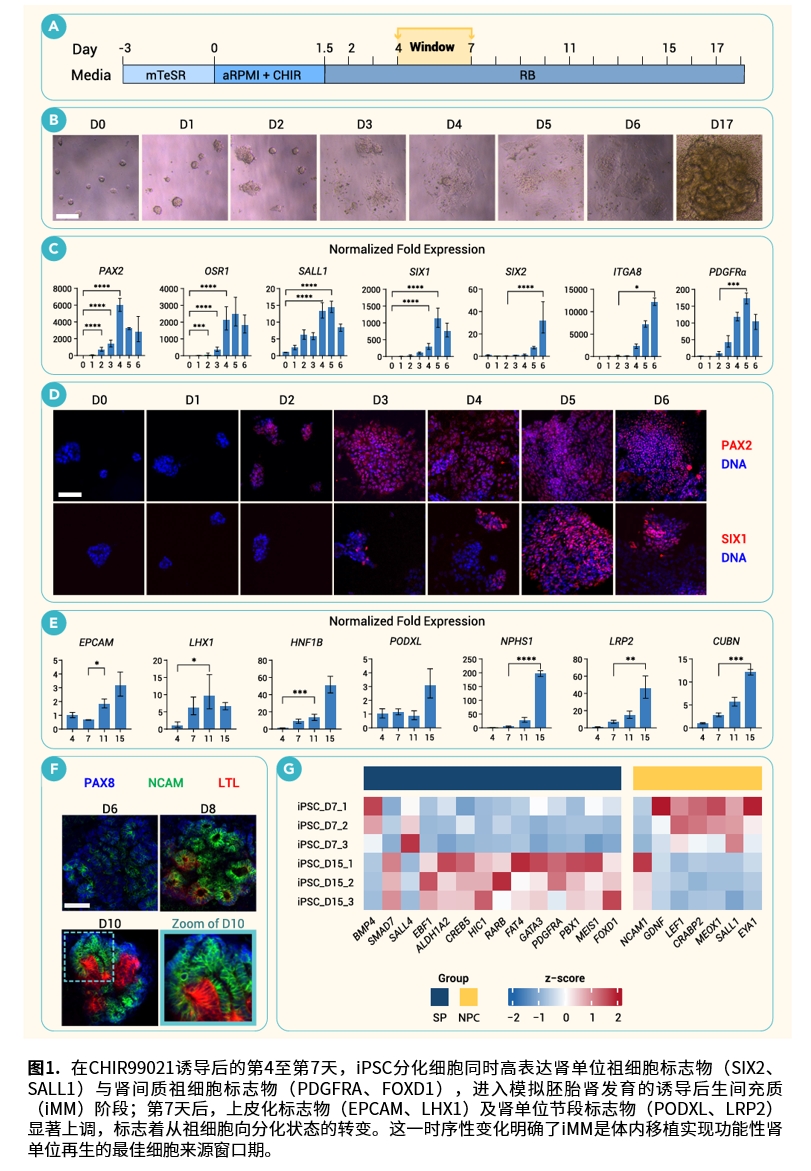
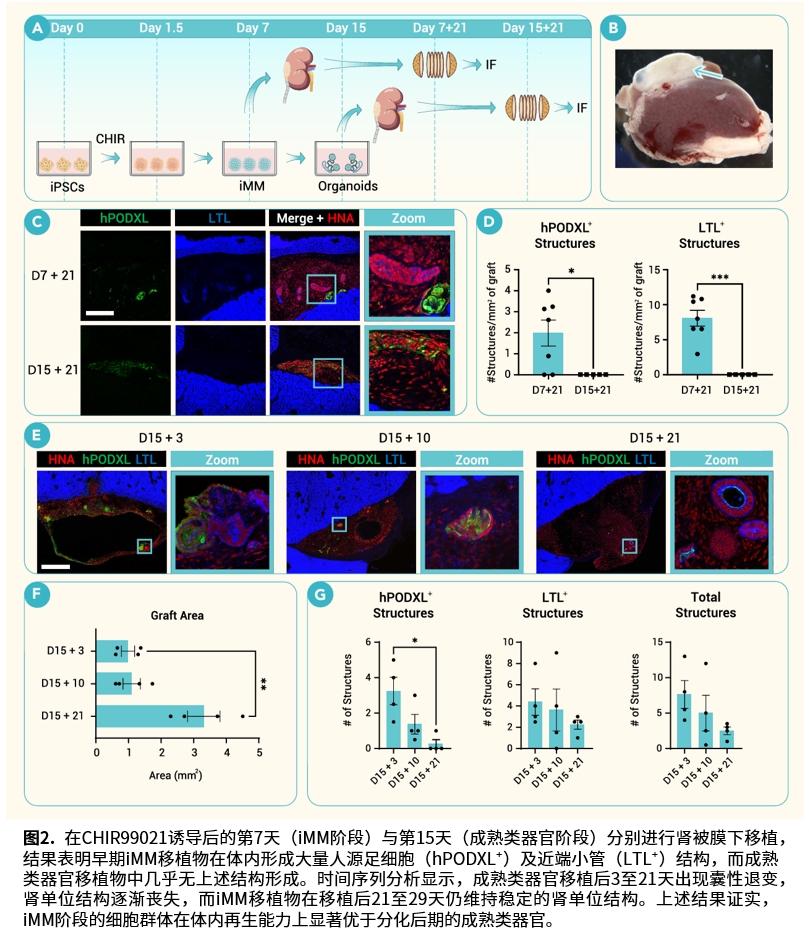
研究团队通过动态追踪iPSC分化过程发现,在CHIR99021诱导后的第4至第7天,细胞群体同时表达肾单位祖细胞标志物(SIX2、SALL1)与肾间质祖细胞标志物(PDGFRA、FOXD1),这一状态与胚胎肾发育早期的后生间充质阶段相似。相比之下,分化至第15天的成熟类器官,尽管已形成上皮化肾单位结构,但移植后出现囊性退变,未观察到稳定的功能性血管化。
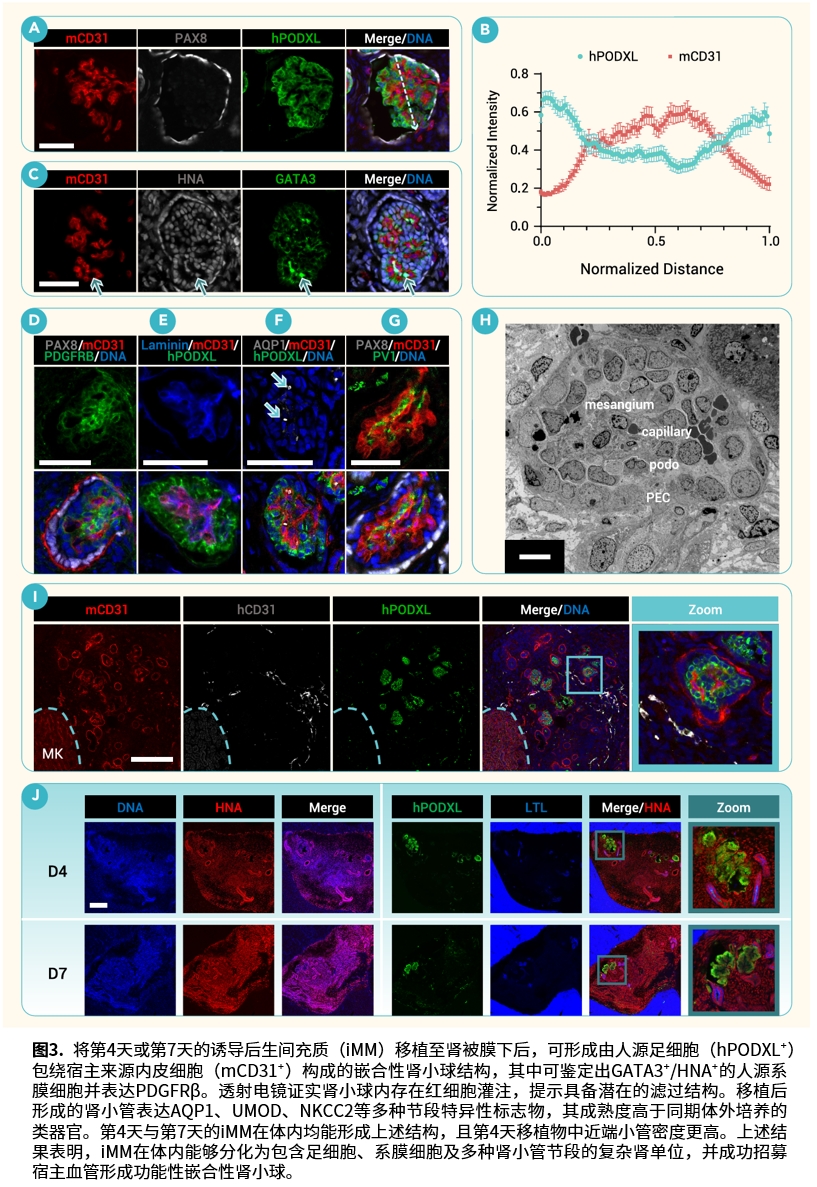
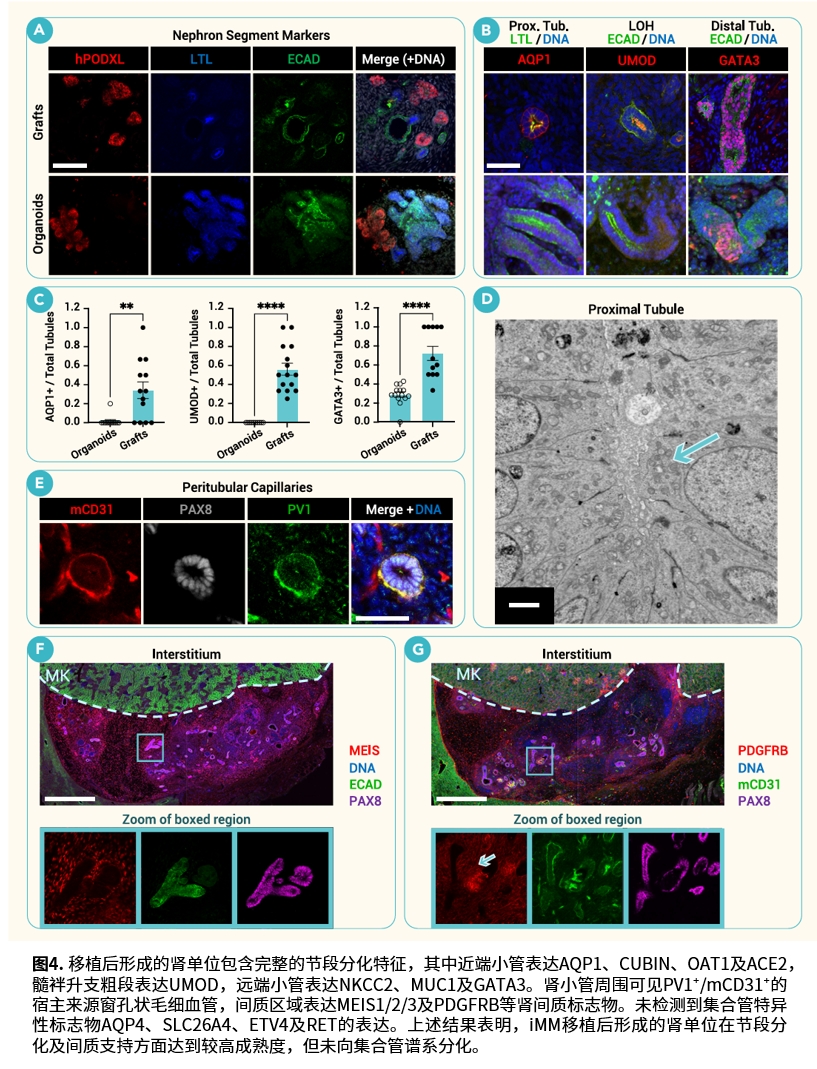
将第4天的iMM移植至小鼠肾被膜下3周后,可观察到嵌合性肾小球结构:人源足细胞包裹宿主来源的内皮细胞形成的毛细血管袢,GATA3阳性的人源系膜细胞位于毛细血管与足细胞之间,并表达PDGFRβ。透射电镜下可见肾小球内存在红细胞,提示具备潜在的滤过结构。移植后形成的肾小管表达AQP1、UMOD、NKCC2等多种节段特异性标志物,其成熟度高于同期体外培养的类器官。
该研究结果表明,在iPSC分化早期存在一个时间窗口,此阶段的祖细胞群体在移植后能够完成进一步分化并与宿主血管系统整合。相较于分别诱导不同祖细胞群体再行组装的策略,这一方法简化了制备流程,为基于iPSC的肾脏再生研究提供了可供参考的实验依据。
参考文献
Vincent T, Nademi S, Namestnikov M, et al. Co-induction of stromal and epithelial progenitors for renal regeneration. The Innovation, 2026, 7(5): 101281.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

扫码关注华津生物的官方微信
