
2026年3月5日,东京大学Hiroki Shioda、Masaki Nishikawa团队在Regenerative Therapy(日本再生医学会官方期刊)发表了题为"Kidney organoid vascularization: current advancements in the field"的系统性综述,全面梳理了从肾脏发育机制到各类血管化策略的研究现状。
血管化不足是制约肾脏类器官成熟度的因素之一,肾小球血管化的实现是该领域面临的技术难点。本文基于该综述的框架,梳理肾脏类器官血管化的研究进展与技术路径。
血管化对肾脏类器官的意义
肾脏的功能包括血液过滤,这一过程涉及肾小球中血管与足细胞的相互作用。目前体外培养的肾脏类器官可形成肾单位结构,但内皮细胞数量有限,肾小球血管化程度较低,类器官仍处于类似胎儿期的未成熟状态。
肾脏发育相关机制
1. 血管内皮细胞的来源
肾脏血管内皮细胞的起源存在两种观点:一是由中间中胚层直接分化形成,二是通过血管新生从主动脉出芽侵入。支持后一观点的证据是,胚胎期第12.5天(E12.5)小鼠肾脏血管已与主动脉建立连接,且红细胞的出现提示血液灌注形成。与此同时,中间中胚层中存在flk-1阳性细胞亚群(flk-1:胎肝激酶1,为血管内皮生长因子受体2(VEGFR2)在小鼠中的同源蛋白),这一亚群具有向内皮细胞分化的能力,为前一观点提供了细胞学基础。
这一讨论对类器官血管化策略具有参考意义——最终血管系统是依赖类器官自身内皮分化,还是依赖外部血管的侵入,会影响技术路线的选择。
2. 肾小球血管化的分子机制
肾小球血管化的实现涉及足细胞与内皮细胞的相互作用。血管内皮生长因子(VEGF)是由足细胞分泌的生长因子,参与引导内皮细胞进入肾小球的过程。BMP4、Semaphorin 3A/3C、Ang1等因子也参与这一过程。
上述因子的过表达或抑制均可导致发育异常。这一现象提示,在类器官中实现肾小球血管化,需要维持生长因子分泌的适当水平。
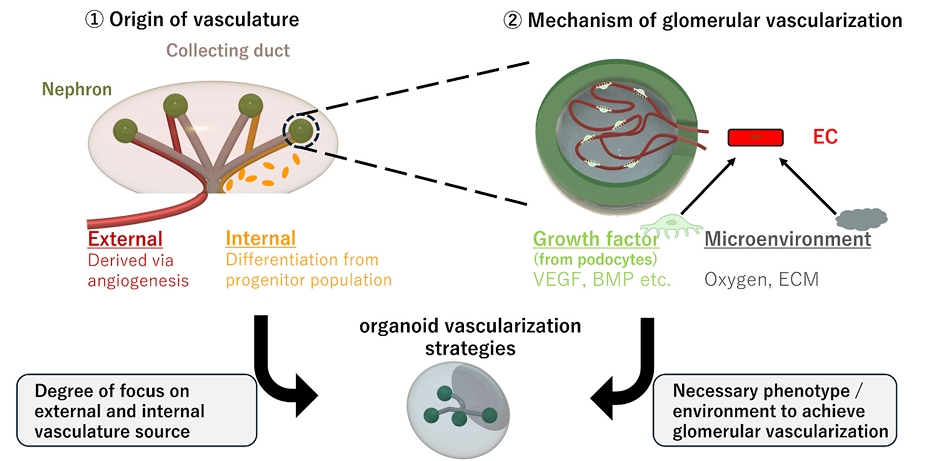
图1. 肾脏血管发育的两个核心问题为类器官血管化研究提供了重要参考:一是血管内皮细胞的起源,涉及由中间中胚层直接分化(间充质来源)还是从主动脉出芽侵入(血管新生),对应类器官移植后内皮细胞源于自身还是宿主的争议;二是S型小体阶段足细胞与内皮细胞的相互作用,涉及VEGF等信号分子的分泌与接收,指向肾小球特异性血管化的实现难点。
血管化的主要技术路径
1. 体内移植
将肾脏类器官移植到动物体内是目前实现肾小球血管化的方法之一。
小鼠肾包膜下移植:研究显示,移植后可观察到肾小球血管化,以及足细胞足突形成、内皮细胞窗孔出现、基底膜形成等形态学特征。
鸡胚绒毛尿囊膜移植(CAM):CAM是血管化膜结构,已被用于血管化研究。有研究将微流控芯片植入CAM,尝试实现芯片与体内血管的结合。
体内移植存在通量较低、存在异种嵌合问题等局限,较难用于药物筛选等应用场景。
2. 体外诱导
流体流动:2019年,Homan团队通过微流控装置向类器官灌注培养基,在体外实现了肾小球血管化。随灌注速率增加,血管密度和肾单位标志基因表达有所提升。后续研究提示integrinα2β1介导的机械感知通路可能参与这一过程。
内皮细胞诱导:2024年,Maggiore团队利用基因工程技术在类器官中诱导ETV2表达,形成了包含动脉、静脉和肾小球内皮亚群的血管网络。部分内皮细胞呈现窗孔形态。
两种方法存在差异:流体流动条件下VEGF产生增加,而ETV2诱导条件下血管内皮生长因子受体(VEGFR)表达增强。
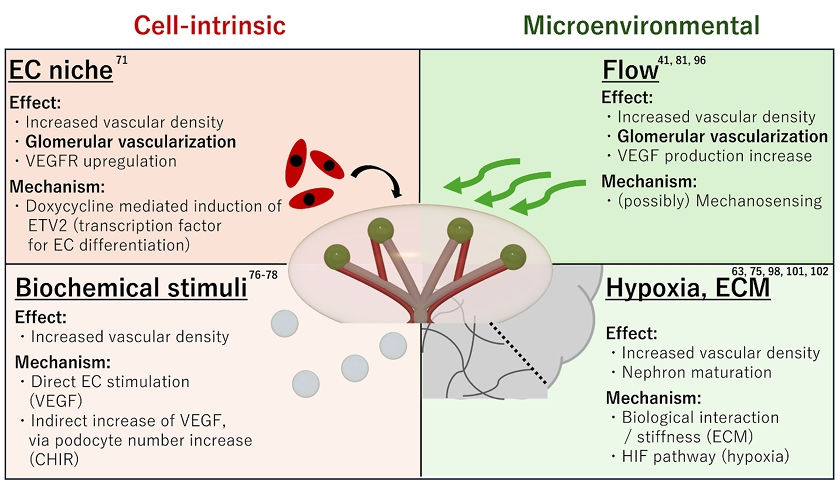
图2. 当前肾脏类器官体外血管化策略分为细胞内在调控与微环境干预两大路径:细胞内在调控包括两种方式:一是通过ETV2诱导形成内皮细胞生态位,可增加血管密度、实现肾小球血管化并上调VEGFR表达;二是通过生化刺激,包括VEGF直接作用于内皮细胞,或通过CHIR增加足细胞数量间接提高VEGF水平,均可增加血管密度。微环境干预包括三种方式:流体流动通过机械感知机制增加血管密度、实现肾小球血管化并促进VEGF产生;低氧通过HIF通路、细胞外基质通过生物学相互作用与硬度调控,均可增加血管密度并促进肾单位成熟。
外部血管连接
内部血管网络与外部灌注系统的连接尚未完全解决。
有研究尝试将人脐静脉内皮细胞(HUVEC)芯片与肾脏类器官共培养,观察到外部内皮细胞侵入类器官,但未实现肾小球血管化,也无直接证据表明灌注建立。另一研究构建了HUVEC血管构造并与类器官连接,实现了内-外血管系统的连通,但肾小球血管化未同时实现。
这一情况提示,血管连接与肾小球血管化可能需要不同的培养条件。
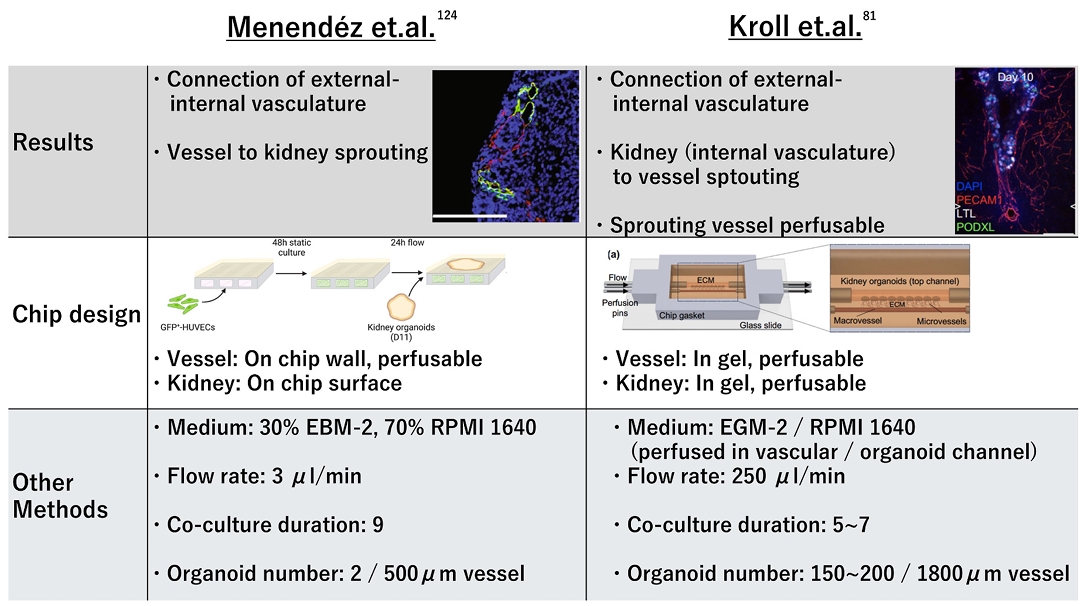
图3. 外部血管连接的尝试:Menéndez等人通过将可灌注血管芯片与类器官共培养,实现血管向肾脏出芽及内外血管系统连接。Kroll等人将类器官包埋于可灌注凝胶中,实现肾脏内部血管向外部血管出芽并形成可灌注连接。
技术挑战与未来方向
肾脏类器官血管化研究仍面临若干问题。肾小球血管化的实现机制尚不明确,成功案例有限且条件各异。血管内皮细胞的来源存在争议,体内移植研究中内皮细胞来自类器官自身还是宿主血管,不同研究结论不一。此外,不同研究使用的类器官分化方案、血管化诱导条件、评价指标存在差异,难以直接比较。
当前流体力学刺激和内皮细胞定向诱导是探索中的两条技术路径,进一步理解肾脏发育机制并应用于工程策略,可能有助于推动该领域的发展。
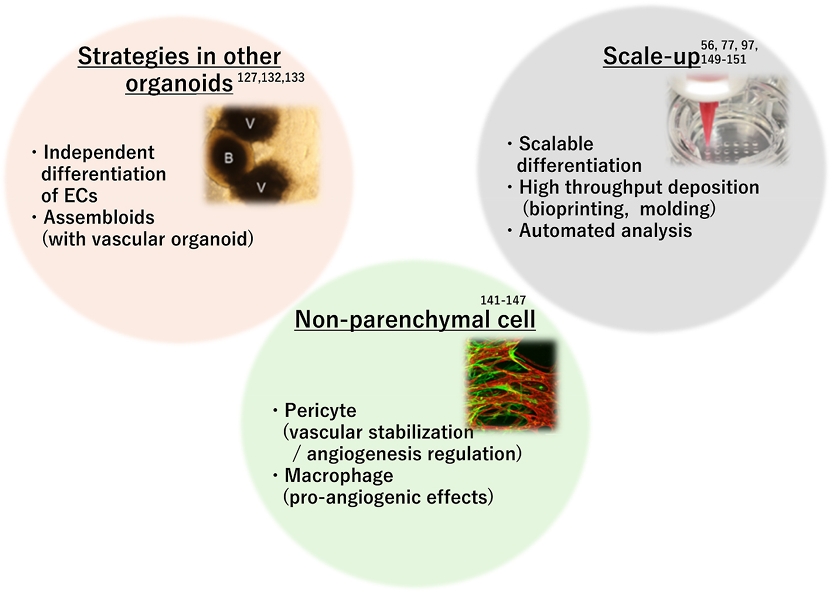
图4. 未来可整合的替代策略:包括其他类器官策略(内皮细胞独立分化、与血管类器官形成类器官联合体)、规模化技术(可扩展分化、高通量沉积、自动化分析)以及非实质细胞(周细胞、巨噬细胞)。
肾脏类器官血管化的核心瓶颈在于肾小球血管化的实现。这一过程涉及足细胞与内皮细胞的精密分子对话,需要维持VEGF等生长因子的适当水平。
当前体外研究中,仅流体力学刺激和内皮细胞定向诱导两条路径成功突破这一难点,前者通过机械感知增强VEGF产生,后者通过上调VEGFR表达;其余方法虽能增加血管数量,但未能实现肾小球特异性血管化。
体内移植虽效果显著,但存在通量低和异种嵌合问题,更适合作为机制研究的参照体系。外部血管连接与肾小球血管化尚未在同一系统中协同实现,提示两者可能需要不同的培养条件。
未来突破有赖于对肾脏发育机制的深入理解、技术方案的标准化,以及血管连接与肾小球血管化协同培养条件的建立。
参考文献:
Shioda H, Tang TH, Raykhel I, Sakai Y, Nishikawa M. Kidney organoid vascularization: current advancements in the field. Regenerative Therapy. 2026 Mar 5;32:101087. doi: 10.1016/j.reth.2026.101087.


