近年来,临床前药物安全性研究的动物实验一直备受争议。动物模型的准确性不足、伦理争议日益突出,且成本高昂,都推动着监管科学的巨大变革。
近日,美国食品药品监督管理局(FDA)发布了重磅战略文件——《减少临床前安全性研究中动物实验的路线图》,首次系统性地提出要用科学验证的新方法学(New Approach Methodologies, NAMs),逐步替代传统动物实验。

图1:FDA法案PDF截图
为什么要淘汰动物实验?
FDA指出,传统的动物模型预测人体药物反应存在重大缺陷,90%以上在动物中有效的药物,在人体实验中却以失败告终。尤其在癌症、阿尔兹海默病、炎症性疾病领域,动物实验的预测性明显不足。
与此同时,公众舆论的压力也越来越大,超过85%的美国公众支持逐步淘汰动物实验。2022年,美国国会通过《FDA现代化法案2.0》,明确授权FDA接受非动物实验数据替代传统动物试验。
图2:动物实验
NAMs究竟是什么?
NAMs是一系列创新技术的集合,包括:
类器官与器官芯片:用人类细胞构建微型器官模型,如肝芯片、心脏芯片等,精准模拟药物对人体器官的毒性反应。
计算建模与人工智能:通过计算机模拟药物在人体内的吸收、代谢过程,以及预测药物的免疫反应和毒性。
高通量细胞平台与人体组织切片:直接在体外人体细胞或组织上进行药物安全评估。
这些方法不仅更符合人体真实反应,而且效率更高、成本更低。
FDA未来3年具体如何实施?
FDA计划从以下几个方面落实:
1)建立国际毒性数据库,共享全球已有的人体毒性数据。
2)鼓励企业提交NAM数据,逐步减少传统动物实验。
3)缩短动物实验周期,如将单抗的灵长类动物试验从6个月缩短至3个月。
4)定期评估NAMs表现,不断优化实施路径。
跨部门合作推动全球监管变革
FDA将与NIH、EPA、VA等18家联邦机构合作,共同通过ICCVAM平台推进NAMs技术验证,推动国际监管协调,最终实现全球药物安全评价模式的变革。
华津肾类器官模型助力NAMS
在药物肾毒性评估领域,传统动物实验难以准确预测人类肾脏反应,且面临伦理和成本问题。我们公司研发的肾类器官模型基于人体干细胞技术,可精准模拟人体肾脏的结构和功能,用于药物筛选和肾毒性评估,已成为替代动物实验的重要工具。
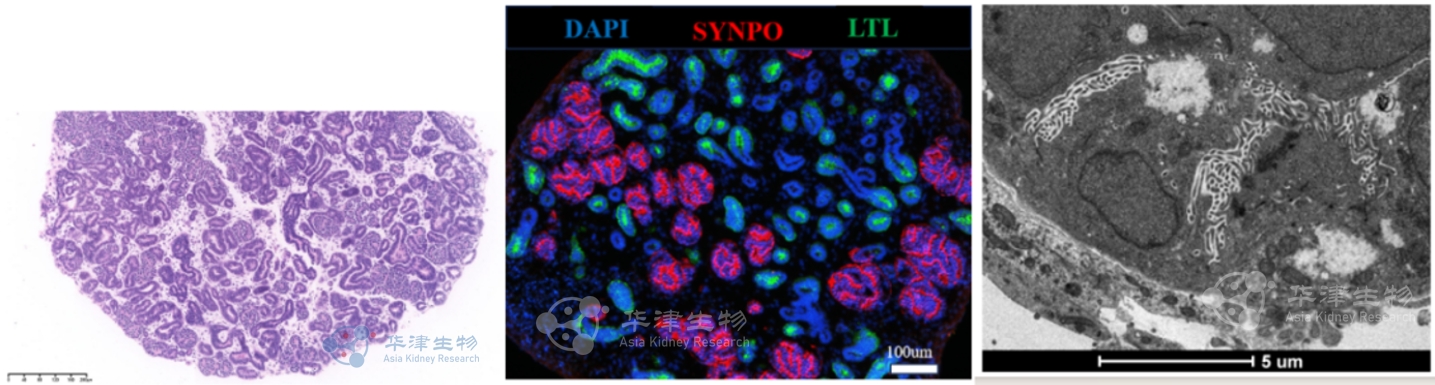
图3:华津肾类器官的HE染色免疫荧光染色和TEM电镜
我们的肾类器官平台具备以下优势:
●高度模拟人体生理环境:能够高度贴近人体的真实生理反应,更准确的药物毒性预测。
●显著降本增效:大幅削减了药物开发的实验成本与研发周期。
●契合伦理趋势:顺应全球减少动物实验的大势。
*欢迎与我们联系,了解更多肾类器官在药物研发与肾毒性测试中的应用。
总结
FDA的这一重大政策信号,标志着临床前安全性研究的动物实验逐步走向终结,一个更科学、更高效、更人性化的新时代正在到来。

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

