
今年 8 月,国际综合性权威期刊 Advanced Science 在线发表了题为 “Developmental Hypoxia Enhances Kidney Organoid Complexity and Maturity” 的最新研究。研究团队在肾类器官早期分化阶段引入适度缺氧(模拟胚胎发育环境),使类器官在同一体系中能够同时生成输尿管芽样细胞(UB-like)和后肾间充质(MM)。这一策略不仅促成了更长、更复杂的小管网络,还系统性地在同一体系中重建集合管样结构及功能亚型细胞在类器官体系中稳定出现集合管样结构及功能亚型细胞(如 AQP2+主细胞、FOXI1+插入细胞)。更重要的是,这些类器官展现出近端小管重吸收与远端小管/集合管钠转运等功能特征,在结构和功能上均更接近真实肾脏,为构建高阶肾模型、开展疾病研究和药物筛选开辟了新路径。
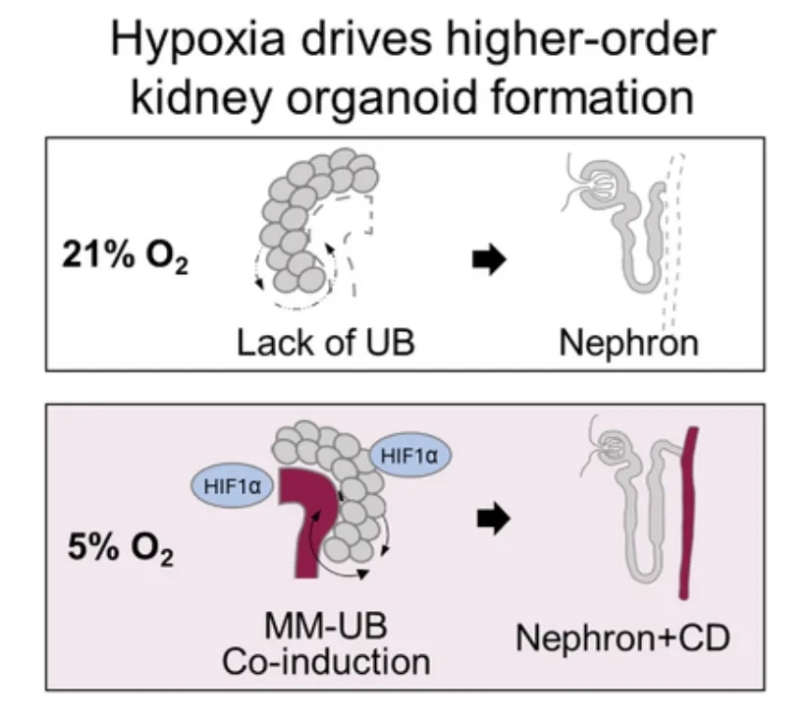
图形摘要
研究内容
在图1中,作者展示了缺氧如何在早期改变肾类器官的分化轨迹。A 图给出了实验流程:在分化前 9 天处于5% O₂ 低氧环境,随后切换回常氧培养。B–D 图显示,低氧组 HIF1α 稳定上调,并显著提高了原始条(PS)的诱导效率,TBXT、TBX6 表达明显增强。E–F 图进一步说明低氧(下同)改变了中胚层分化方向:常氧下主要生成 WT1+/HOXD11+ 的后中间中胚层(pIM),而缺氧则促使更多细胞进入 LHX1+/PAX2+ 的前中间中胚层(aIM),为输尿管芽样细胞奠定基础。G–J 图揭示在第 9 天,缺氧组不仅有 SIX2+ 的后肾间质(MM),还出现了 CALB1+/SOX9+ 的 UB-like 细胞,并且这些 UB-like 呈环绕分布在 SIX2+ 区域周边,空间格局与体内发育相似。I–L 图则显示到第 14 天,缺氧组依然能维持 SOX9+ UB-like 细胞的存在,并出现 PAX8+/SOX9+ 双阳性细胞,而常氧下几乎检测不到。整体来看,这一组实验明确表明:在肾类器官早期分化引入适度缺氧,不仅提升了原条的生成效率,更让类器官在同一体系内同时分化出 MM 与 UB-like 双谱系,这是传统 protocol 难以实现的关键突破。
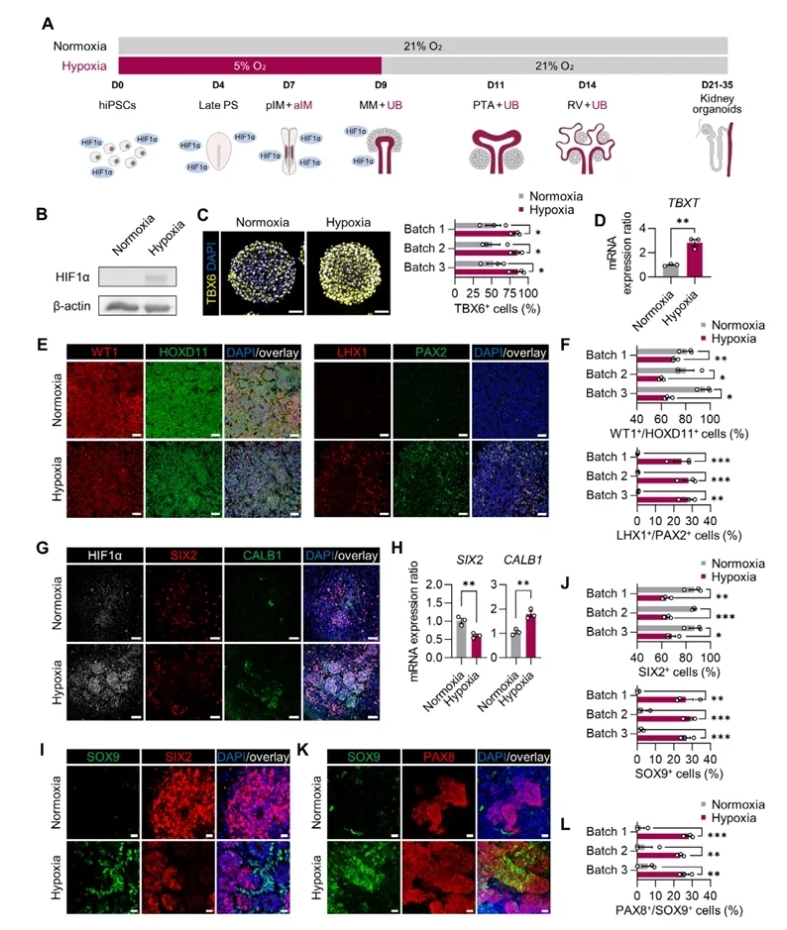
图1. 在缺氧刺激下,人诱导多能干细胞(hiPSCs)实现了后肾间充质(MM)与输尿管芽样细胞(UB-like)的双重诱导(点击图片查看大图)
在图2中,作者展示了缺氧如何显著提升肾类器官的结构复杂性与功能成熟度。A 图显示在第 21 天,缺氧组类器官形成了更长、互联性更强的小管网络,而常氧组小管形态短且零散;B 图用示意图直观对比了不同氧气条件下的组织构成:常氧组以肾小球为主,小管比例偏低;而 5% O₂ 缺氧组则同时具备肾小球和丰富的小管结构,尤其是集合管样区域显著增加;相比之下,过低氧(1% O₂)则导致整体结构稀疏,几乎不成形。C–D 图进一步量化了类器官数目,结果表明缺氧不仅增加了单个类器官的复杂度,也提升了整体诱导效率。E 图的免疫荧光揭示,缺氧类器官中近端小管(LTL+)和远端/集合管(CDH1+)区域显著扩展,而足细胞标志 PODXL 的面积相对减少,使细胞组成更接近真实肾脏;F–G 图的统计也证实了这一点。H 图更为关键,缺氧组出现了 PODXL+ 足细胞与 PECAM1+ 内皮细胞共存的结构,提示血管样成分的形成;同时 I 图显示多个肾脏功能基因表达显著上调,包括近端小管的 AQP1、SLC34A1,远端/集合管的 CDH1,以及药物转运相关的 ABCB1。总体来看,Figure 2 清楚展示了:缺氧不仅改善了肾类器官的形态结构,还优化了细胞组成和功能基因表达,使其在多个层面更接近真实肾脏。
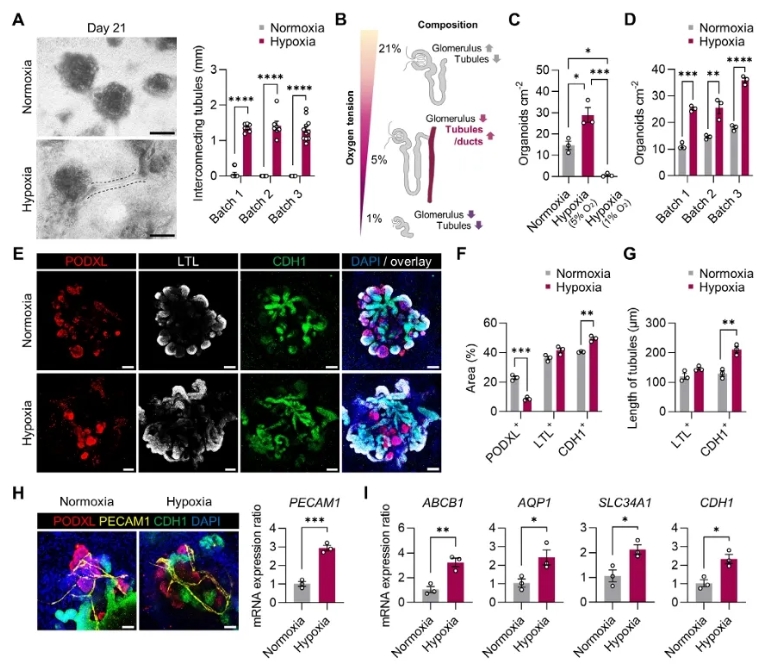
图2. 在优化的缺氧条件下形成具有延伸且成熟小管结构的肾类器官(点击图片查看大图)
在图3中,作者重点展示了缺氧如何推动集合管谱系的形成与功能化。A–B 图的免疫染色显示,缺氧类器官中 CDH1+/CALB1+ 的远端小管显著增多,并与 PODXL+ 足细胞区相邻,提示形成了更复杂的肾单位连接结构。进一步的 C–E 图揭示,在缺氧条件下首次出现了 AQP2+ 主细胞和 FOXI1+ 闰细胞细胞,而常氧组几乎完全缺失这些亚型,这是集合管成熟的关键标志。F–G 图用 DBA 标记进一步确认这些管段确实属于集合管,而 H 图则表明缺氧类器官中集合管与远端肾小管(BRN1+)共同存在,结构层次更贴近体内发育。最后的 I–J 图提供了量化与转录学证据:缺氧组的 CALB1+ 区域面积和管道长度均大幅增加,同时集合管相关基因(包括 AQP2、AQP4、SLC4A1、SLC26A4 等)显著上调。整体来看,Figure 3 确立了缺氧类器官在体外首次稳定重建集合管谱系,不仅有形态学上的集合管结构,还能分化出功能亚型细胞,标志着类器官向更高阶模型迈进。
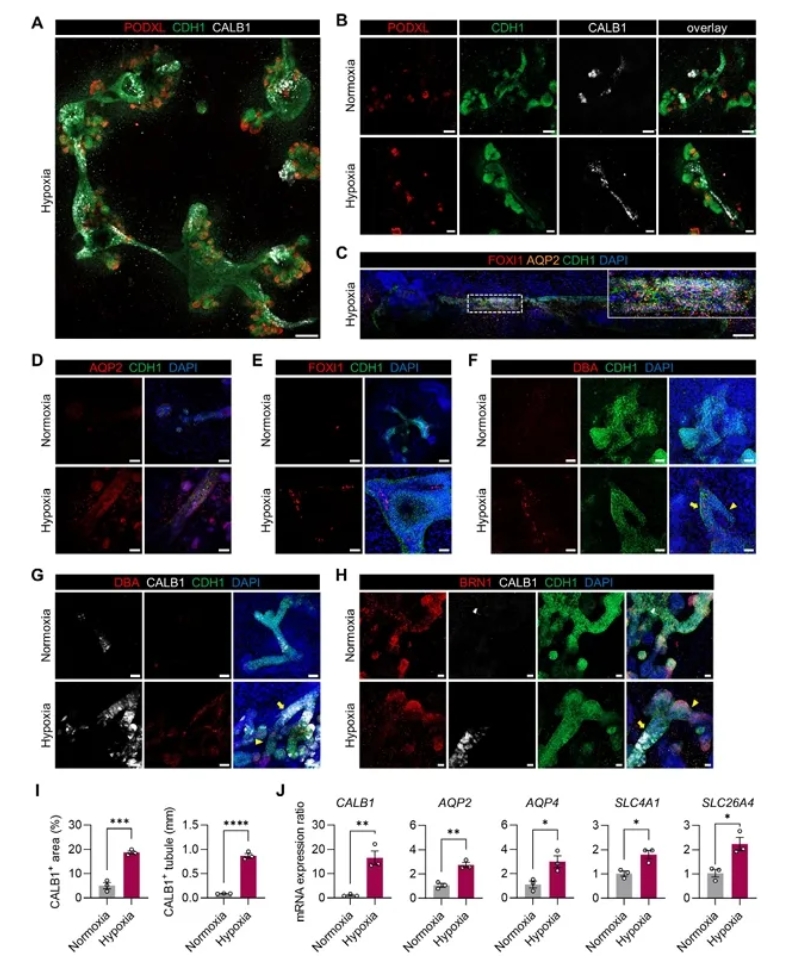
图3. 缺氧增强型肾类器官中高结构化小管的集合管亚型细胞标志物表达(点击图片查看大图)
在图4中,作者通过单细胞转录组分析,直接验证了缺氧组类器官中集合管谱系的真实性与独特性。A–B图的UMAP可视化表明,常氧类器官主要由足细胞、近端小管和亨利袢细胞组成,而缺氧类器官则多出了一个明确的 集合管(CD)细胞簇。C–D图的细胞比例对比显示,缺氧类器官中的远端小管/集合管细胞比例显著提升,更接近胎儿和成人肾的谱系构成。E–F图进一步揭示,集合管特异性基因(如 GATA3、AQP2、SLC14A2、SCNN1B)仅在缺氧组显著表达,常氧组中几乎检测不到;G图总结了CD簇中高表达的核心基因,包括上皮结构蛋白KRT8、转录因子GATA3,以及关键转运蛋白 AQP2、SCNN1A/1B,为其集合管身份提供了有力佐证。最后的H–I图通过通路富集分析显示,这些集合管细胞活跃于Wnt、PI3K-AKT、HIF-1等发育信号通路,并富集于 管道分支、细胞迁移和血管生成 等生物过程。综上,Figure 4从单细胞层面为缺氧类器官中的集合管谱系提供了坚实证据,证明其不仅存在于免疫学和形态学观察中,还在分子层面形成了与体内一致的功能性细胞群。

图4. 单细胞转录组分析鉴定缺氧增强型肾类器官中的集合管样细胞群(点击图片查看大图)
在图5中,作者通过超微结构观察和功能实验,证明缺氧类器官不仅“长得像肾”,更具备实际功能。A 图的扫描电镜清晰展示了不同管段的形态特征:缺氧类器官中的肾小球足突排列更紧密,近端小管的刷状缘更加致密,远端和集合管表面的初级纤毛更长、更规整;这些超微结构都明显优于常氧组。B 图对纤毛长度的统计结果进一步证实了这一点,缺氧组平均纤毛长度显著延长,更接近体内生理水平。随后 C–D 图通过功能检测揭示了关键的生理活性:缺氧类器官的近端小管能够高效摄取 10 kDa Dextran,说明具备再吸收能力;远端/集合管 CDH1+ 区域则能够积累 Sodium Green,提示其具备钠离子转运功能。综上,Figure 5 证明缺氧不仅优化了肾类器官的超微结构,还赋予了其核心的肾脏功能属性,为类器官“能工作”提供了直接证据。
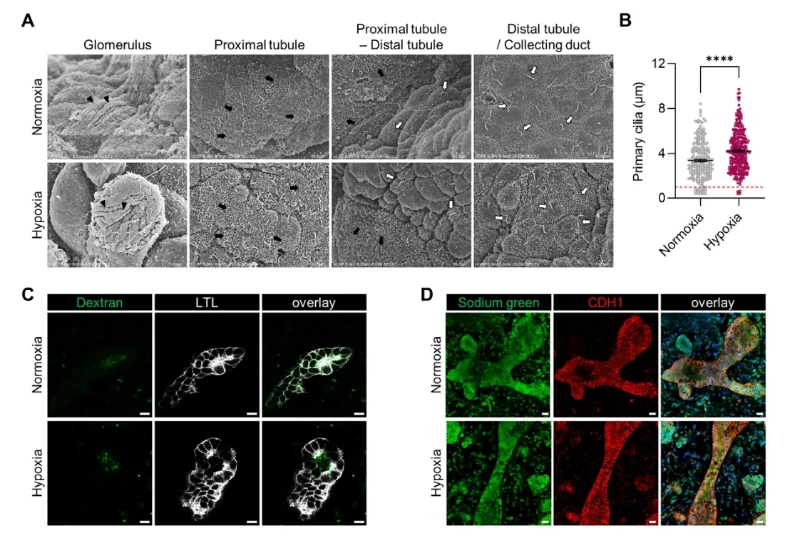
图5. 缺氧增强型肾类器官展现成熟的超微结构与肾脏功能(点击图片查看大图)
在图6中,作者揭示了缺氧通过 HIF1α 介导的信号调控促进肾类器官发育。A 图显示,不同分子呈现出阶段性的动态模式:GDNF 与 WNT9B 在早期(第 9 天)达到峰值,推动 UB 与 MM 的互作和分支;而 WNT4 与 WNT11 在中后期(第 14–21 天)逐渐升高,支持小管与集合管的进一步成熟。B 图给出的实验流程表明,使用 CoCl₂ 缺氧模拟剂 同样可以在第 9 天激活缺氧反应。C–D 图的免疫染色结果显示,在 CoCl₂ 处理的类器官中,第 9 天即可检测到 SIX2+ MM 与 SOX9+ UB-like 的共存,第 21 天更能同时看到 PODXL+ 足细胞、CDH1+/CALB1+ 远端小管,说明缺氧效应可被药物复现。E 图的明场图像则表明 CoCl₂ 类器官整体结构更饱满。F 图的转录结果显示,缺氧显著上调了近端(AQP1、ABCB1、SLC34A1)、亨利袢(UMOD、CDH1)及远端/集合管(AQP4、SLC4A1、SLC26A4)等功能基因的表达。最后 G 图再次确认,在缺氧或模拟缺氧下,WNT9B 早期升高,而 WNT4/WNT11 在后期维持较高水平。整体来看,Figure 6 强调了缺氧并非简单的持续激活,而是通过阶段性调控 WNT/GDNF 等信号,实现了 UB–MM 互作和肾小管、集合管的协调发育。
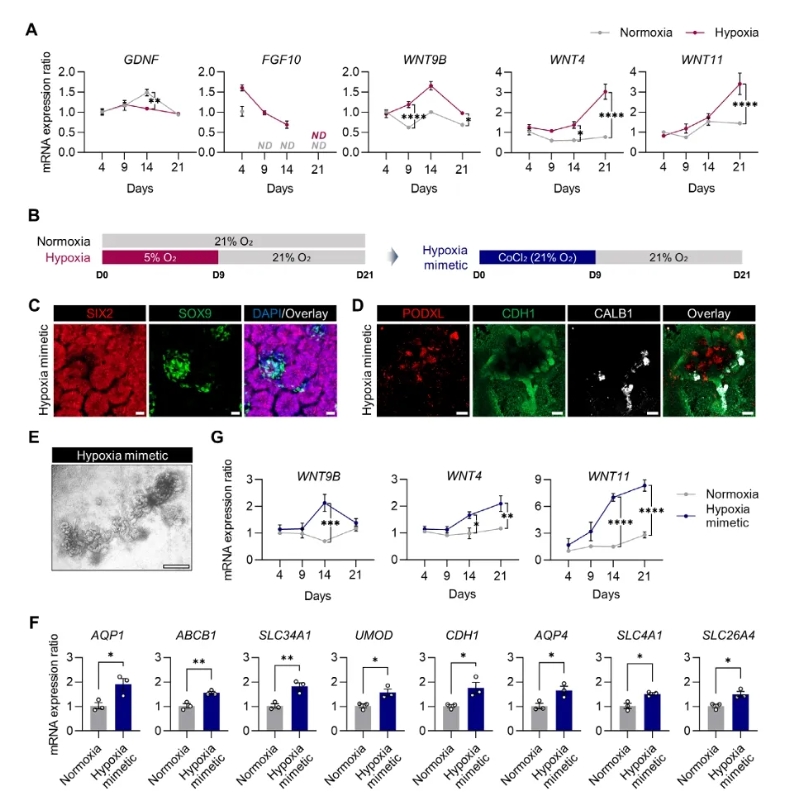
图6. HIF1α介导的互作信号促进小管发育的改善(点击图片查看大图)
在图7中,作者验证了缺氧类器官在疾病建模和药物测试中的应用潜力。A 图展示了实验流程:先用 Forskolin 处理 48 小时诱导囊泡形成,模拟 PKD 模型,再在 24 小时内加入 Niclosamide 或 CFTR 抑制剂-172 进行干预。B 图表明,在缺氧类器官中,PKD 相关通道基因 ANO1 与 CFTR 表达显著上调,提示其对囊泡形成更敏感。C–D 图显示,Forskolin 在缺氧类器官中诱导的囊泡显著更大,说明其更接近病理状态。随后 E–F 图发现,Niclosamide 能明显抑制囊泡膨胀,且缺氧类器官对药物的反应更显著。类似地,G–H 图表明 CFTR 抑制剂-172 也能有效缩小囊泡,进一步验证了药物敏感性。综上,Figure 7 说明缺氧增强的肾类器官不仅能更真实地重建 PKD 囊泡病变,还能作为药物筛选和疗效评估的可靠平台。
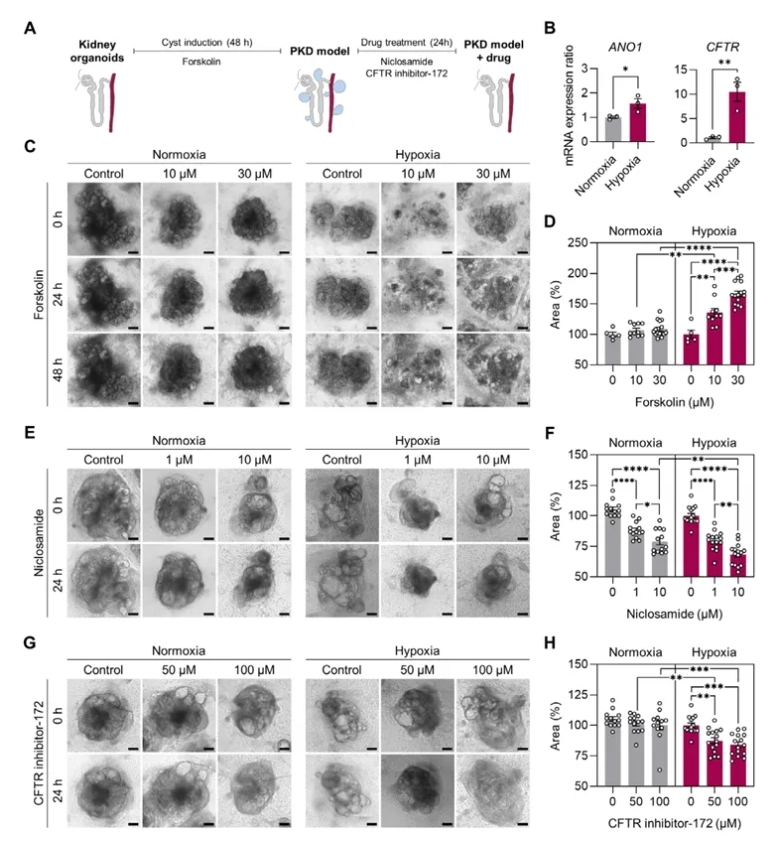
图7. 缺氧增强型肾类器官在 PKD 建模与药物测试中的应用(点击图片查看大图)
总结与展望
本研究首次证明,在肾类器官早期分化阶段引入适度缺氧,可显著提升原始条的诱导效率,推动类器官在同一体系中同时生成 MM 与 UB-like 双谱系,并进一步形成集合管样结构及功能亚型细胞。与传统 protocol 相比,这种方法不仅改善了类器官的组织复杂性,还赋予其更接近体内肾脏的功能属性,包括近端再吸收、远端/集合管钠转运等关键生理过程。同时,缺氧增强的类器官在 PKD 囊泡形成与药物筛选、肾毒性检测中表现出更真实的疾病表型,展示了其作为高阶疾病建模平台的应用潜力。
展望未来,这一研究为肾类器官的发展提供了新的思路:
机制层面:需进一步解析 HIF1α 与 WNT/GDNF 信号在谱系双诱导中的精确调控机制。
模型拓展:结合基因编辑(如 PKD1/PKD2 突变 hiPSC),有望建立更接近患者病理的遗传性肾病模型。
临床转化:优化规模化培养与标准化流程,将缺氧增强的高阶类器官用于药物筛选、肾毒性评估,甚至探索功能替代疗法的可能性。
参考文献:
Lim H, Kim D, Yoon H, Kang JH, Kim YJ, Kim DS, Park TE. Developmental Hypoxia Enhances Kidney Organoid Complexity and Maturity. Adv Sci (Weinh). 2025 Aug 21:e01661. doi: 10.1002/advs.202501661. Epub ahead of print. PMID: 40841925.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

