肾类器官展现新价值:成功解析发育中线粒体重排机制
本研究阐明了肾脏发育过程中近端小管线粒体空间重排的核心机制。研究发现,随着肾小管腔内流体流动启动,线粒体从细胞顶端迁移至基底侧,与Na-K ATP酶共定位以满足局部能量需求。利用人源肾类器官模型,研究锁定LRRK2激酶为关键调控因子,证实流体剪切力通过下调LRRK2磷酸化水平,解除其对线粒体迁移的抑制作用,从而促进线粒体基底侧定位。该研究首次建立了“流体剪切力-LRRK2失活-线粒体重定位”的完整调控轴,揭示了肾脏发育中能量供给系统建立的新机制,为理解LRRK2相关肾病及线粒体功能障碍提供了重要理论基础。

近日,美国Rogosin研究所Leif Oxburgh教授团队联合多所研究机构在《Nature Communications》(IF 15.7)发表研究,系统阐明了发育中肾近端小管线粒体由顶端向基底侧迁移的核心机制。
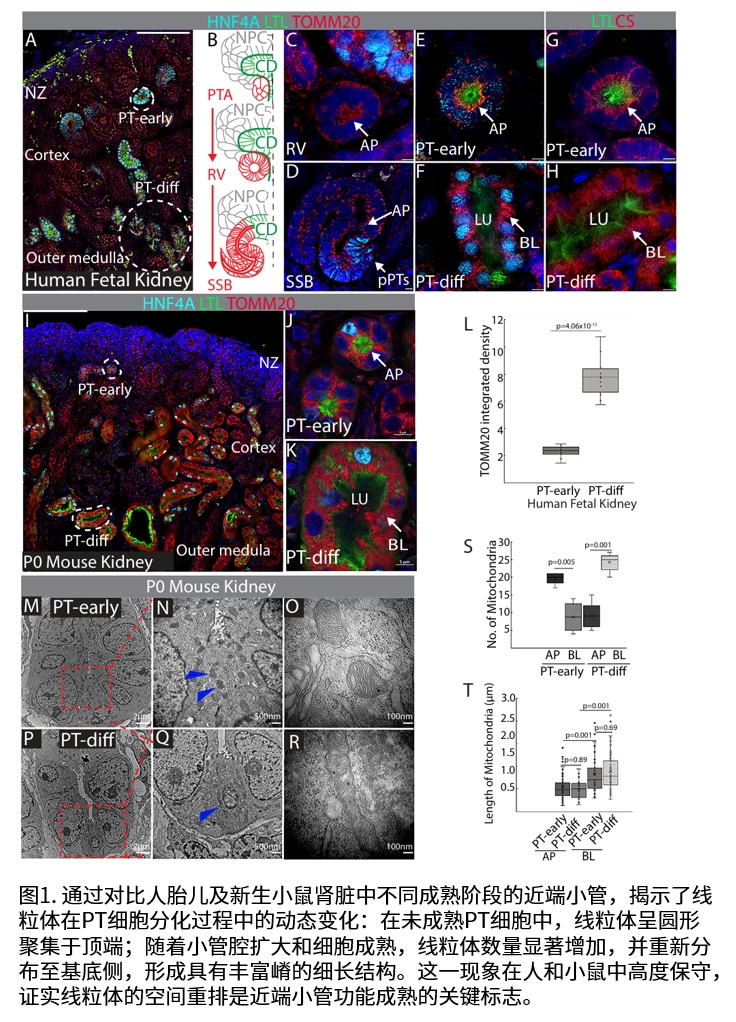
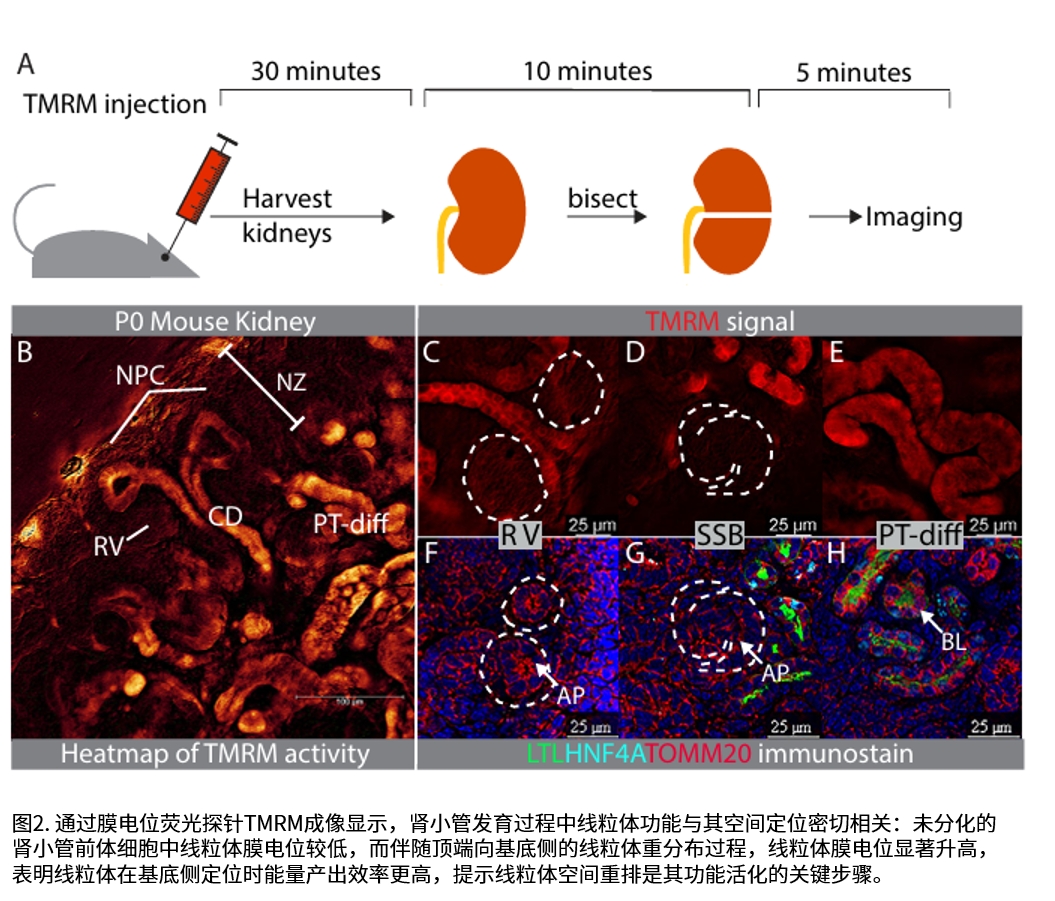
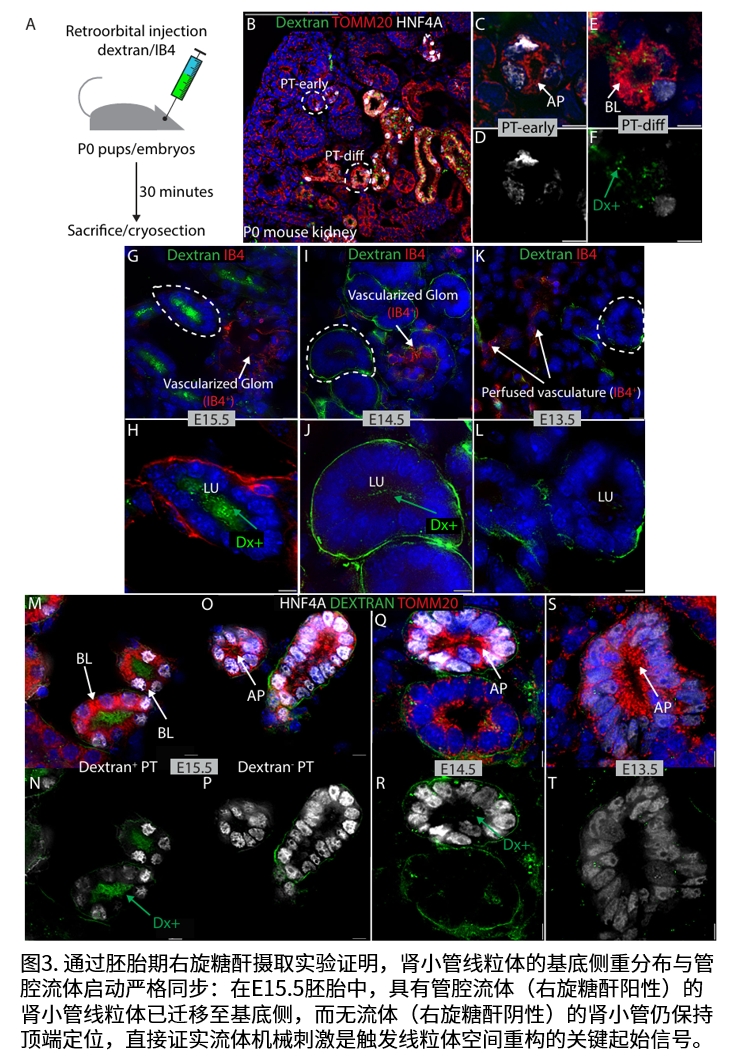
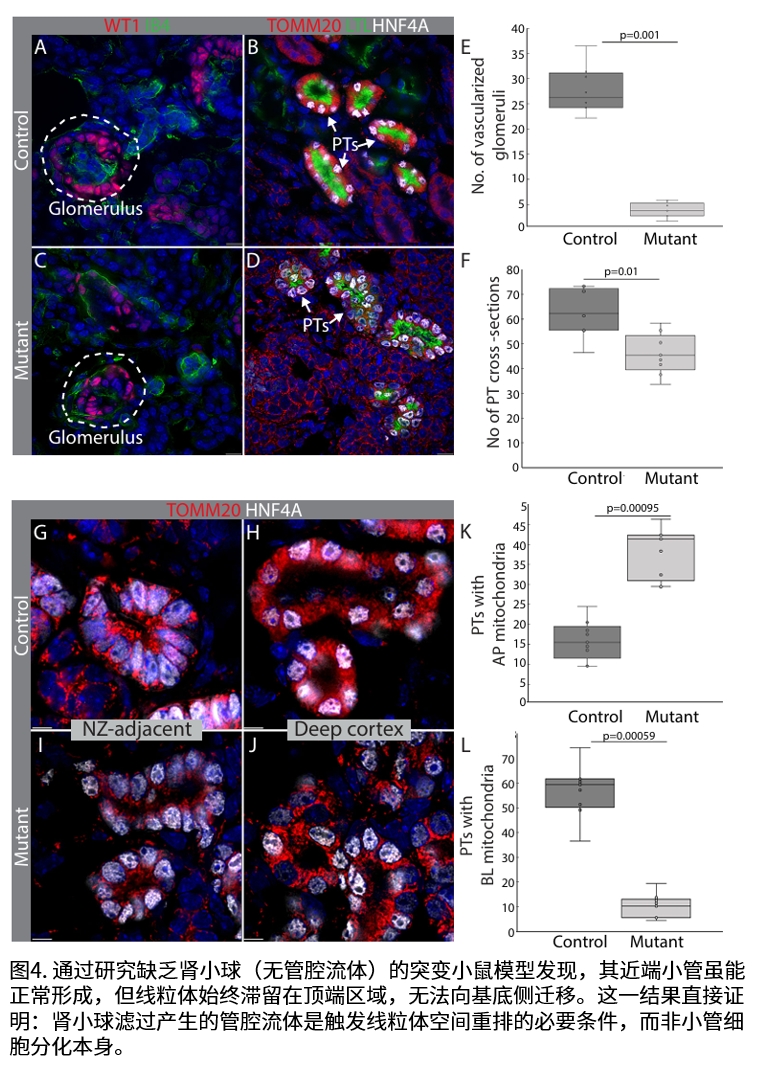
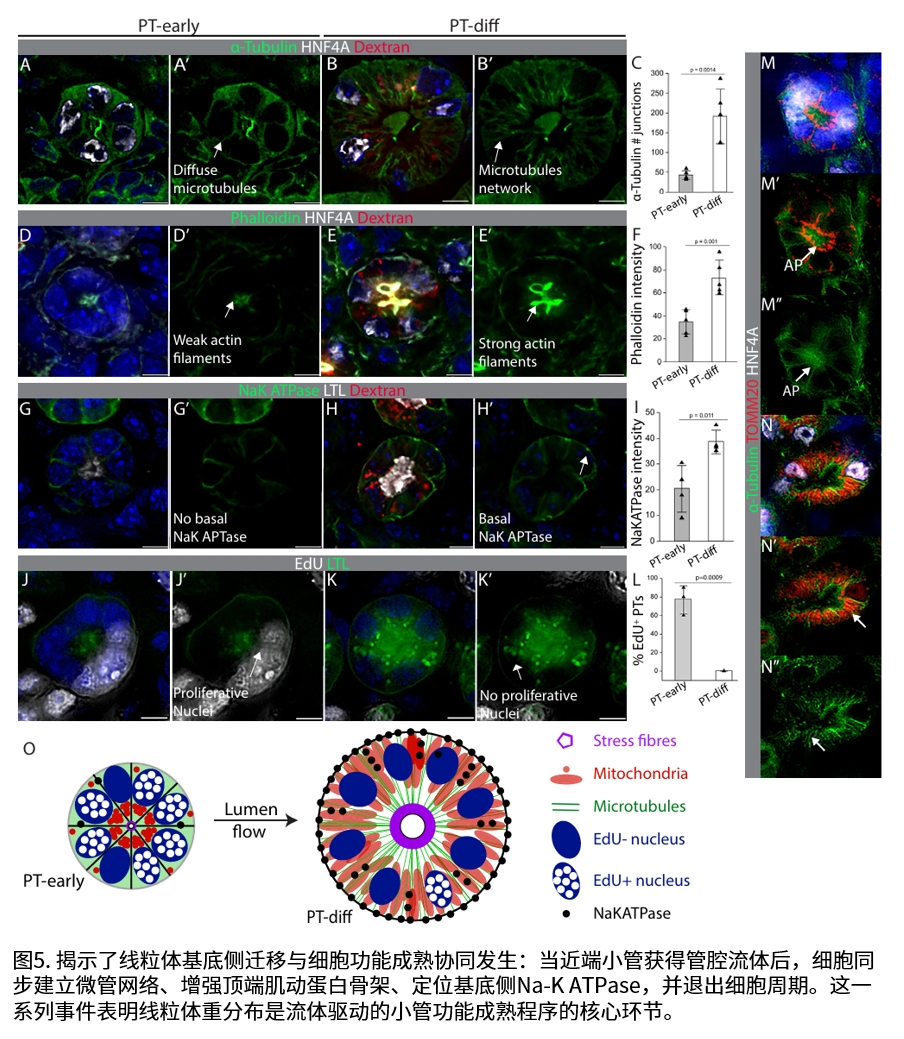
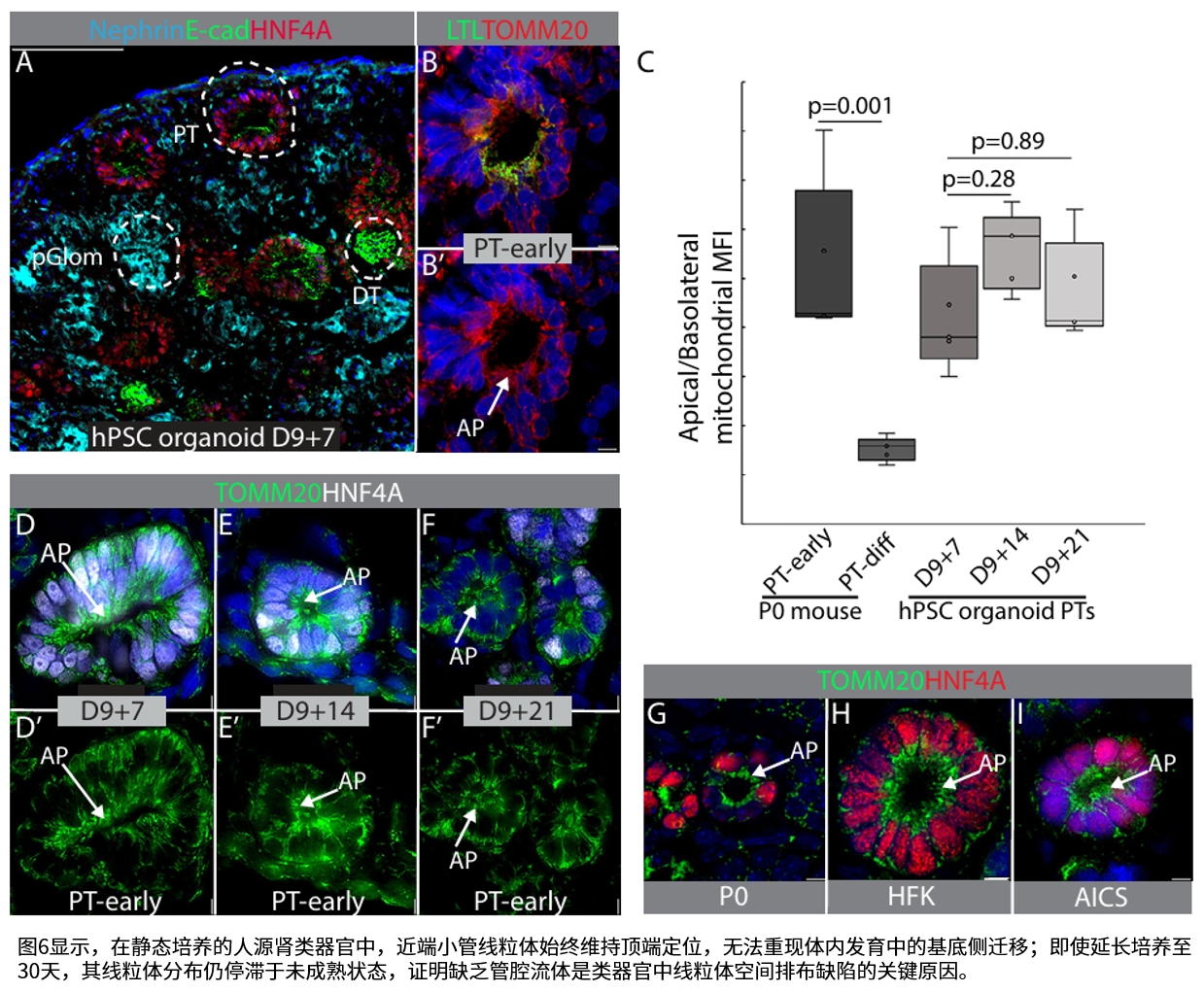
研究团队发现,随着肾小管腔内流体流动的启动,线粒体从顶端的初始位置重新分布至基底侧,与能量需求部位Na-K ATP酶共定位。这一重排过程与细胞功能成熟同步:在无滤过功能的突变小鼠模型中,线粒体滞留于顶端;而在功能活跃的肾小管中,线粒体完成基底侧迁移并伴随能量输出显著提升。
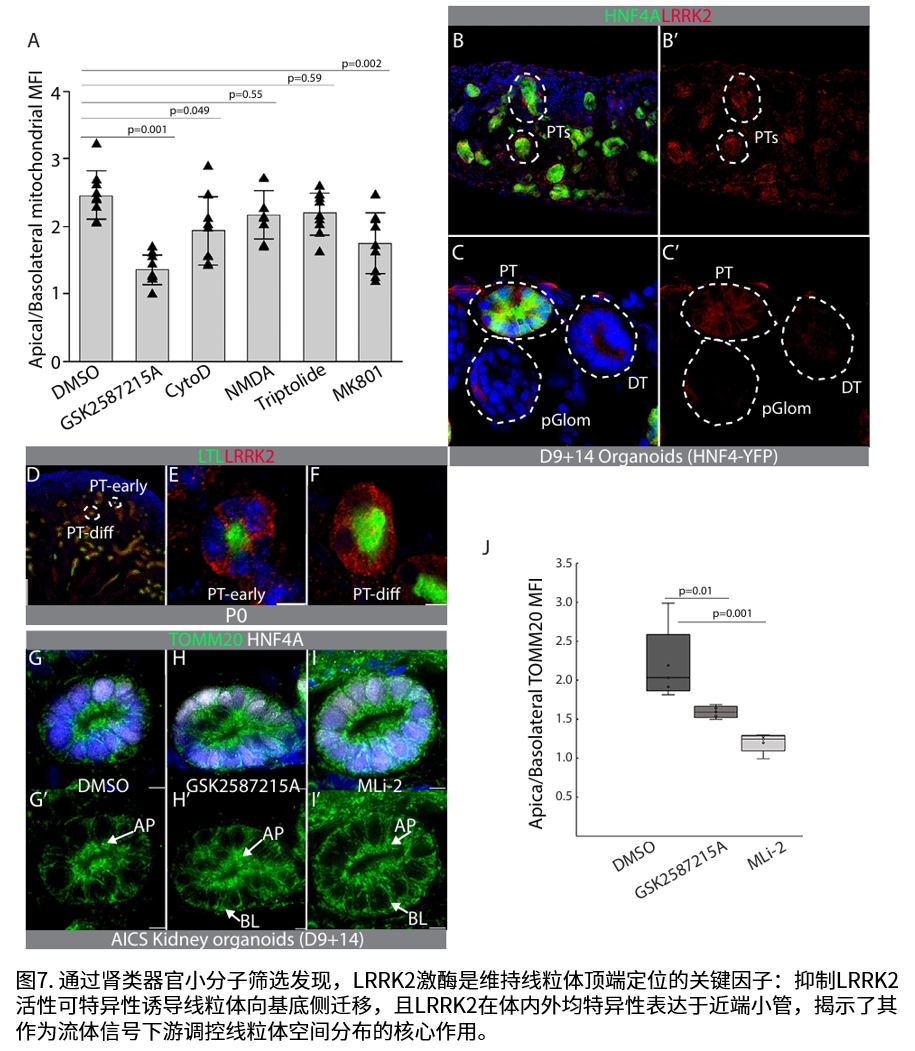
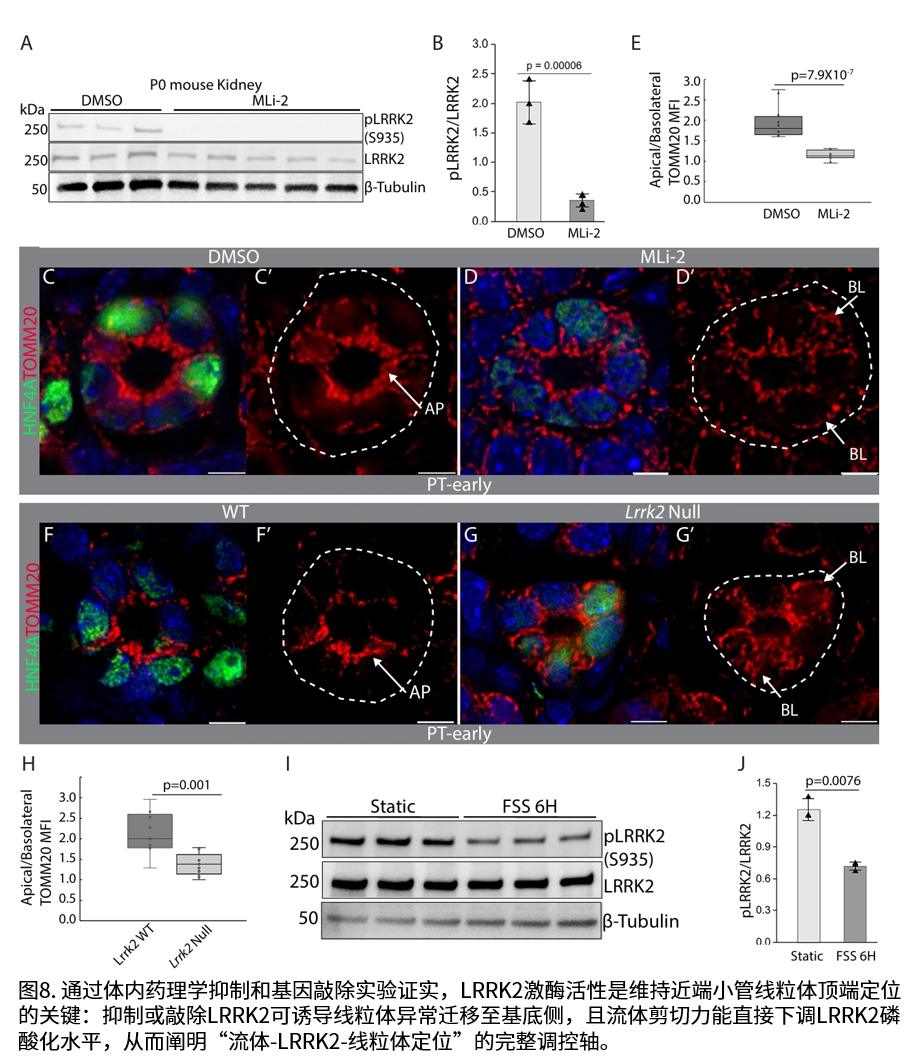
通过人源肾类器官模型验证,研究锁定LRRK2激酶为调控此过程的关键因子。抑制LRRK2活性可促进线粒体向基底侧迁移。机制上,研究首次证实流体剪切力通过下调LRRK2磷酸化水平,解除其对线粒体迁移的抑制作用。
该研究构建了“流体剪切力-LRRK2失活-线粒体重定位”的完整调控轴,揭示了肾脏发育中能量供给系统建立的新机制,为理解LRRK2相关肾病及线粒体功能障碍提供了新视角。
参考文献
Khan, Mohsina et al. “Mitochondrial organization in the developing proximal tubule is controlled by LRRK2.” Nature communications vol. 16,1 9611. 30 Oct. 2025

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

扫码关注华津生物的官方微信
