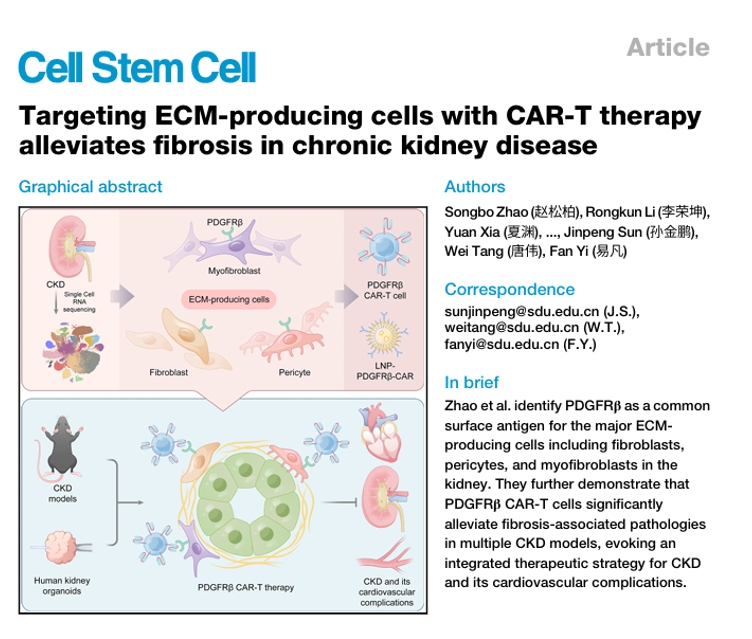
慢性肾病以细胞外基质(ECM)异常沉积和肾纤维化为共同病理基础,与心血管并发症相互牵连,迫切需要能够直接干预纤维化进程的治疗策略。这项研究基于单细胞层面的证据,将成纤维细胞、周细胞与肌成纤维细胞界定为肾脏主要ECM产出细胞,确定血小板衍生生长因子受体β(PDGFRβ)为其共性表面抗原,并据此构建抗纤维化CAR-T方案。
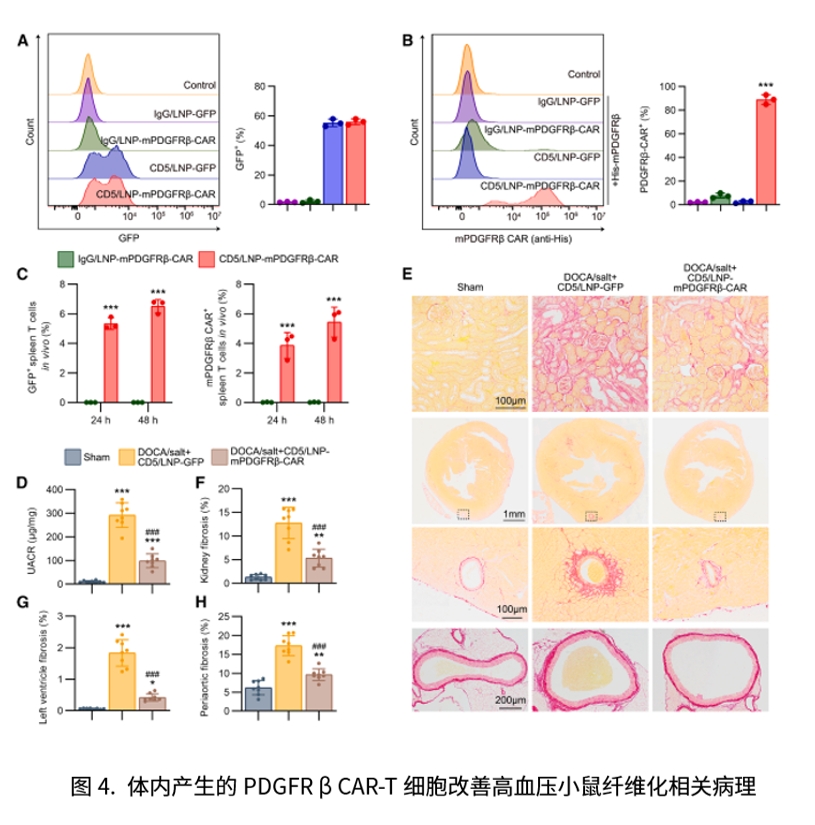
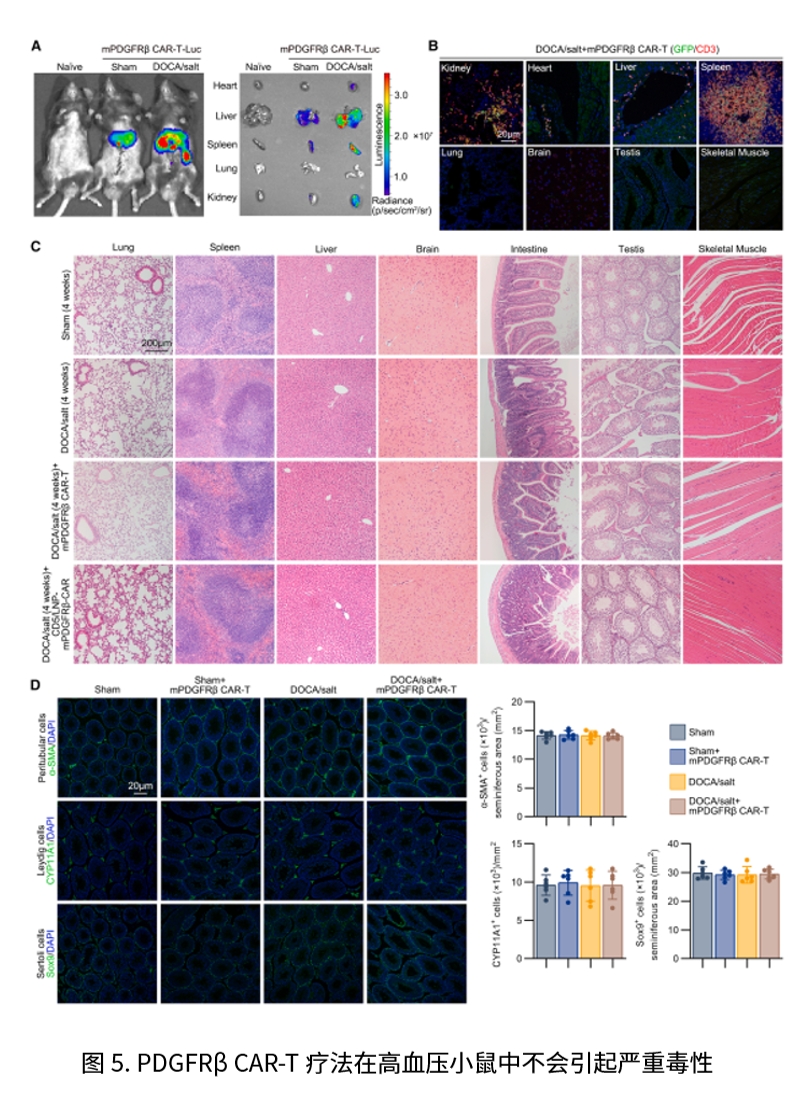
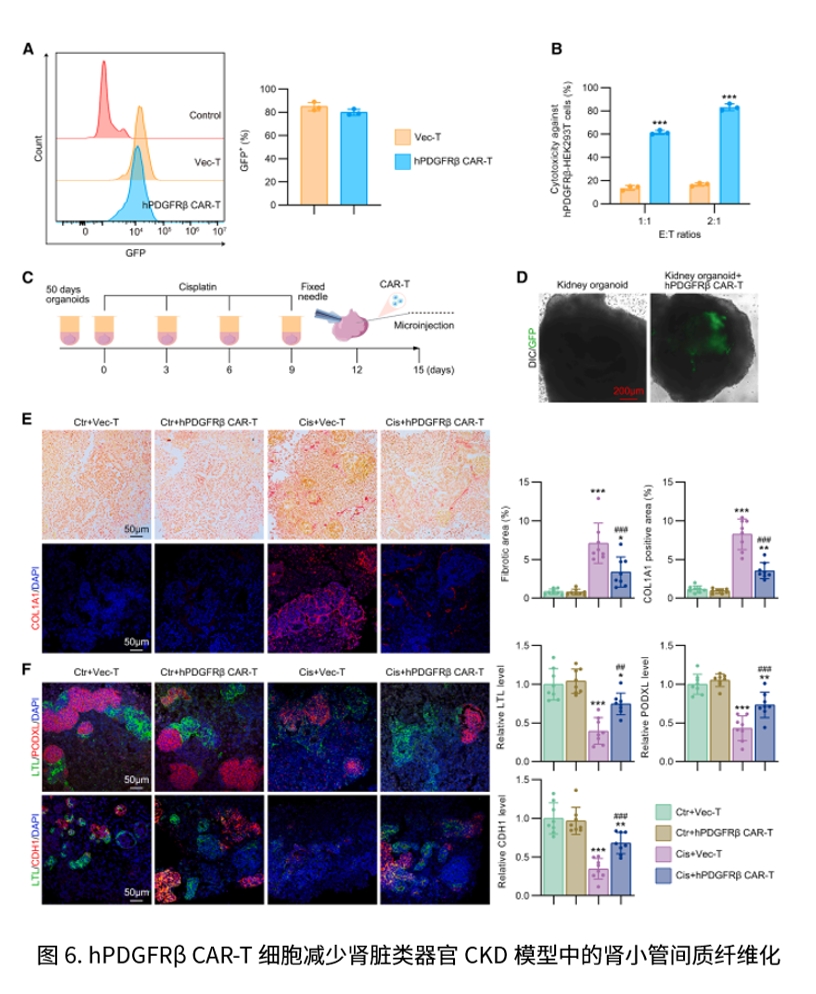
在DOCA/salt高血压、UUO及STZ/HFD诱导的糖尿病肾病等模型中,研究分别通过体外回输与CD5/LNP在体内转导两种路径生成PDGFRβ CAR-T,均观察到肾功能改善并且肾、心肌间质与周血管纤维化下降;体内监测显示CAR表达在给药后出现峰值并随时间下行。在人源肾类器官的顺铂致纤维化模型中,人源化hPDGFRβ CAR-T减少胶原沉积,并改善LTL、CDH1、PODXL等指标,对正常类器官未见on-target/off-disease毒性。系统安全性评估亦提示主要脏器形态、血液与炎症等指标未出现显著异常,最长12周未见严重毒性。综合动物与类器官两条证据链,作者提出以同时靶向多类ECM产出细胞为思路,构建了从前期验证走向潜在转化的清晰路径,并指向肾—心血管系统的协同获益。
研究亮点
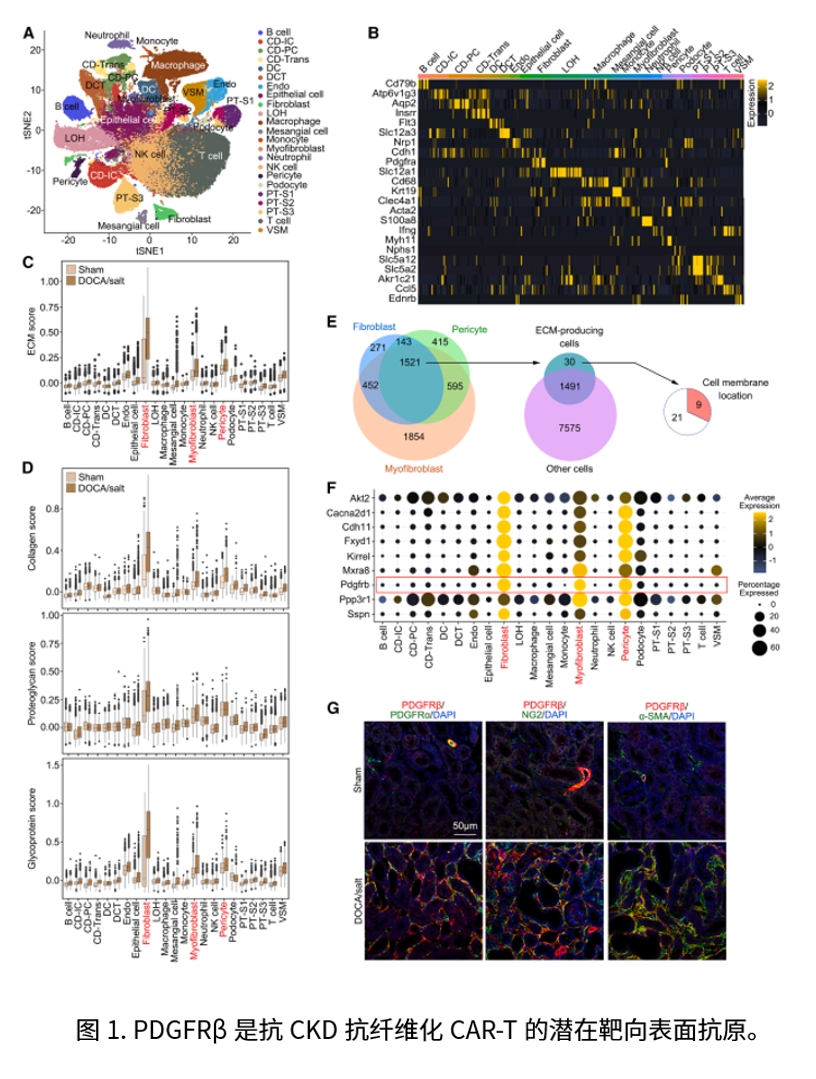
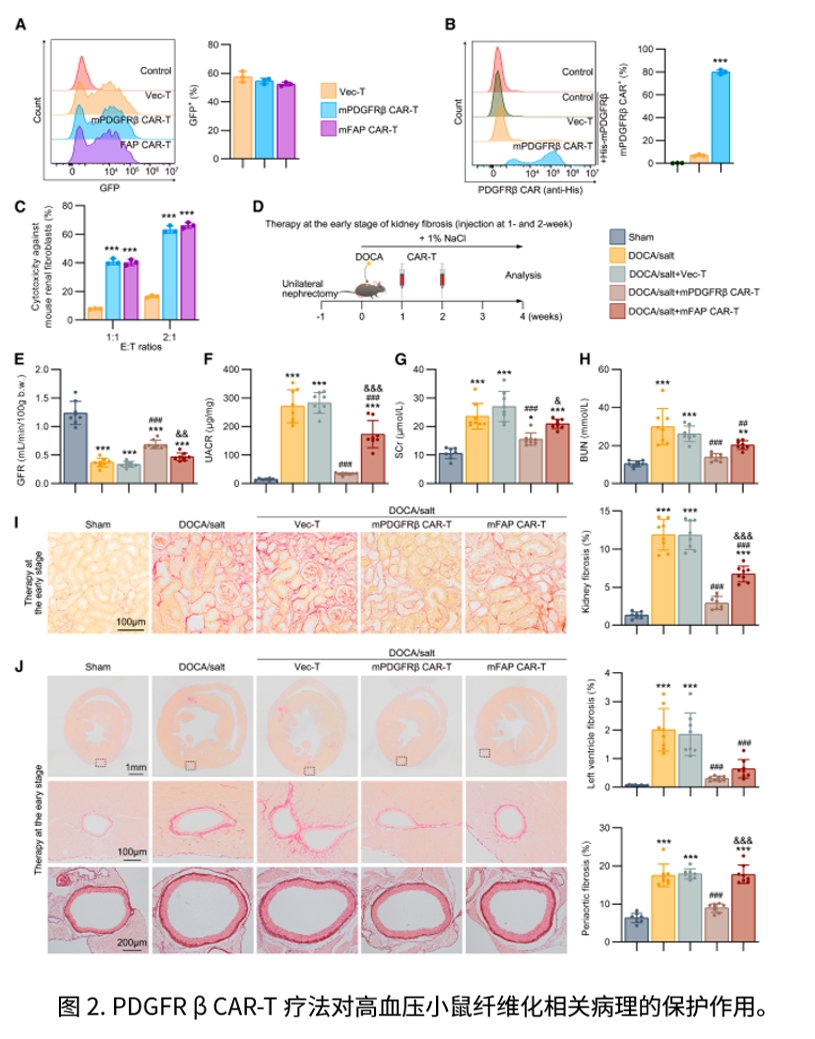
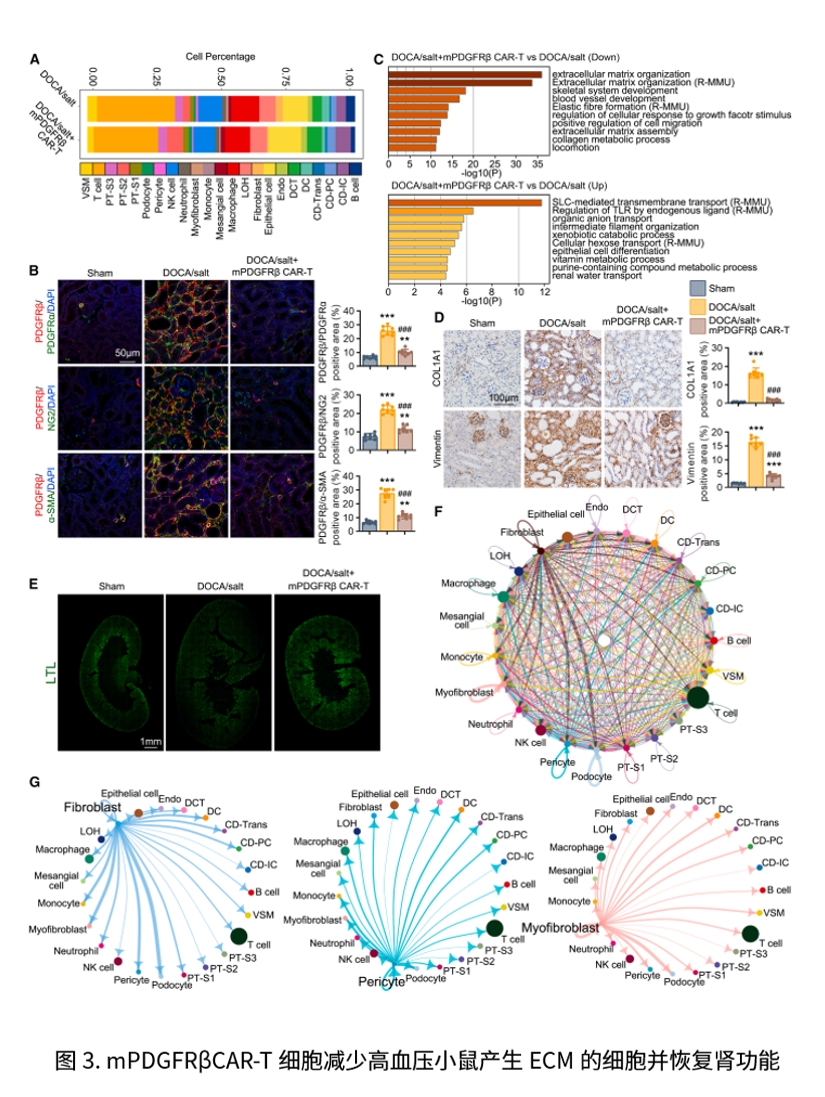
意义与展望
本研究的创新点在于把“动物模型验证”与“人肾类器官验证”紧密衔接:前者显示PDGFRβ CAR-T无论采取体外回输还是CD5/LNP体内转导,均能在多种CKD模型中改善肾功能并减轻肾、心肌间质及周血管纤维化,奠定疗效与安全的体内证据;后者在人源顺铂致纤维化类器官中进一步证明其可显著降低胶原沉积、改善近端/远端肾小管与足细胞标志(LTL、CDH1、PODXL),且对正常类器官未见on-target、off-disease毒性,从而补足了动物实验在人类相关性与组织特异安全评估上的空白,形成清晰的“动物—类器官—转化”路径。展望来看,以类器官作为PDGFRβ CAR-T的前置筛选与安全窗口平台,并与两种给药路径的动物数据联动,有望用于优化剂量与给药时序、监测短暂表达与风险边界,并在多靶点组合与更系统的早期/长期安全评估后,推动进入临床检验。

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

