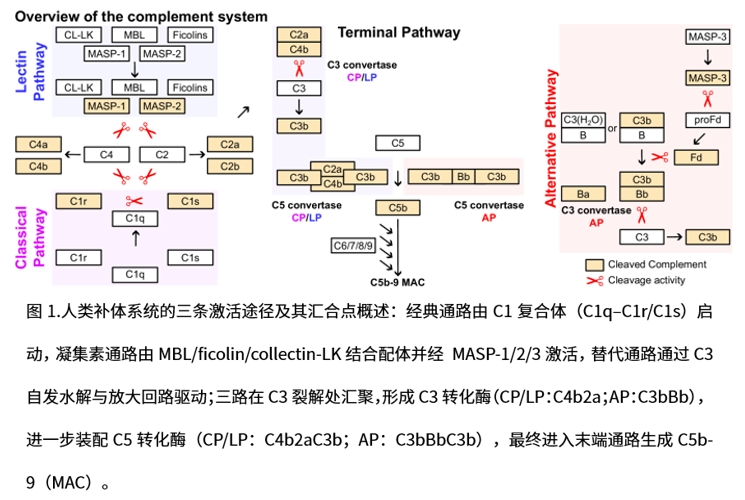
补体C3新片段 C3-LHF1:从血浆蛋白水解到肾类器官的免疫信号“桥梁”
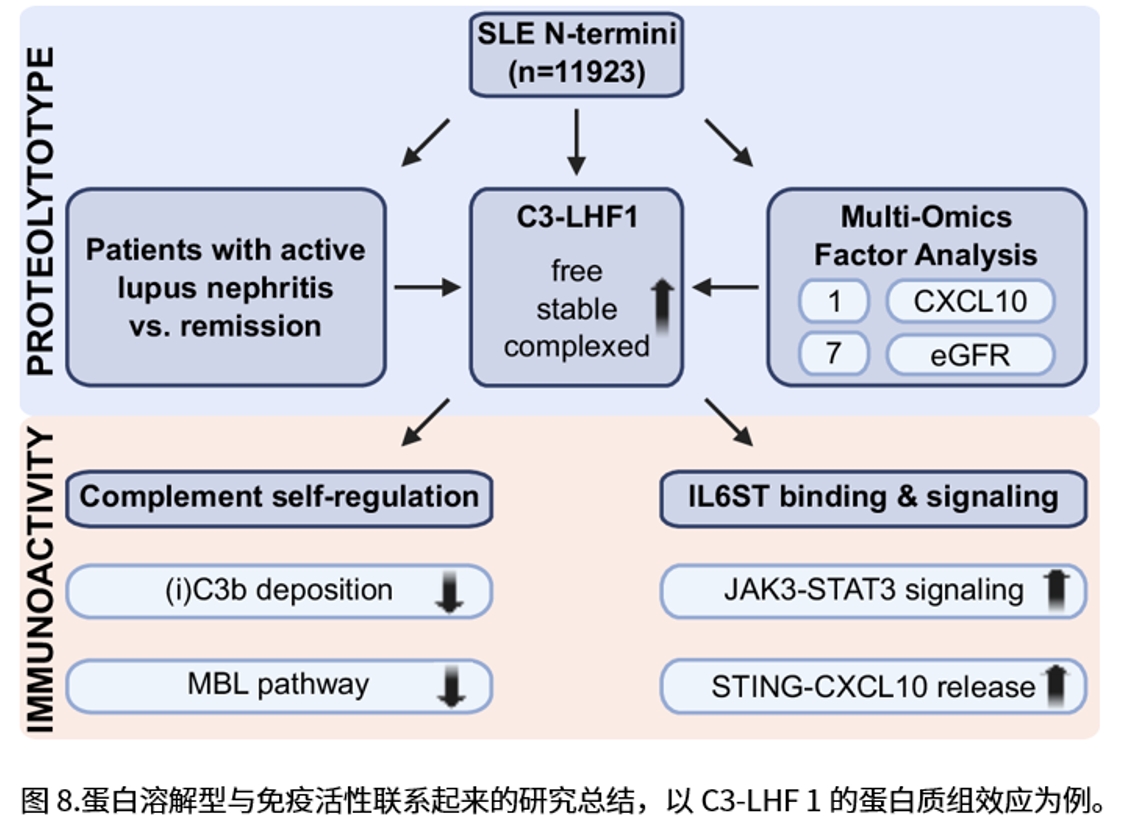
本研究在狼疮肾炎患者血浆中鉴定出新补体C3片段C3-LHF1。体外实验证实其由MASP-1/3切割产生,并能抑制经典与凝集素补体通路。关键机制上,C3-LHF1在人源肾类器官中激活gp130-JAK/STAT3通路,诱导IL6ST/gp130自磷酸化,上调足细胞nephrin磷酸化并降低足细胞标志蛋白,直接参与足细胞损伤。该片段在患者血浆中稳定存在,揭示了其作为补体系统与肾脏损伤间的新型免疫信号桥梁,为狼疮肾炎机制研究与靶向治疗提供了新方向。

本研究由丹麦奥胡斯大学的Fatih Demir和德国汉堡大学医学中心的 Markus M. Rinschen联合领导,于2025年10月发表于《The EMBO Journal》。研究团队基于可扩展的血浆N-terminomics(SHUNTER)技术,在系统性红斑狼疮及狼疮肾炎背景下鉴定出新的补体C3片段C3-LHF1,并揭示其在肾类器官中通过gp130-JAK/STAT3通路介导免疫信号与足细胞损伤的机制。
研究亮点
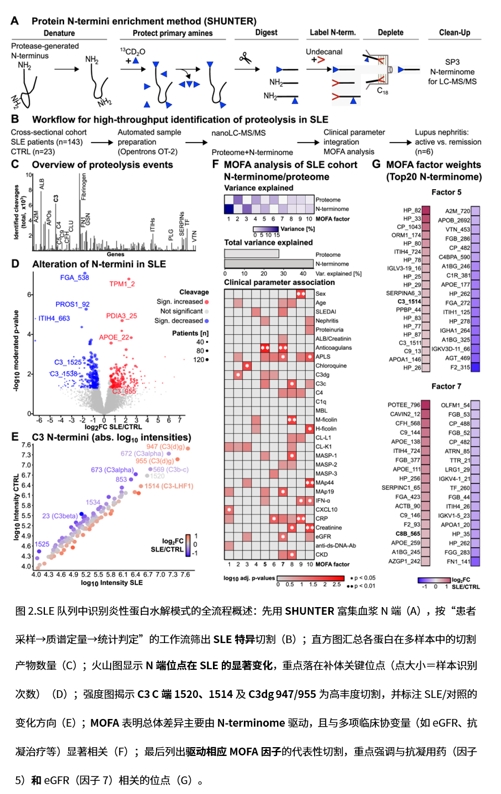
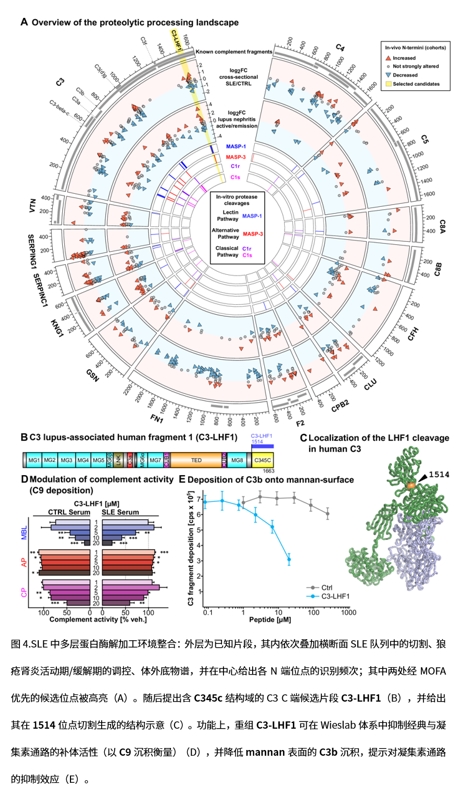
1. 用血浆N-terminomics锁定新C3片段:研究采用改良的N-terminomics(SHUNTER)在患者血浆中系统富集并定量蛋白质新生N端位点;在补体C3的C端发现1514位点切割能释放独立片段,由此提出候选C3-LHF1进入功能验证,奠定后续机制学研究的标的基础。
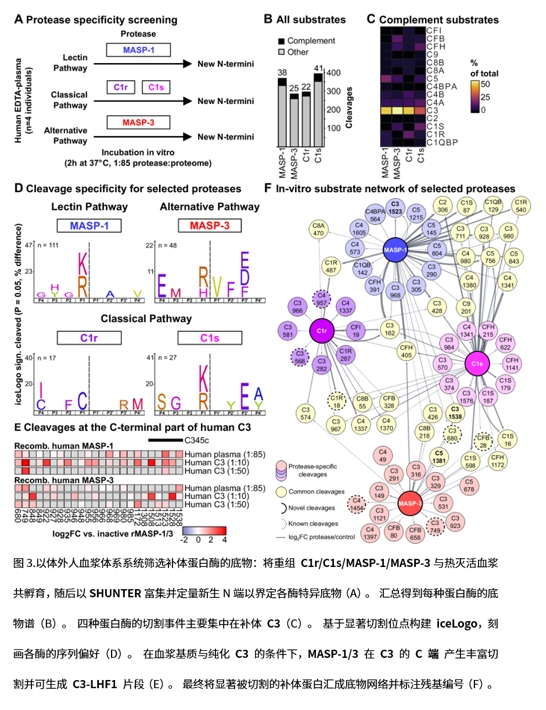
2. 体外酶学为“片段从何而来”提供证据:在人血浆与纯化体系中,通过MASP-1/3(并结合C1r/C1s)进行酶谱映射,观察到C3C端的MASP依赖性切割富集,为体内产生C3-LHF1的来源路径提供直接的酶学支持。
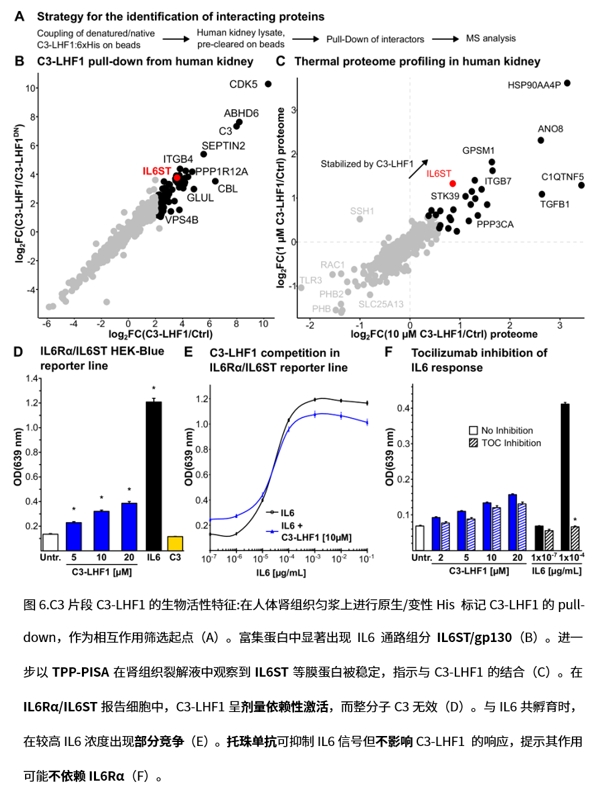
3. 抑制经典与凝集素通路补体活化:重组C3-LHF1在Wieslab体系中显著降低C9沉积,对经典与凝集素通路抑制明确,而对替代通路影响较弱;在mannan表面读出中还可降低C3片段沉积,提示其对上游补体激活具有负调控作用。
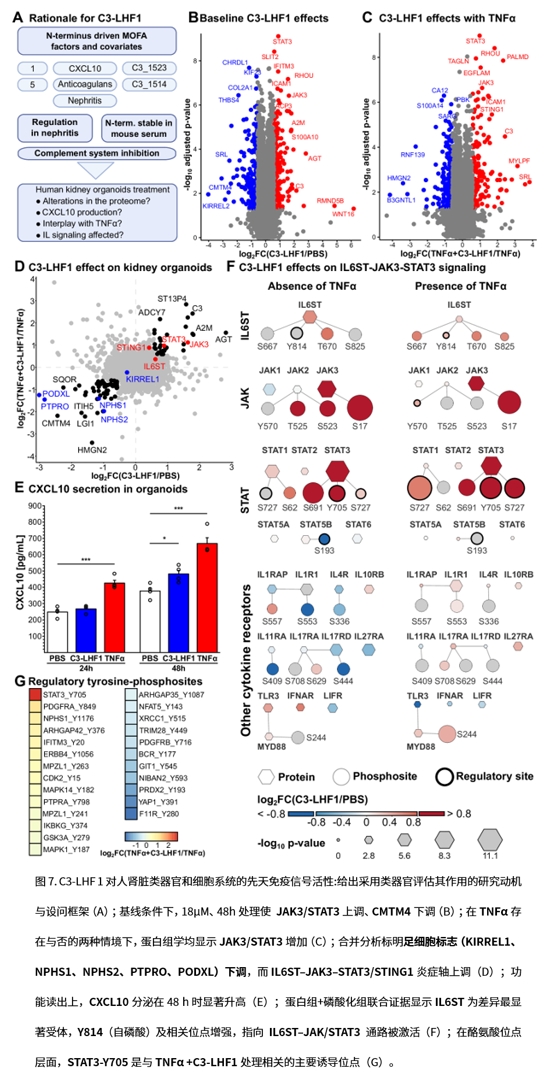
4. 在人源肾类器官激活gp130-JAK/STAT3并影响足细胞表型:在人肾脏类器官中,C3-LHF1诱导IL6ST/gp130自磷酸化并主导JAK3-STAT3通路,即使在TNFα存在时亦然;同时观察到nephrin(足细胞)磷酸化上升与足细胞标志蛋白整体下降。
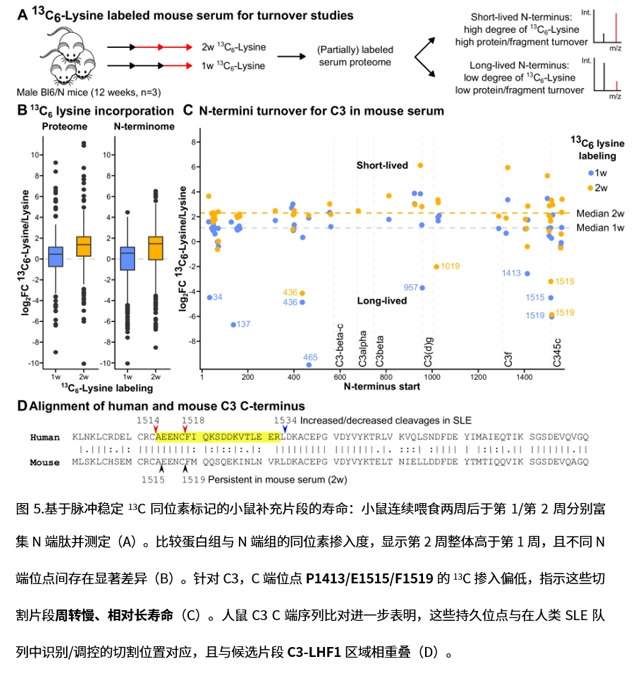
5. 体内相关性:在 LN 患者血浆中,SEC 分级结合 N-terminome 显示 C3 的 1514/1520/1534 位点 N 端洗脱晚于整分子 C3,位于 C3b 与 C3(d)g 之间,提示对应片段以游离或与 C3c 相关的形态存在;小鼠 ^13C-赖氨酸脉冲标记进一步表明 C3 C 端多处 N 端呈低掺入、长寿命特征,支持其在循环中的相对稳定。
意义与展望
本研究将蛋白水解网络与肾实质细胞信号贯通:在人肾类器官中,C3-LHF1激活IL6ST/gp130–JAK/STAT3,提高CXCL10分泌,并伴随nephrin磷酸化上升与足细胞标志下调,确立其为可塑造肾组织炎症反应的免疫活性介质而非惰性片段。体内生成与调控尚待厘清:尽管MASP-1/3在体外可产生该片段,真实的上游剪切酶及患者/疾病特异性辅因子仍需鉴定。作者提供了可查询的在线/源数据资源,便于后续功能挖掘;同时,论文建议系统探索补体—凝血—纤维化的交互,为转化研究提供方向。
参考文献
Demir et al. The EMBO journal, 10.1038/s44318-025-00598-8. 27 Oct. 2025

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

扫码关注华津生物的官方微信
