
这篇于2022年发表于Nature Genetics的经典论文由德国亚琛工业大学(RWTH Aachen University)实验医学与系统生物学研究所和肾脏病学与临床免疫学科的Rafael Kramann团队牵头完成,并联合德国海德堡大学计算生物医学研究所、亚琛大学附属医院泌尿及小儿泌尿外科、马丁路德大学(Halle)泌尿及肾移植科等多家德国研究机构协作完成。论文的第一作者为Yaoxian Xu和Christoph Kuppe,通讯作者为Rafael Kramann。
该研究以成人肾脏为起点,成功建立了来源于CD24⁺肾小管上皮细胞的三维类器官体系(adult kidney tubuloids),并通过系统的单细胞与单核转录组分析阐明了其发育轨迹、细胞组成及功能特征。研究进一步通过CRISPR/Cas9成对敲除PKD1/PKD2基因,在体外重建了常染色体显性多囊肾(ADPKD)囊肿病理,并结合患者来源肾组织的单核转录组对比证明tubuloids与真实病灶在关键信号通路(MAPK、mTOR、MYC、cAMP等)及核心基因表达方面高度一致。最终,临床药物tolvaptan在该体系中显著降低cAMP水平并抑制囊肿生长,而在诱导多能干细胞(iPSC)类器官中无明显作用。
作为成人肾类器官研究的奠基之作,这项工作不仅提供了可长期扩增、功能成熟且高度贴近成人肾生理的模型,还为精准疾病建模和药物开发开辟了新的实验与转化路径。
明确起源细胞:锁定成人肾散在分布的CD24⁺上皮细胞,尤其是近端S3段和亨利袢CD24⁺/CD13⁺双阳性群体,作为tubuloids的主要来源。
优化培养体系:提出四阶段培养流程,成球率和肾小管段数显著提升,可长期维持扩增。
结构与功能成熟:类器官呈现出近端肾单位标志。
高保真疾病建模:CRISPR/Cas9成对敲除PKD1/PKD2成功诱导囊肿形成。
准药效验证:临床药物tolvaptan在tubuloids中显著降低cAMP和缩小囊肿,而在iPSC类器官中无效,体现了成人来源类器官在药物筛选中的特异优势。
成人肾tubuloids的起源细胞
研究的起点是阐明成人肾类器官的细胞来源。作者推测在肾小管中存在具有干细胞特性的亚群,因此首先对成人肾组织进行免疫染色与流式分选,鉴定出散在分布的CD24⁺上皮细胞,并与传统的CD13⁺近端小管细胞进行代谢和染色质可及性比较。单细胞转录组分析进一步发现,CD24⁺群体涵盖多个肾单位分段,而CD13⁺ 细胞主要对应近端S1/S2区域。培养实验显示,CD24⁺细胞尤其是近端S3段和亨利袢薄段的CD24⁺/CD13⁺双阳性群体拥有最高的类器官形成率和扩增潜力,确立了CD24⁺细胞是tubuloids的关键起源。
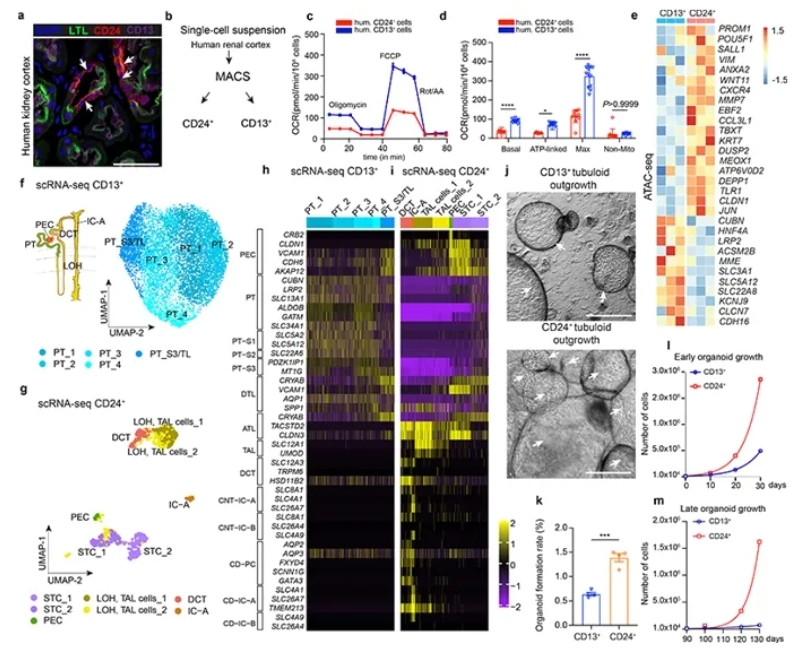
图1. 人肾组织中散在的CD24⁺上皮细胞与近端小管标志物CD13/LTL共定位(a),经分离后代谢分析表明其基础及最大氧耗率显著低于CD13⁺细胞,提示代谢活性低、具干细胞特征(c–d)。ATAC-seq揭示两者在基因启动子区的染色质开放模式存在差异(e)。单细胞测序及UMAP分析显示,CD13⁺细胞主要对应近端小管及亨利袢薄段,而CD24⁺细胞则涵盖远曲小管、亨利袢粗升支、集合管A型插入细胞等多种节段(f–g),并通过KPMP标志基因表达得到验证(h–i)。在体外培养中,CD24⁺细胞形成的肾小管类器官具有典型囊样结构且形成率显著高于CD13⁺,并能在早晚期持续增殖(j–m),确立了CD24⁺细胞是人肾类器官的主要起源。
优化培养体系以维持和扩增多样的肾单位谱系
在明确起源后,作者比较了传统单阶段培养与改良的四阶段(4-phase)培养方案。结果显示4-phase协议显著提高了类器官的成球率和每个类器官的肾小管段数量。单细胞转录组分析早期(第21天)与长期(第97天)的类器官,确认主要细胞群为近端小管来源的tubuloid progenitor cells (TPC),且长期培养后仍可维持增殖型TPC,并包含少量远端样细胞群。
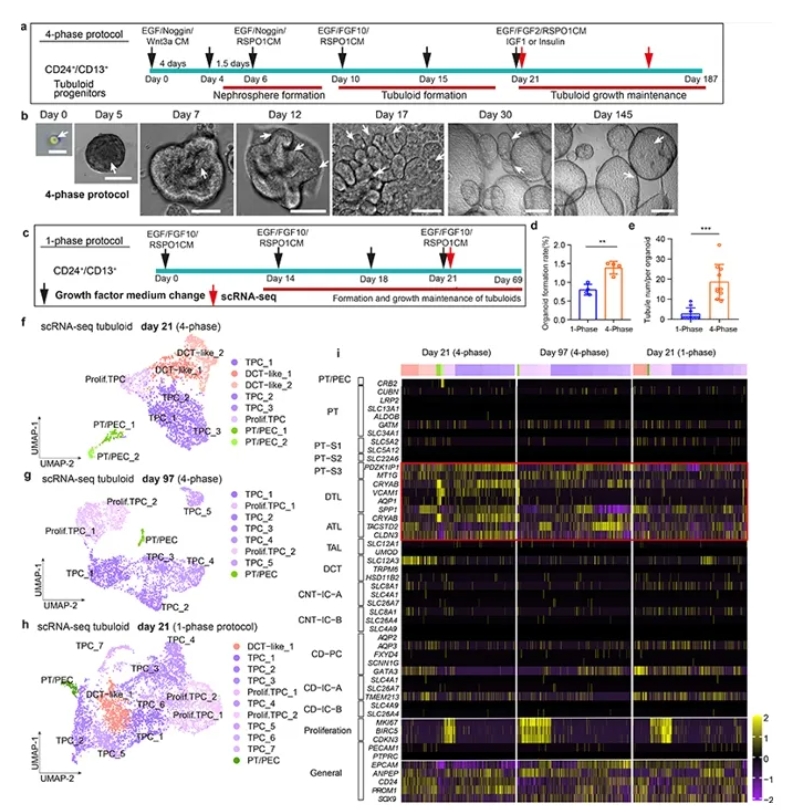
图2. CD24⁺细胞来源tubuloids的培养流程和单细胞测序结果。作者建立四阶段(4-phase)培养方案,并在关键时间点更换培养基和生长因子,同时进行单细胞RNA测序(a)。代表性图像显示从接种到145天,类器官持续生长并形成多分支管道(b)。与传统单阶段(1-phase)相比,4-phase在第22天的类器官形成率更高,且第25天单个类器官中肾小管数明显更多,平均约18根(c-e)。单细胞UMAP分析表明,4-phase早期(第21天)类器官包含8个细胞群,主要为tubuloid前体细胞(TPC1-3)、增殖TPC及少量远曲小管和近端小管/肾小囊上皮细胞(f);晚期(第97天)则以TPC1-5及增殖TPC为主,并保留少量PT/PEC(g)。相比之下,1-phase早期类器官虽有更多细胞群,但以TPC为主且分化有限(h)。关键标志基因的热图分析进一步确认4-phase培养的类器官在早期和晚期均呈现更完整的肾单位谱系及稳定的分化状态(i)。
验证类器官的成熟结构与近端小管功能
基于稳定的培养体系,作者对类器官的结构和功能进行全面检测。免疫荧光和透射电镜显示tubuloids建立了侧顶端极性,形成了典型近端肾单位结构。功能实验进一步证明其具有P-gp介导的外排转运能力:在抑制P-gp的条件下,calcein-AM荧光显著积聚。与iPSC类器官比较,tubuloids缺乏足细胞等非肾小管成分,突显其在成人肾小管研究中的特异性。
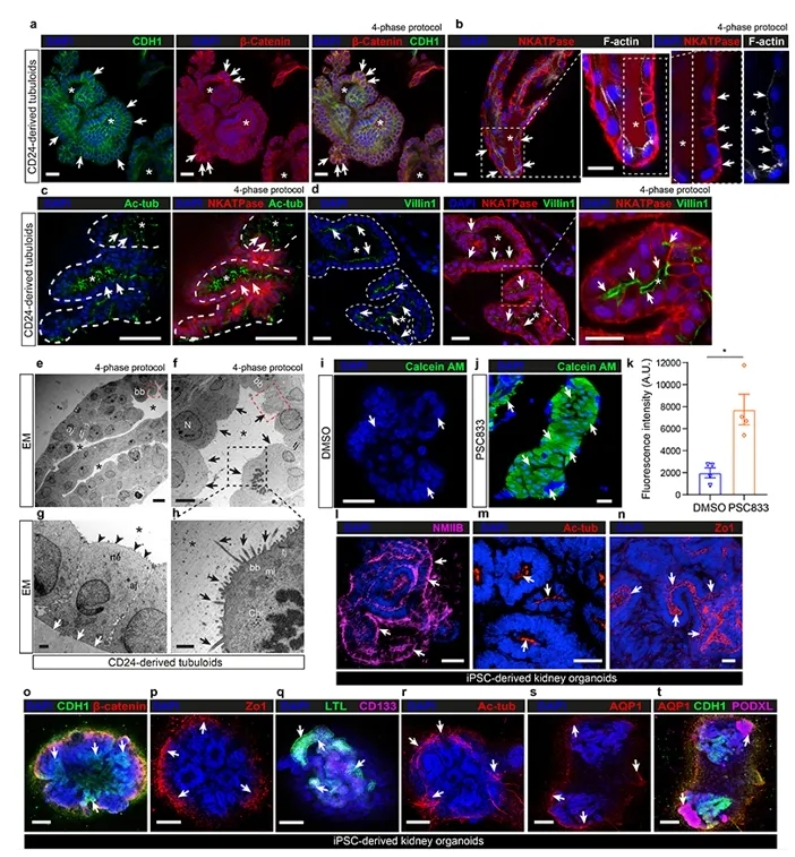
图3. 4阶段培养的CD24⁺细胞来源肾小管类器官的结构和功能成熟度。免疫荧光表明类器官具有典型的上皮极性:表达E-cadherin/CDH1和β-catenin(a)、Na⁺/K⁺-ATPase与顶端F-actin(b)、基底侧乙酰化微管蛋白与 Na⁺/K⁺-ATPase(c),并呈现Villin1阳性刷状缘(d)。透射电镜进一步确认类器官形成了紧密连接、黏附连接、刷状缘、原纤毛等成熟肾小管超微结构(e–h)。功能检测中,在P-gp抑制剂PSC833处理下,calcein-AM在细胞内显著积累,证明其具有典型的近端小管药物外排能力(i–k)。对照的iPSC衍生肾类器官虽然含有NMIIB、ZO1、AQP1、podocalyxin等多种节段细胞并表现出复杂的多谱系结构(l–t),但与CD24⁺tubuloids相比,其纯度较低。整体结果说明,CD24⁺细胞形成的tubuloids在结构和功能上均高度接近成熟的近端肾小管。
构建 PKD1/PKD2 缺失的多囊肾类器官模型
为了验证tubuloids的疾病建模潜力,作者使用成对gRNA-CRISPR/Cas9敲除PKD1 和PKD2。在标准3D培养下,编辑后的类器官可自发形成囊肿,但比例相对较低。基于已知cAMP与肌球蛋白驱动囊肿的机制,研究者进一步添加forskolin(升高 cAMP)、blebbistatin(抑制肌球蛋白II)并采用悬浮培养,结果显著增加囊肿的发生率与体积,成功重建了常染色体显性多囊肾(ADPKD)的核心病理特征。
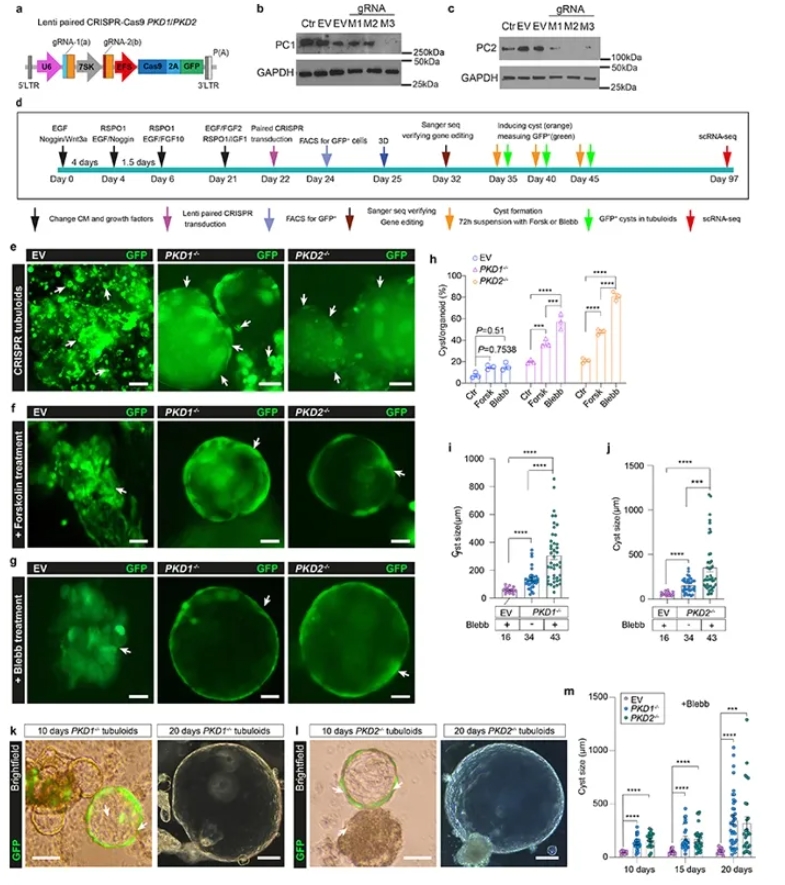
图4. 利用CRISPR/Cas9构建PKD1/PKD2缺失的人肾小管类器官并诱导囊肿形成。作者设计了包含U6与7SK成对gRNA的慢病毒载体(a),在CD24⁺tubuloids中实现高效基因敲除,并通过 Western blot验证PKD1与PKD2蛋白的缺失(b–c),实验时间线如图示(d)。转导后10天,PKD1⁻/⁻和PKD2⁻/⁻类器官形成明显囊肿,而对照组未见变化(e)。进一步处理显示,cAMP激动剂forskolin和肌球蛋白II抑制剂blebbistatin能显著提高PKD缺失类器官的囊肿发生率和体积,其中blebbistatin作用最强(f–j)。时间序列分析证实,在blebbistatin条件下,PKD1⁻/⁻ 和PKD2⁻/⁻类器官的囊肿在第10天即可明显出现,并在第20天显著增大(k–m)。这些结果表明,成对CRISPR/Cas9敲除PKD1/PKD2能在tubuloids中快速重现成人常染色体显性多囊肾的核心病理特征,且blebbistatin能显著促进囊肿的生成与扩张。
与人ADPKD肾组织的转录组比较揭示高度一致的病理机制
作者采集ADPKD患者与健康供体的肾组织,进行单核RNA测序(n=26,509细胞),发现患者样本在MAPK、EGFR、NF-κB、mTOR、cAMP等通路显著激活,并伴有包括SYNE2、BIRC3、EGR1在内的关键基因上调,而ANPEP、CDH6等基因下调。将PKD缺失tubuloids的单细胞图谱映射到人肾参考图谱后,发现其细胞群主要对应PT_4与TAL_2,且与患者组织共享大量差异通路和基因,证实该类器官模型在分子层面真实再现了人类ADPKD的病理过程。
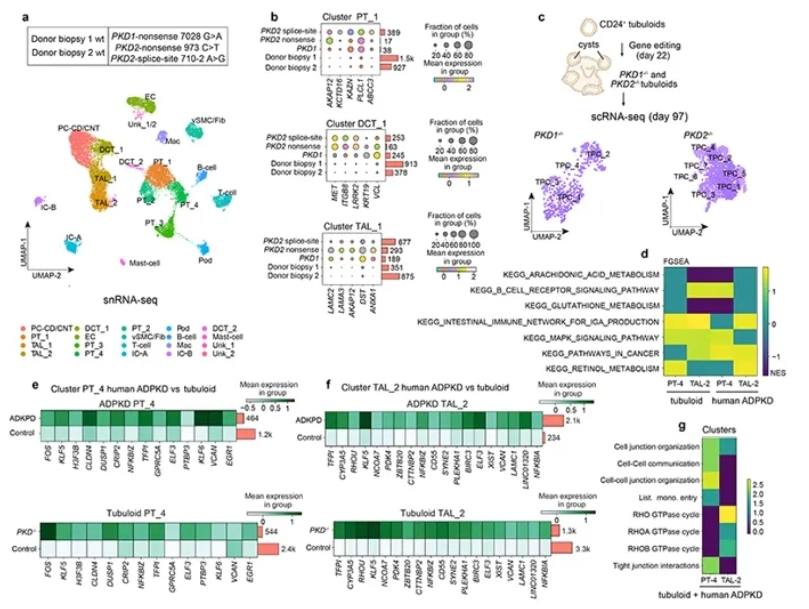
图5. 人类ADPKD(常染色体显性多囊肾)肾组织与PKD基因编辑tubuloids的单细胞转录组比较。研究首先对来自5份人肾组织(含ADPKD与健康供体)共26,509个细胞进行单核RNA测序并UMAP聚类,识别出内皮细胞、巨噬细胞、成纤维细胞、血管平滑肌细胞、近端小管(PT)、足细胞、集合管主细胞、远曲小管(DCT)、粗升支(TAL)等主要群体(a),并筛选出ADPKD相较健康供体上调最显著的5个基因(b)。随后,作者在tubuloids中构建PKD1⁻/⁻与PKD2⁻/⁻模型(4阶段培养),并完成496个与1,483个细胞的单细胞测序,确定主要细胞群为tubuloid 前体细胞(TPC)(c)。将ADPKD组织中PT-4和TAL-2亚群的差异表达基因与tubuloids中对应映射的细胞进行KEGG富集分析,发现两者在MAPK、mTOR、cAMP等关键信号通路中均存在共同异常(d)。进一步筛选出在患者组织与PKD缺失类器官中均上调的核心基因,如PT-4相关的SYNE2、BIRC3等以及TAL-2相关的EGR1、RHOU等(e–f)。Reactome通路富集证实这些共同上调基因集中于细胞连接、Rho GTP酶信号等关键过程(g),整体表明PKD基因编辑tubuloids在分子和通路层面与人ADPKD肾组织高度一致。
托伐普坦在 PKD 类器官中的药效验证
在AVP刺激提高cAMP水平后,作者对PKD1⁻/⁻与PKD2⁻/⁻类器官分别加入临床用药托伐普坦(tolvaptan),观察到其显著降低cAMP并呈时间依赖性缩小囊肿直径。对照实验显示,在iPSC衍生肾类器官中托伐普坦未能产生相同效果。进一步的转录与免疫证据表明,这一差异与AVPR2在tubuloids中的高表达有关,明确了该体系可直接用于临床候选药物的机制评估与疗效预测。
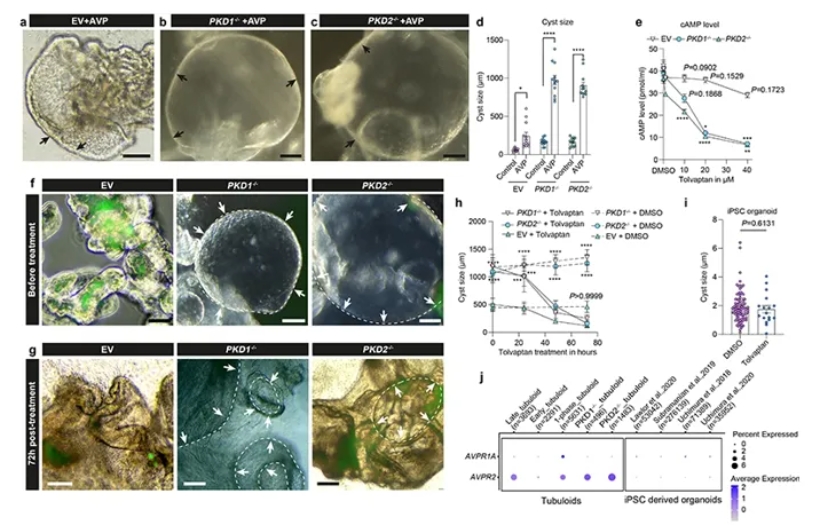
图6. 托伐普坦(tolvaptan)在PKD基因编辑tubuloids中的药效验证。首先,AVP(加压素)处理显著促进PKD1⁻/⁻与PKD2⁻/⁻类器官囊肿扩大,而对照EV仅轻度增大(a–d)。进一步检测cAMP水平发现,托伐普坦10–40 µM在PKD1⁻/⁻和PKD2⁻/⁻中剂量依赖性降低cAMP,最高剂量时差异最显著(e),而EV对照无显著变化。时间序列实验表明,托伐普坦可在24小时起显著抑制囊肿增长,至48–72小时后PKD1⁻/⁻和PKD2⁻/⁻囊肿尺寸与对照差异不再扩大,显示药效随时间趋于稳定(f–h)。相比之下,在iPSC衍生的PKD2基因编辑类器官中,托伐普坦处理并未显著缩小囊肿(i)。结合转录组和已发表数据,研究发现AVPR2受体在tubuloids中表达显著高于 iPSC类器官(j),解释了两种模型对托伐普坦敏感性的差异。整体表明,基因编辑的PKD tubuloids可作为托伐普坦作用机制和药效评估的理想平台。
本研究系统性确立了成人肾tubuloids的CD24⁺起源,提出并验证了4-phase高效培养策略,构建出结构与功能均接近成人肾上皮的体外模型;在疾病建模与药效学方面,PKD1/PKD2-/-tubuloids复现ADPKD囊肿表型并对托伐普坦产生与临床一致的响应,且跨模型转录组对照显示与患者组织在关键通路上的一致性,使其成为更贴近成人肾病理的研究与筛药平台。需要指出的是,该研究在成人肾上皮疾病建模与药物机制验证方面已具里程碑意义。
参考文献:
Xu, Yaoxian et al. “Adult human kidney organoids originate from CD24+ cells and represent an advanced model for adult polycystic kidney disease.” Nature genetics vol. 54,11 (2022): 1690-1701. doi:10.1038/s41588-022-01202-z

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

