
近日,日本东京医科齿科大学医学部附属医院肾脏内科Koichiro Susa与Eisei Sohara团队在Stem Cell Research & Therapy发表重要研究,利用肾类器官技术成功破解了儿童遗传性肾病研究的长期困境。
该研究聚焦于NPHP1缺陷型肾单位硬化症(NPH)——这是最常见的儿童遗传性肾病,却长期缺乏能够再现其关键病理特征的模型。论文明确指出:“现有的Nphp1缺陷小鼠模型均未能表现出纤维化表型”,揭示现有动物模型在模拟该病纤维化表型上的严重不足。因此,建立能够准确模拟疾病病理的模型,成为阐明机制和开发疗法的首要前提。
通过构建NPHP1基因敲除的人源肾类器官模型,研究发现低剂量IL-1β刺激能够稳定再现NPHP1缺陷相关的纤维化表型,包括纤维连接蛋白表达显著增加、胶原蛋白基因上调等特征,成功突破了传统动物模型的局限。
进一步研究发现,NPHP1蛋白直接与Hippo信号通路的核心激酶LATS1/2结合,其缺失导致LATS功能失调,使下游YAP/TAZ转录复合体过度活化,从而驱动纤维化进程。
实验还发现,靶向Hippo通路的抑制剂——包括实验性药物肽段17和已在临床使用的维替泊芬(Verteporfin),能够有效缓解类器官中的纤维化表现。特别是维替泊芬,因其成熟的临床安全性数据,展现出良好的转化潜力。
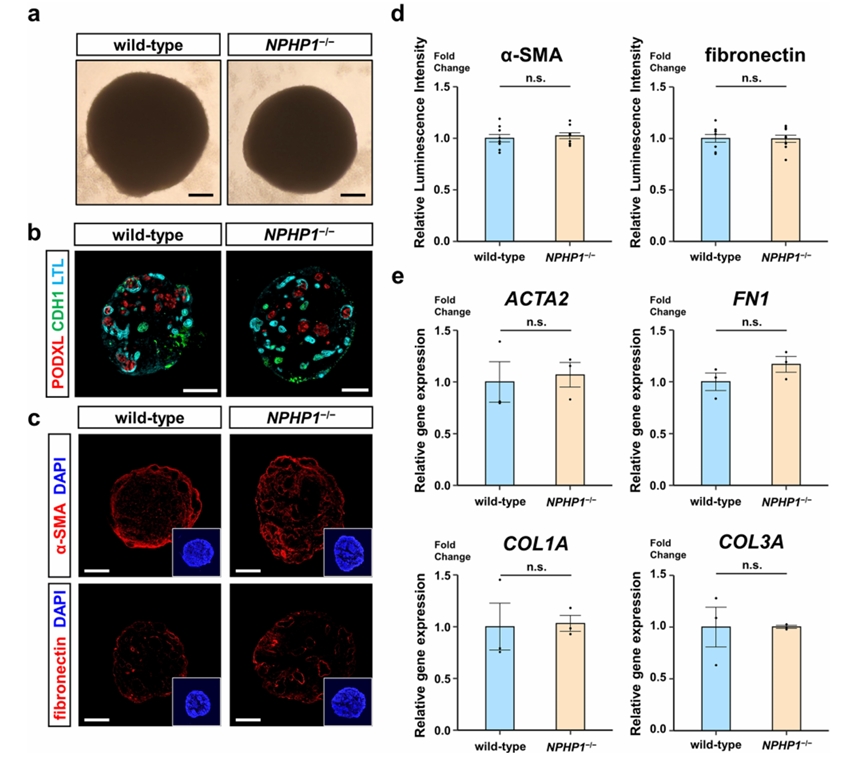
图1. 利用NPHP1基因敲除诱导多能干细胞成功构建的3D肾类器官在未受刺激状态下的基础特征。研究显示,在分化培养28天后,野生型与NPHP1⁻/⁻类器官在肾脏标志物(PODXL、CDH1、LTL)表达、结构形态以及早期纤维化标志物(α-SMA、Fibronectin)的表达水平上均无显著差异,证明基因缺失本身在类器官早期发育阶段并未自发诱导纤维化表型。
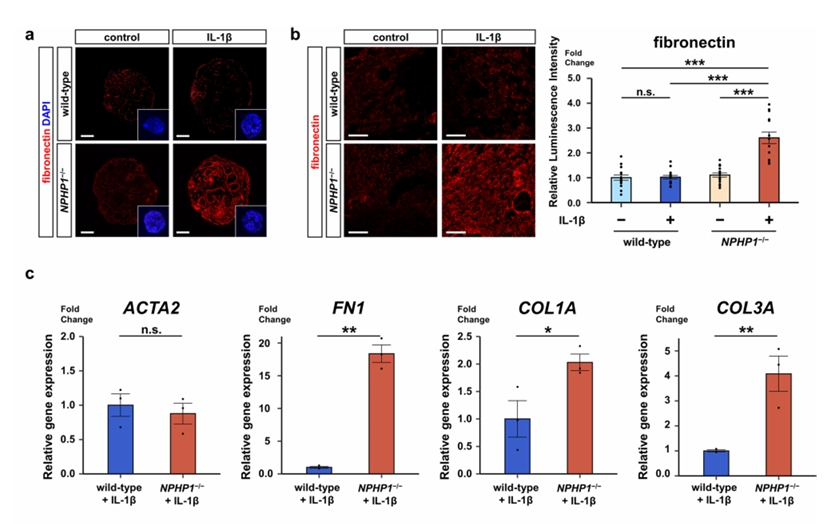
图2. 低剂量IL-1β刺激对肾类器官纤维化的特异性影响:在NPHP1缺陷型类器官中,IL-1β处理能显著诱导纤维连接蛋白表达并上调纤维化相关基因FN1、COL1A、COL3A的转录水平;而野生型类器官在相同处理下未出现明显纤维化反应。该结果提示NPHP1缺失会增强肾组织对炎症刺激的敏感性,从而推动纤维化进程。
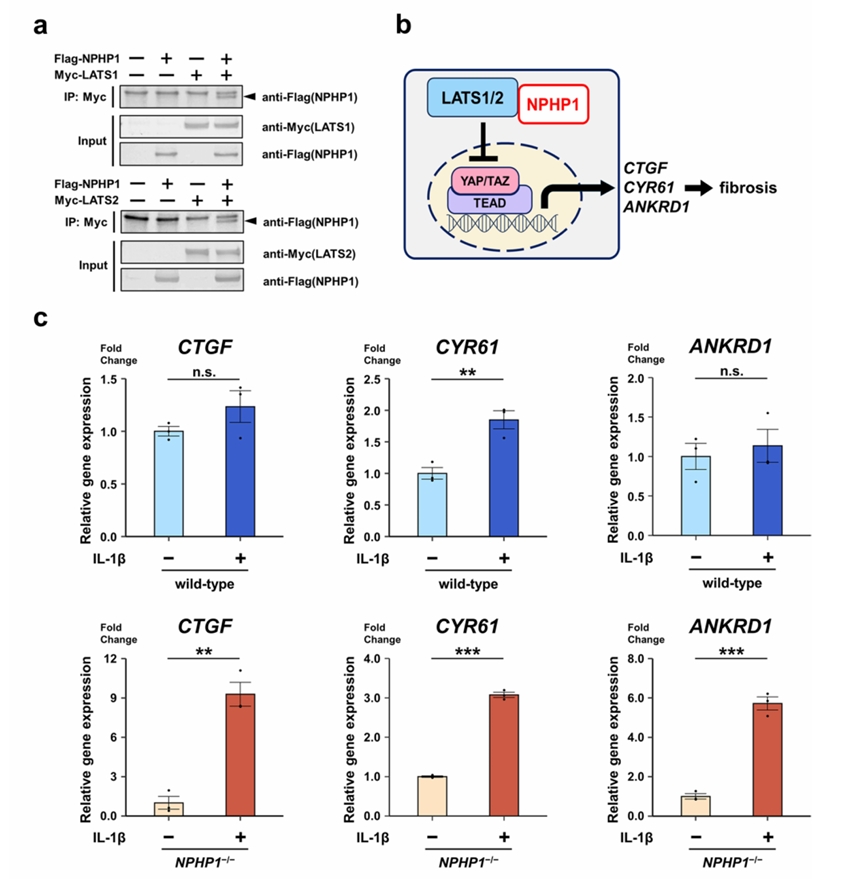
图3. NPHP1与Hippo信号通路的直接相互作用及其在纤维化中的功能:实验证实NPHP1可与Hippo通路核心激酶LATS1/2直接结合;在NPHP1缺陷类器官中,IL-1β刺激特异性上调Hippo下游促纤维化基因CTGF、CYR61和ANKRD1的表达,提示NPHP1缺失可能通过干扰LATS功能导致Hippo通路过度激活,从而驱动纤维化进程。
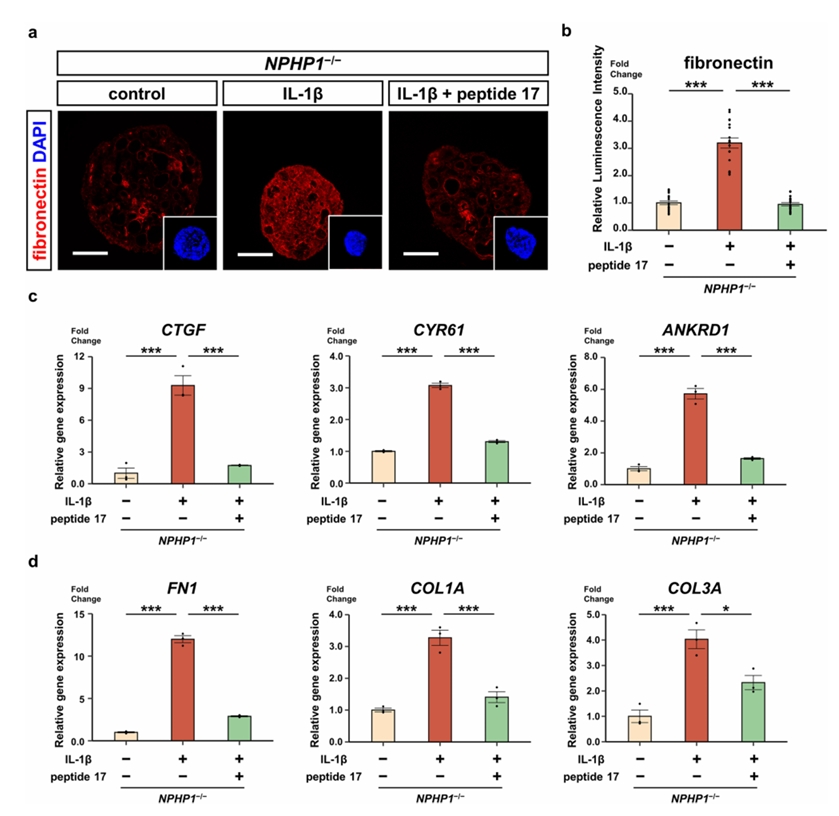
图4. Hippo通路抑制剂对纤维化的治疗潜力:在NPHP1缺陷型肾类器官中,使用肽段17抑制Hippo通路下游的YAP/TAZ-TEAD结合,能够有效逆转IL-1β诱导的纤维化表型,显著降低纤维连接蛋白表达,并下调CTGF、CYR61、ANKRD1及胶原蛋白基因的表达水平。
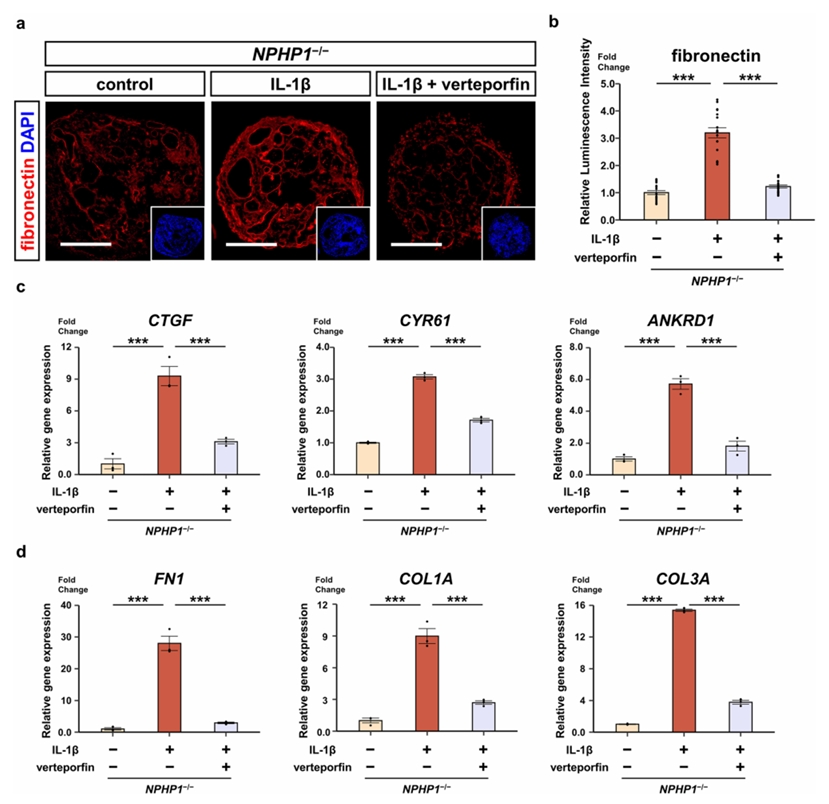
图5. 临床药物维替泊芬(Verteporfin)的治疗效果验证:在NPHP1缺陷型肾类器官中,维替泊芬可显著抑制IL-1β诱导的纤维化,降低纤维连接蛋白表达,并下调Hippo通路下游基因CTGF、CYR61、ANKRD1及纤维化相关基因的表达水平,证明了该已上市药物具有作为NPHP1相关肾病治疗候选药物的潜力。
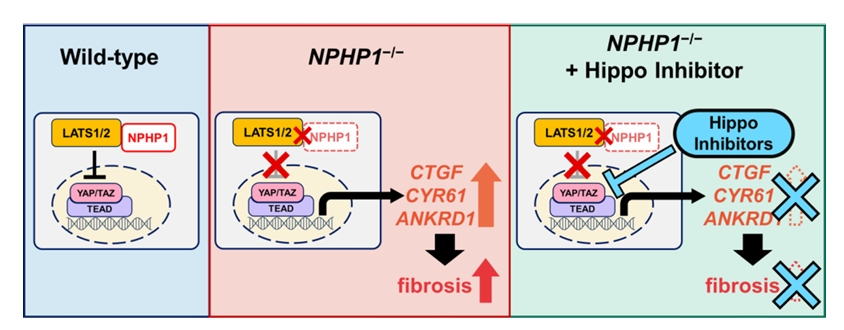
图6. NPHP1缺失导致其与Hippo通路激酶LATS1/2的结合中断,引起YAP/TAZ-TEAD转录复合体过度活化,进而驱动促纤维化基因表达和肾脏纤维化;而Hippo通路抑制剂可通过阻断该信号级联反应,在NPHP1缺失背景下仍能有效抑制纤维化进程。
该研究构建了“NPHP1缺失-Hippo通路激活-纤维化发生”的完整病理调控轴,不仅成功建立了首个能模拟该疾病纤维化表型的有效模型,还为开发靶向Hippo通路的治疗策略提供了理论基础,为儿童遗传性肾病的精准治疗开辟了新方向。
参考文献:
Suzuki, Takefumi et al. "iPSC-based drug discovery identified the Hippo signaling pathway as a therapeutic target in the fibrosis of NPHP1-deficient nephronophthisis." Stem cell research & therapy vol. 16,1 489. 19 Sep. 2025.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

