
在最新发表于 The EMBO Journal 的一篇研究中,以色列 Sheba 医学中心的 Benjamin Dekel 团队主导,联合特拉维夫大学、华盛顿大学以及魏茨曼科学研究所等国际研究机构,成功建立了人类胎肾类器官(hFKOs) 模型,并深入探讨了 Notch 信号在肾单位发育中的作用。研究发现,hFKOs 不仅能够完整再现人类胎肾发育的多样性和发育轨迹,还揭示了 Notch 信号在肾单位近端小管与远端小管分化中的差异作用。这项工作为肾脏发育机制、先天性肾畸形的病理机制研究、肾脏药物筛选和再生医学提供了重要的实验平台。
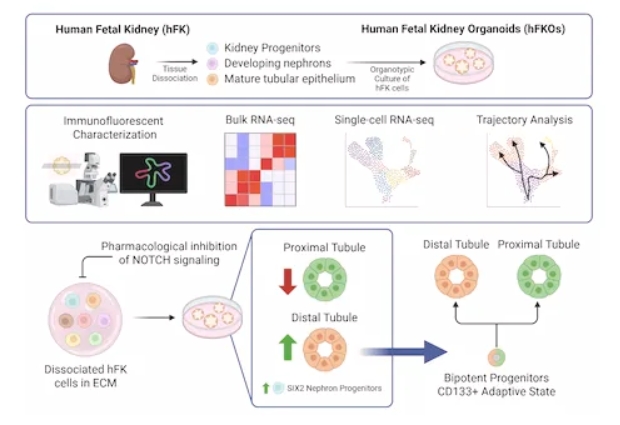
肾脏器官发生异常会导致发育综合征和肾脏病理。本研究建立了一种人胎源性肾脏类器官培养体系,可用于体外探索人类肾脏的早期发育过程。
化学定义的胎肾类器官(hFKOs)能够重现肾单位和输尿管谱系及其细胞层级结构。
hFKOs 在体外培养中可维持肾上皮祖细胞与小管分化长达三个月。
hFKO 组织来源的祖细胞能够逐步成熟,并自组织形成分化的上皮结构。
在 hFKOs 中抑制 Notch 信号,会导致分化受阻并引起祖细胞群体的扩增。
胎肾类器官的建立与功能验证
为了验证胎肾细胞是否能够在体外重建复杂的肾小管结构,本研究的第一步是验证:胎肾细胞能否在体外形成稳定、长期存在的类器官模型。研究者从 15–20 周胎龄的人类胎肾组织出发,将其进行酶解和单细胞化处理,再嵌入基质(BME/Matrigel)并用化学定义的 hNPSR 培养基进行培养。结果显示,类器官在培养 2–3 周后即可自组织形成极化的肾上皮结构,并在超微结构水平上表现出微绒毛、紧密连接和初级纤毛。部分类器官在 Forskolin 处理下发生膨胀,提示其具备正确的水和离子通道功能。这一步骤奠定了后续研究的基础,证明 hFKOs 可以作为可行的体外模型。
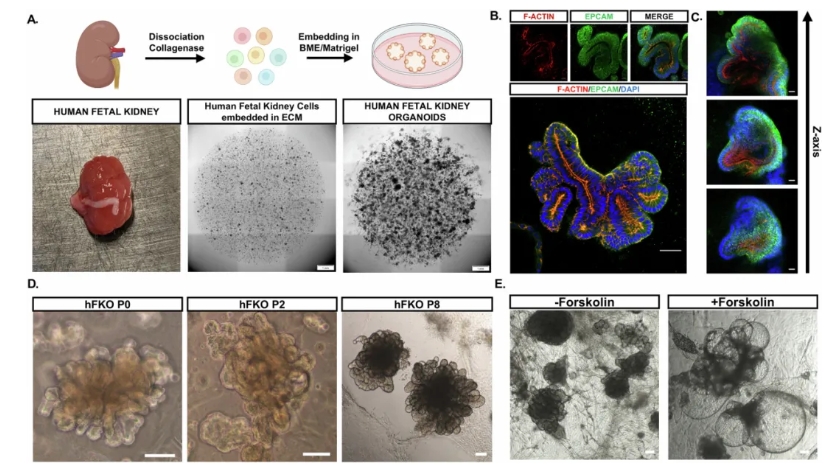
图 1. 胎肾类器官(hFKOs)构建方案
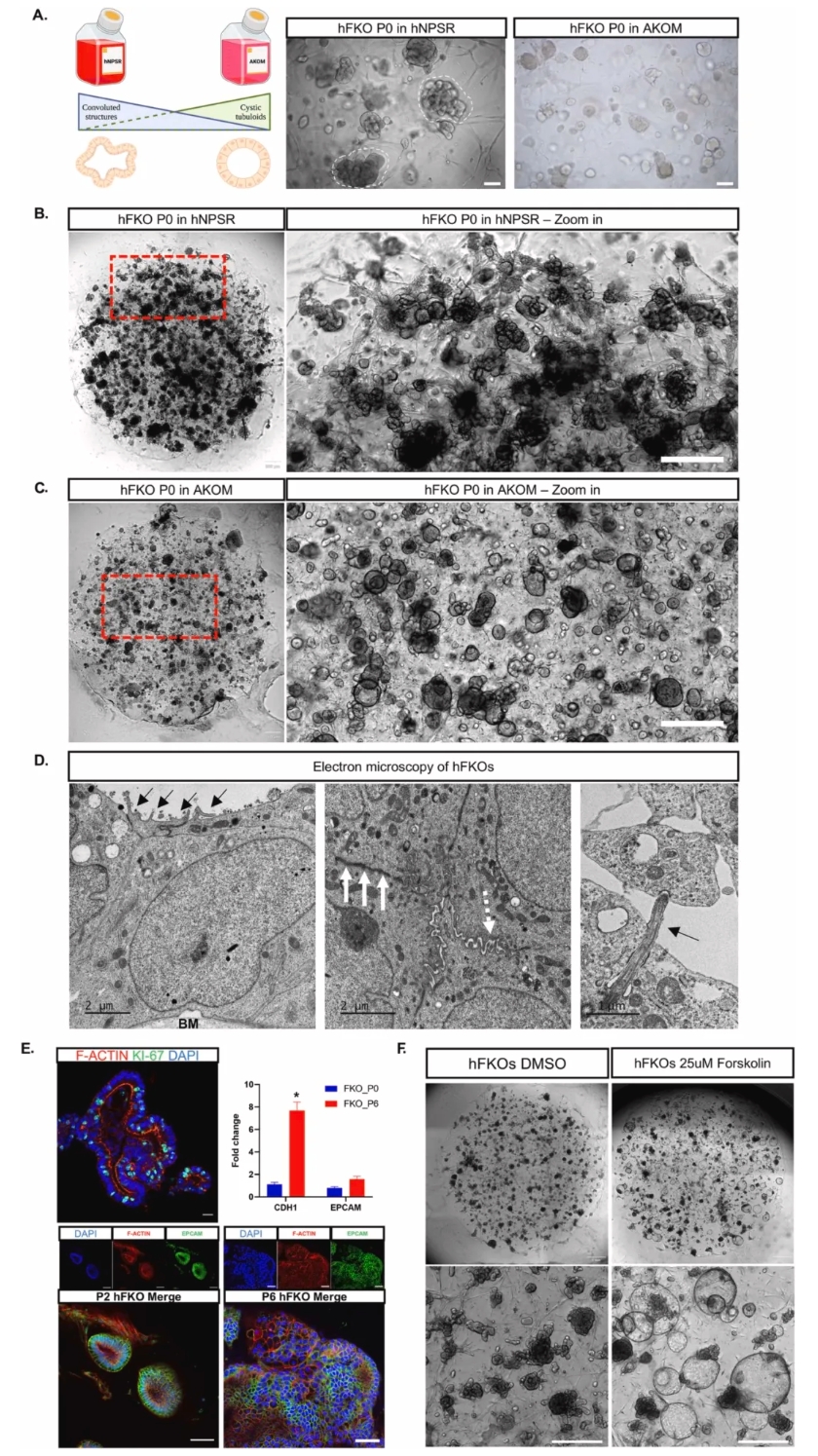
图 EV1. 人胎肾类器官(hFKO)在不同培养基中的表型
验证类器官是否重现胎肾发育层级
在确认了类器官的形态和功能特征后,研究团队进一步探索其是否能保留胎肾的发育层次。通过免疫染色和流式细胞分析,作者发现 hFKOs 内存在 NCAM1⁺/SIX2⁺ 的肾单位祖细胞,表明在hFK中驱动肾发生的干细胞也存在于体外模型,以及 PAX2⁺ 早期上皮、WT1⁺/CDH6⁺ 近端小管、MUC1⁺/ECAD⁺ 远端小管和 GATA3⁺ 连接小管 等多种结构(见补充材料)。同时,类器官周围还观察到 MEIS1⁺ 间质细胞和 CD31⁺ 内皮细胞,进一步增强了其与胎肾组织的相似性。
基于这些结果,作者认为 hFKOs 的确能够在体外重现胎肾中从祖细胞到分化小管的完整发育层级。
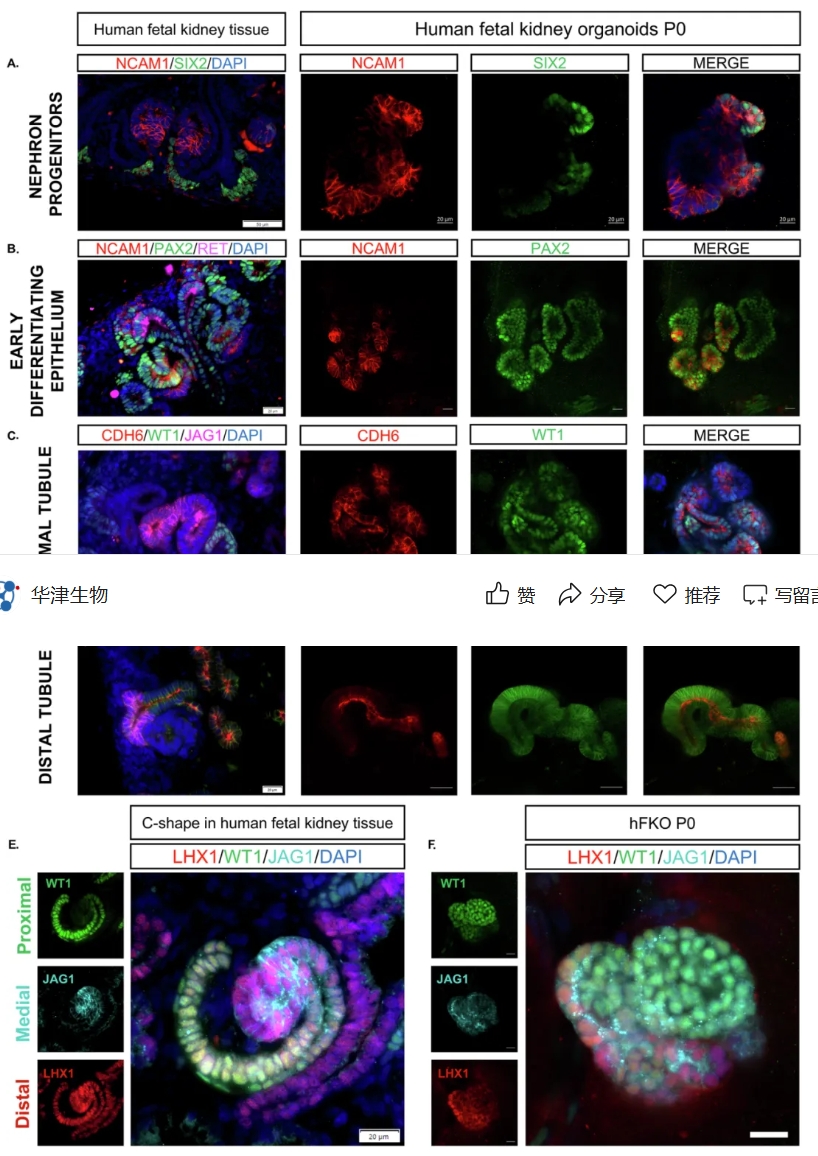
图 2. 保留的胎肾发育层次
转录组分析验证发育动态与祖细胞潜能
在确认类器官能重建发育层级后,作者通过 bulk RNA-seq 对不同代次 hFKOs 进行分析。结果显示:P0 阶段(2–3 周)富集表达 SIX2、PAX2、LHX1、JAG1 等祖细胞和早期发育基因,而 P2 及 P5–P6 阶段则逐渐上调 CDH6、HNF1A、CUBN、MUC1、KRT18、AQP3/2 等成熟小管和集合管标志,呈现出与胎肾类似的发育时间轴。尽管随着培养传代,部分发育基因下调,但 NCAM1⁺/PAX2⁺ 祖细胞和早期小管结构仍可被检测到,提示其持续的发育潜能。进一步,研究者利用磁珠分选(MACS)富集 P2 阶段的 NCAM1⁺ 祖细胞,结果显示仅该群体能够重新生成类器官,并再次形成祖细胞位点及多种小管结构。与 iPSC 来源的类器官比较发现,hFKOs 在早期阶段表达更高的祖细胞和发育基因,且长期培养后仍保留上皮祖细胞标志(如PAX2、CD24、HNF1B、PROM1);相比之下,iPSC 类器官在 3–4 周后停滞,并更倾向于表达足细胞成熟基因(如 MAFB、WT1)。这些结果表明,hFKOs 不仅能模拟人类胎肾的分化动态过程,还提供了一个可长期维持祖细胞群体的体外模型。
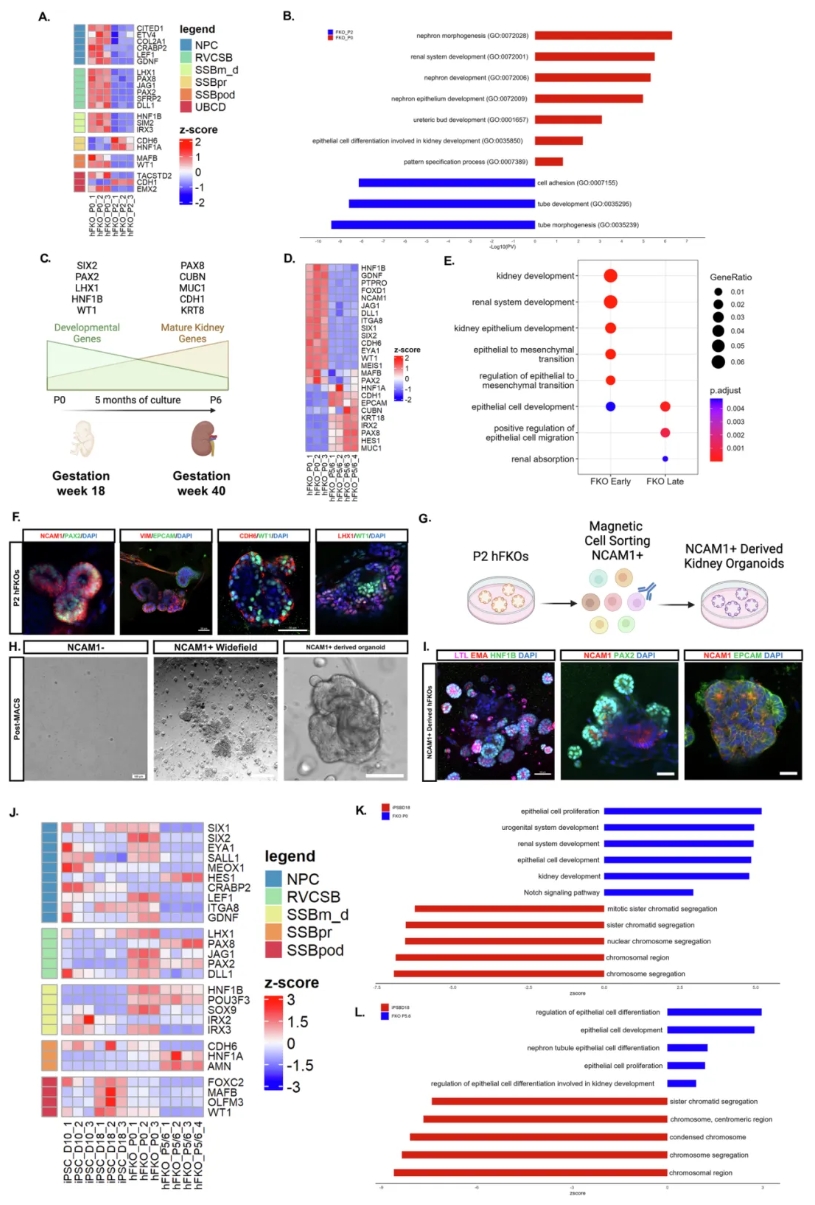
图 3. 对人胎儿肾脏组织(hFKOs)进行的RNA测序显示,其发育过程呈现出与天然胎儿肾脏相似的动态变化特征
单细胞测序与伪时序分析揭示发育轨迹
在 bulk RNA-seq 证明 hFKOs 具有发育动态后,作者进一步通过 scRNA-seq 来解析其复杂的细胞组成与分化路径。将两个健康 hFK (来自妊娠第 15 周和第 20 周)培养 3 周,分别取样,并合并在一起以形成包含 13,368 个细胞的 hFKO 单细胞数据集,共识别出 15 个细胞簇,其中包含 10 个典型的肾单位相关群体,包括 NPCs、肾小泡(RVs)、S 型体(CSBs/SSBs)、早期及成熟足细胞、近端与远端小管、集合管等。进一步的分析发现,NPCs 在 肾小泡阶段发生分支,分别走向 足细胞与近/远端小管谱系,伪时序结果显示这一轨迹与人类及小鼠胎肾的发育过程高度吻合。值得注意的是,类器官在冻存后仍能维持这些细胞类型和轨迹,且与胎肾组织和 iPSC 类器官的公开数据比较时,hFKOs 在 早期肾单位细胞和足细胞群体 上更接近胎肾。综合来看,hFKOs 在单细胞和时间维度上均忠实再现了胎肾的 发育层次和分化动力学。
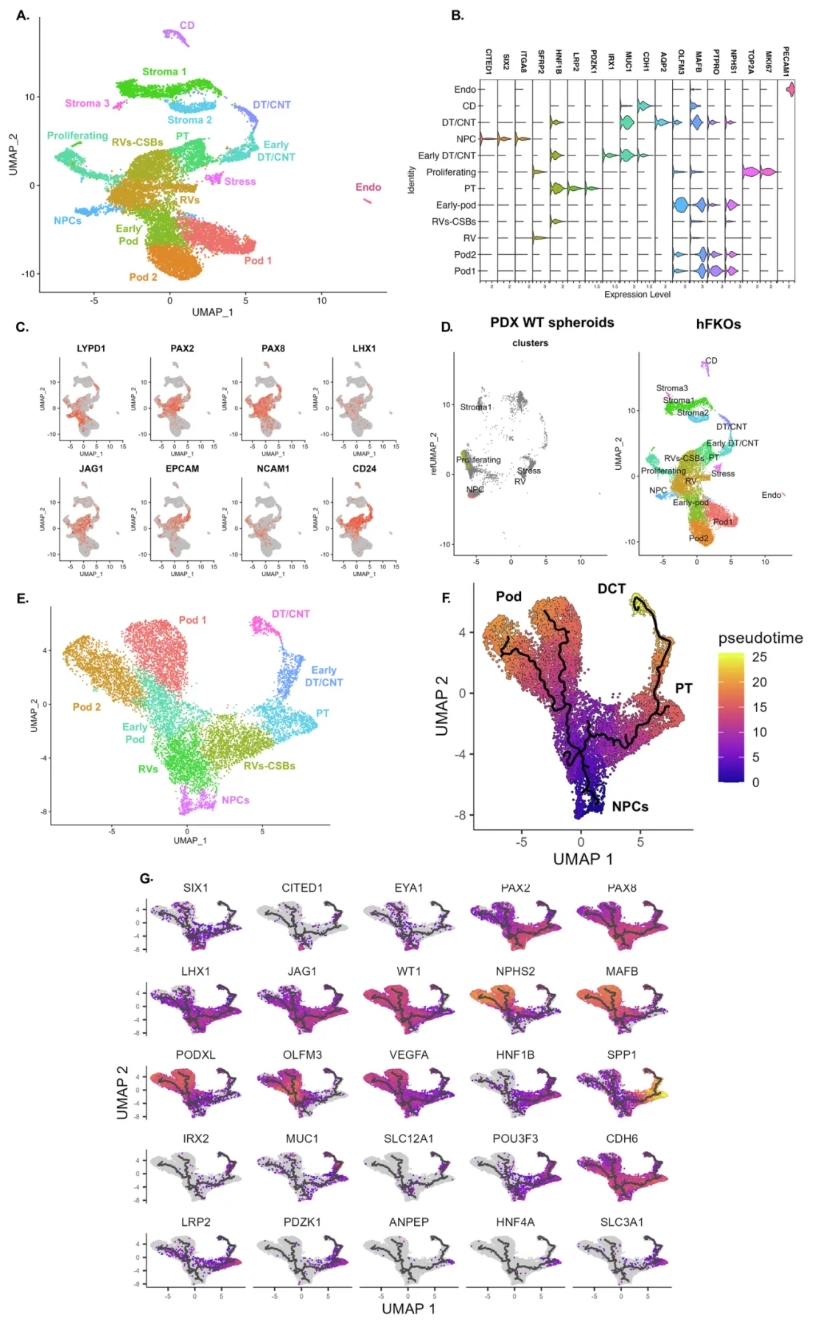
图 4. hFKO的单细胞RNA测序揭示其发育过程与天然胎儿肾脏相似
Notch 信号在近端与远端小管分化中的差异作用
在前述转录组学与单细胞分析确认 hFKOs 保留发育轨迹后,研究团队进一步利用该模型探究 Notch 信号在肾单位分化中的功能。由于 hFKOs 显示出 Notch 通路基因的显著富集,研究者采用 γ-分泌酶抑制剂 DAPT 阻断 Notch 信号。结果表明,Notch 抑制导致类器官整体增殖能力下降,早期祖细胞(SIX2⁺)被维持在未分化状态,无法正常越过前小管聚集体(PTA)阶段。在形态学上,CDH6⁺/LTL⁺ 的近端小管结构明显减少并出现了萎缩,而远端小管(EMA⁺/ECAD⁺)的结构基本保留,在伪时序分析中甚至表现出更成熟的分化趋势。同时,Notch 抑制条件下出现了异常的多阳性小管结构(EMA⁺/ECAD⁺/LTL⁺),这表明分段过程受到干扰。进一步的单细胞分析显示,DAPT 处理后 NPC 和增殖细胞比例上升,并出现了包含近端和远端早期标志物的双潜能前体簇,其中 PROM1 与 ALDH1A1 表达上调,并可向近端与远端两类谱系分化。这些结果整体支持:Notch 信号在近端小管和足细胞的正常分化中起关键作用,而远端小管的发育对 Notch 抑制不敏感,甚至在一定程度上表现出成熟增强。
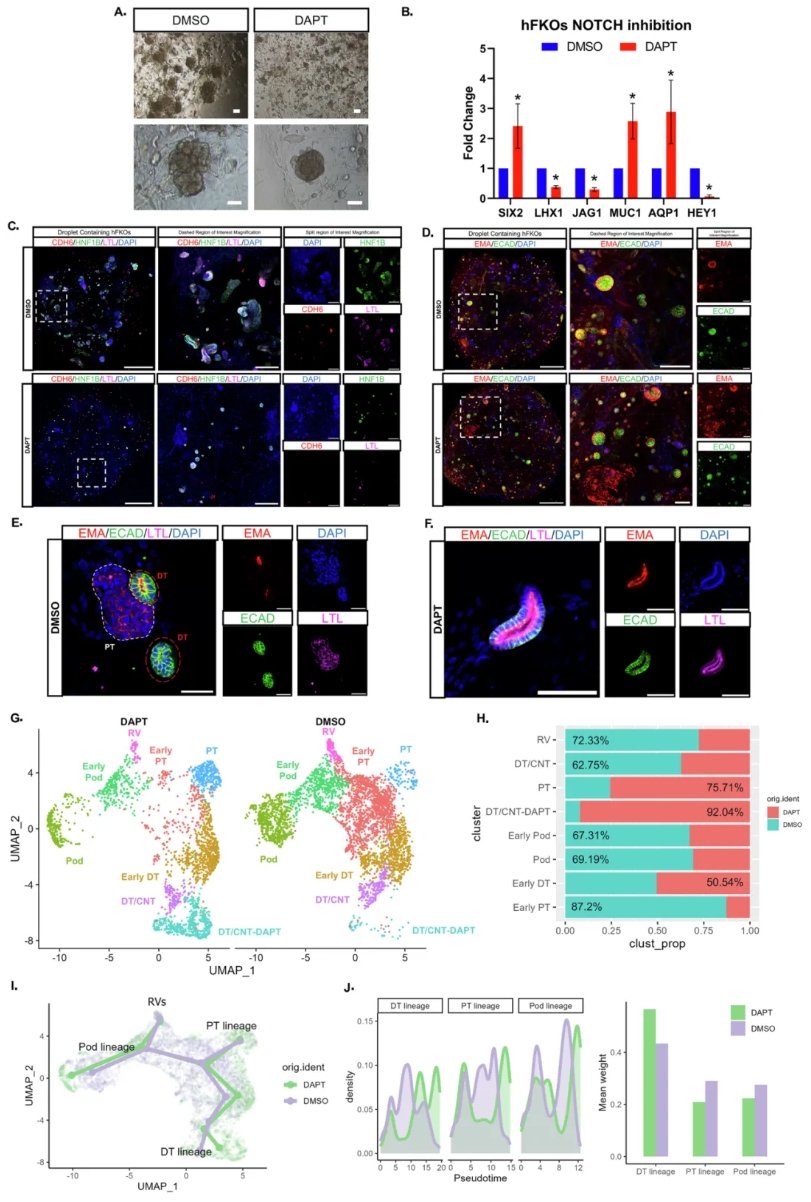
图 5. 在hFKOs敲除Notch基因的细胞中,近端小管谱系分化受到抑制
总结
Dekel团队建立了一个化学定义的,无血清的方案来分化胎肾类器官(hFKOs),该模型能在体外长期维持,并在形态、细胞组成和分子水平上高度还原人类胎肾发育的层次与轨迹。通过对 Notch 信号通路的系统研究,作者发现 Notch 对近端小管和足细胞分化至关重要,而远端小管在 Notch 抑制下仍能分化并表现成熟。同时,研究发现了新的双潜能前体细胞状态,提示可能存在补偿性机制。该模型为研究先天性肾发育异常(如 Alagille 综合征) 及探索药物筛选与再生医学应用提供了坚实基础,尽管目前仍存在如免疫染色验证受限、原代细胞操作难度大等不足,作者认为该模型为肾脏发育与再生医学研究打开了新的方向。
参考文献:
Namestnikov M, Cohen-Zontag O, Omer D, Gnatek Y, Goldberg S, Vincent T, Singh S, Shiber Y, Rafaeli Yehudai T, Volkov H, Folkman Genet D, Urbach A, Polak-Charcon S, Grinberg I, Pode-Shakked N, Weisz B, Vaknin Z, Freedman BS, Dekel B. Human fetal kidney organoids model early human nephrogenesis and Notch-driven cell fate. EMBO J. 2025 Jul 21. doi: 10.1038/s44318-025-00504-2. Epub ahead of print. PMID: 40691416.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

