
今年8月,微生物与酶工程领域权威期刊 Enzyme and Microbial Technology 在线发表了题为 “Effect of lipopolysaccharide on ganglioside expression in human induced pluripotent stem cell-derived kidney organoids” 的研究论文。该研究团队利用人源 iPSC 构建肾类器官,并通过脂多糖(LPS)处理建立脓毒症相关急性肾损伤(SA-AKI)模型,系统分析了炎症反应与神经节苷脂代谢之间的联系。
结果发现,LPS 不仅引发炎症因子和氧化应激显著上调,同时导致 GM3、GM2、GD3 和 GD1a 等神经节苷脂及其合成酶显著下调,提示神经节苷脂在炎症调控和 SA-AKI 发病机制中可能发挥关键作用。
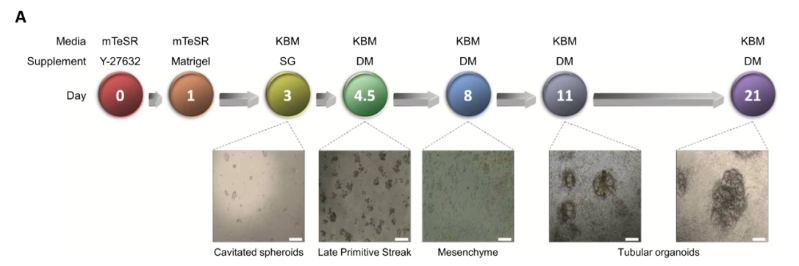
图1. 分化protocol(点击图片查看大图)
炎症损伤建模:利用人源 iPSC 构建 3D 肾类器官,并通过 LPS 处理成功建立脓毒症相关急性肾损伤(SA-AKI)模型,表现为肾脏标志物下调、损伤和间充质标志物上调。
炎症与应激反应:LPS 处理后,肾类器官中促炎因子(IL-1β、IL-6、IL-8)和氧化/硝化应激分子(iNOS、COX-2)显著升高,伴随 ROS 增加和线粒体膜电位下降。
信号通路激活:实验证据表明 LPS 主要通过 TLR4/MyD88/NF-κB 及 p38 MAPK 通路介导炎症反应,成功再现 SA-AKI 的核心分子机制。
神经节苷脂下调:首次发现 LPS 处理会导致 GM3、GM2、GD3、GD1a 等神经节苷脂及其合成相关基因/蛋白显著下调,提示神经节苷脂在炎症和肾损伤发病机制中的关键调控作用。
模型应用价值:证明人类肾类器官可作为研究肾损伤和炎症反应的重要体外模型,并为探索新型炎症调控靶点和药物干预提供实验基础。
背景与目的
急性肾损伤(AKI)是常见且严重的临床问题,其中脓毒症相关 AKI(SA-AKI)最为常见,主要机制涉及炎症和氧化应激。但目前缺乏理想的体外模型来研究其发生机制。神经节苷脂是细胞膜的重要成分,已知可调控炎症信号,但其在肾损伤中的作用仍不明确。本研究利用人iPSC 衍生的肾类器官,通过 LPS 处理建立 SA-AKI 模型,旨在分析炎症与应激反应,并探索 神经节苷脂在其中的表达变化和潜在作用。
研究方法
类器官生成:利用人源 iPSC 在三维诱导分化体系中培养,形成 3D 肾类器官,包含足细胞、肾小管、内皮等多种细胞类型。
LPS 处理:在类器官成熟(Day 21)时加入 10 μg/mL LPS,处理 24 小时,用于建立脓毒症相关急性肾损伤(SA-AKI)模型。
炎症与应激检测:通过 qPCR、Western blot、免疫荧光检测肾标志物(NEPHRIN、PODXL、HNF4α、GATA3、CD31)、损伤标志物(KIM1、VIM)及炎症因子(IL-1β、IL-6、IL-8)、应激分子(iNOS、COX-2),并测定 ROS 水平和线粒体膜电位。
神经节苷脂分析:采用有机溶剂萃取结合 HPTLC 薄层层析检测 GM3、GM2、GD3、GD1a 水平,同时结合 qPCR、Western blot 和免疫荧光分析合成相关基因(ST3GAL5、ST8SIA1、β4GALNT1、ST3GAL2)的表达。
结果
类器官构建成功:iPSC 经分化形成含足细胞、肾小管、内皮和间充质等多种细胞类型的 3D 肾类器官,肾特异性标志物逐步上调,而多能性标志物逐渐下降。
LPS 诱导炎症与损伤:LPS 处理后,足细胞、近端小管、输尿管芽及内皮标志物(NEPHRIN、PODXL、HNF4α、GATA3、CD31)显著下降,肾损伤标志物 KIM1 和间充质标志物 VIM 明显上调。
炎症因子和应激分子升高:IL-1β、IL-6、IL-8 等炎症因子表达升高;iNOS、COX-2 等氧化/硝化应激分子水平增加;ROS 生成增强,线粒体膜电位明显下降。
神经节苷脂下调:HPTLC 显示 GM3、GM2、GD3、GD1a 水平显著下降;qPCR 和 Western blot 显示 ST3GAL5、ST8SIA1、β4GALNT1、ST3GAL2 等合成相关基因和蛋白均下调;免疫荧光验证信号减弱。
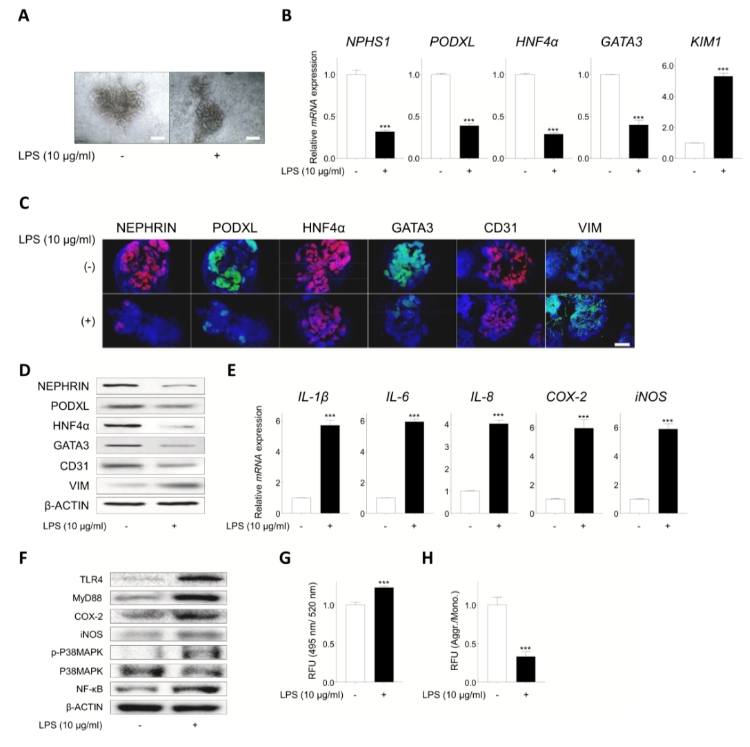
图2. LPS 降低了肾脏标志物的表达,并在 iPSC 衍生的肾类器官中诱导了炎症反应(点击图片查看大图)
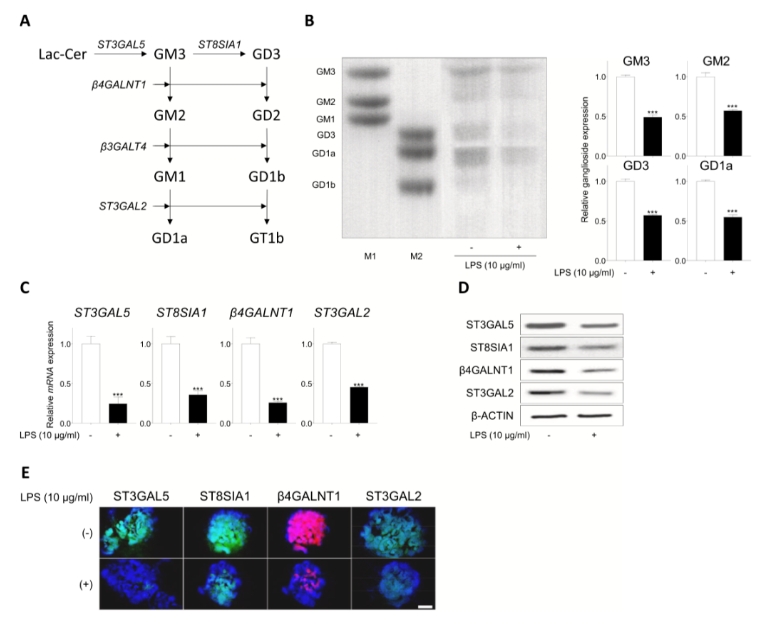
图3. 脂多糖刺激下人诱导多能干细胞衍生的类肾器官中神经节苷脂表达的变化(点击图片查看大图)
结论
研究团队利用人源 iPSC 构建肾类器官,并通过 LPS 处理建立了脓毒症相关急性肾损伤(SA-AKI)模型。结果发现,LPS 不仅引起肾类器官中典型的炎症反应、氧化应激和线粒体功能障碍,还显著降低了肾脏特异性标志物的表达。更为关键的是,研究首次揭示神经节苷脂(GM3、GM2、GD3、GD1a)及其合成酶的水平在 LPS 刺激下显著下调,提示神经节苷脂可能在炎症调控和 SA-AKI 发病机制中发挥重要作用。
总结
本研究通过“LPS 处理人 iPSC 衍生肾类器官建立脓毒症相关急性肾损伤模型”的方式,系统评估了炎症反应、氧化应激和线粒体功能变化,并首次揭示 LPS 会导致多种神经节苷脂及其合成酶显著下调。研究结果表明,肾类器官是研究 SA-AKI 机制的重要体外工具,同时提示神经节苷脂可能成为未来炎症干预和肾损伤治疗的新靶点。
参考文献:
Ryu J, Kim J, Lee H, et al. Effect of lipopolysaccharide on ganglioside expression in human induced pluripotent stem cell-derived kidney organoids. Enzyme and Microbial Technology. 2025;191:110730. doi:10.1016/j.enzmictec.2025.110730

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

