
肾纤维化是慢性肾病进展和终末期肾功能衰竭的重要病理机制。而间充质干细胞(MSC)在抗炎与抗纤维化方面展现潜力,但由于其体内存留时间短、体积较大阻碍肺毛细血管通行,限制了临床应用。荷兰鹿特丹伊拉斯姆斯医学中心 Li 教授团队提出新的思路:从 MSC 膜制备纳米颗粒(membrane particles, MP),探索其在小鼠 IRI 模型与人源肾类器官中的抗纤维化效果。研究成果发表于 Stem Cell Research & Therapy(2025)。
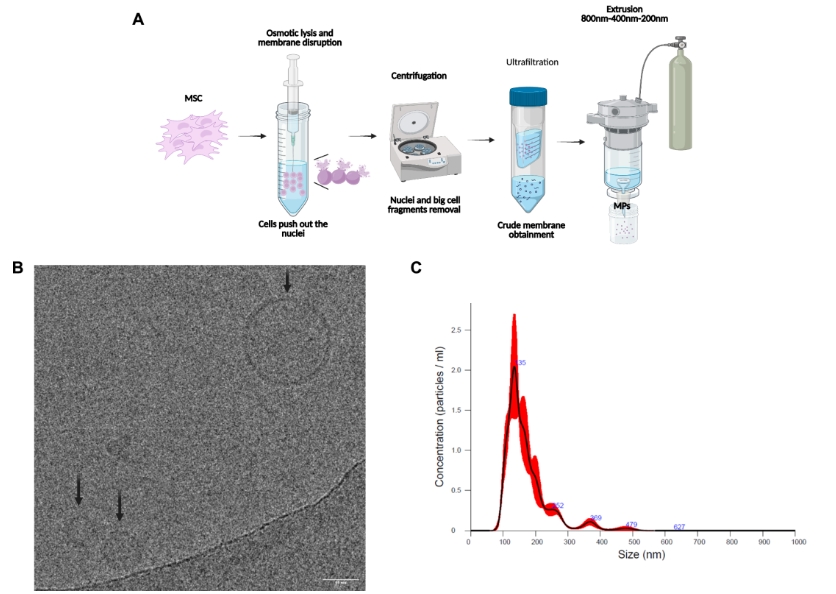
图1. MSC 膜颗粒的制备与表征A:MP 制备流程示意图;B:冷冻电镜显示 MP 呈球形并具脂质双层(箭头所示);C:纳米颗粒追踪分析结果,展示 MP 的粒径分布与浓度。
- MSC 膜颗粒制备成功:MP 直径约 134.5 nm,具备稳定的脂质双层结构。
- 直接抗纤维化作用:显著下调 TGF-β、FN1、PAI1 等 ECM 基因,减轻胶原沉积。
- 作用靶点明确:MP 主要抑制成纤维细胞活化,对肾小管上皮细胞影响不显著。
- 肾脏类器官验证:在人源 iPSC 肾类器官中同样抑制纤维化,提示临床转化潜力。
研究团队首先建立并表征了 MSC 膜颗粒(MP),确认其具备稳定的球形结构和均一的纳米级粒径。在小鼠 IRI 模型中,检测结果显示 MP 并未显著改变巨噬细胞、T 细胞及 Tregs 等免疫细胞比例,提示其作用机制并非依赖免疫调节。进一步分析发现,MP 能够显著下调 TGF-β 及 FN1、PAI1 等纤维化相关基因的表达,减少胶原沉积和 ECM 积聚,从而有效抑制纤维化进程。体外实验进一步明确,MP 的主要作用靶点为肾成纤维细胞,其能够抑制成纤维细胞的增殖和 ECM 合成,而对肾小管上皮细胞影响不大。整体而言,MP 通过直接调控成纤维细胞活化发挥抗纤维化作用,而非依赖免疫细胞的改变。
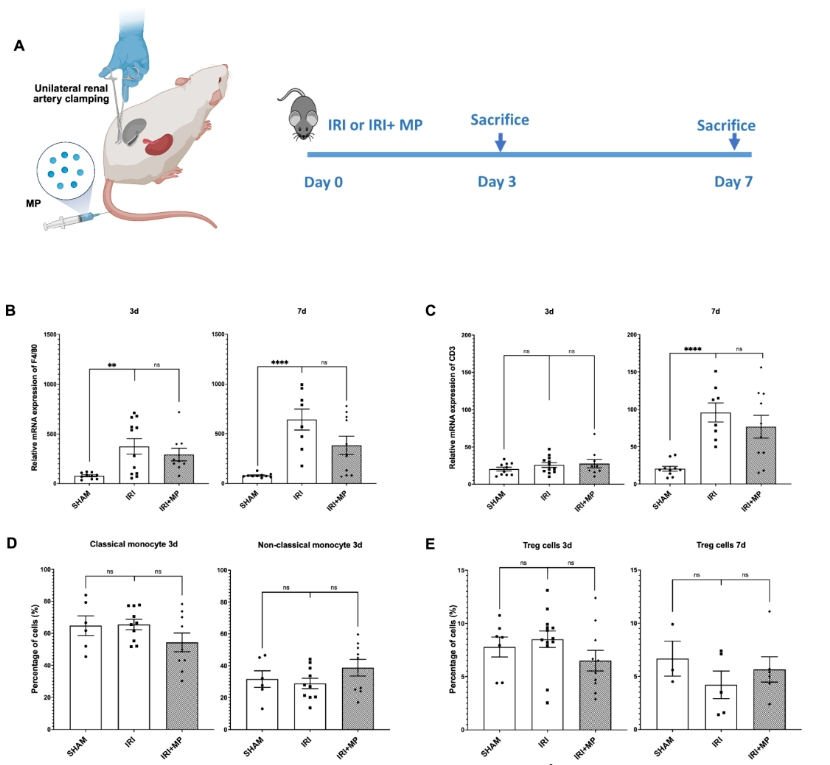
图2. MP 对 IRI 肾脏及血液中单核细胞、巨噬细胞和 T 细胞无显著影响A:小鼠 IRI 模型建立及 MP 给药流程示意图;B–C:IRI 后 3 天和 7 天肾脏中巨噬细胞标志物 F4/80 与 T 细胞标志物 CD3 的基因表达分析;D:IRI 后 3 天外周血中经典与非经典单核细胞比例(流式细胞术);E:不同时间点外周血中 Treg 细胞比例。结果均以均值±SEM 表示,符号代表单个样本数据。MP 处理组与 IRI 对照组间差异不显著(ns)。
肾脏类器官验证
而比较有趣的是,为进一步评估跨物种应用潜力,研究团队利用 iPSC 分化的人类肾类器官,在低氧与 IL-1β 条件下诱导纤维化。结果显示,纤维化类器官出现 ECM 积聚和纤维化基因上调,而 MP 干预显著抑制这些变化,改善了类器官的结构与功能。这一部分结果表明,MP 在人类系统中同样有效,具备向临床转化的潜力。
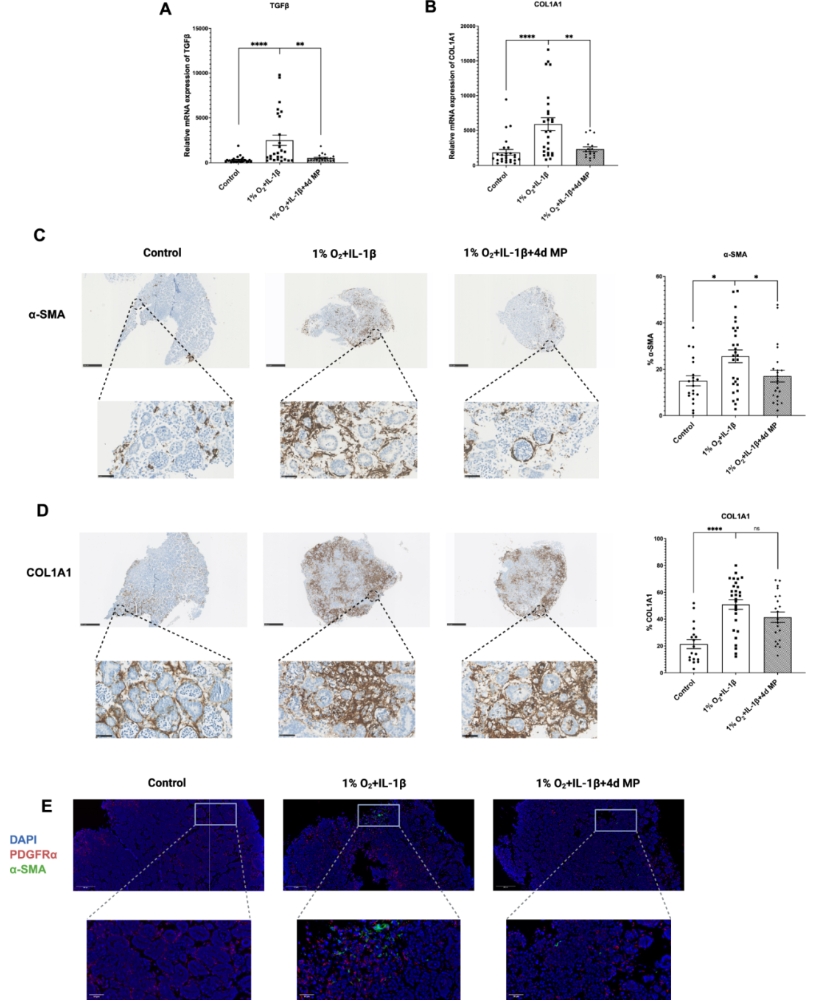
图5. MP 抑制肾类器官纤维化A–B:对照组、纤维化组(1% O₂+IL-1β)及纤维化+MP 处理组在第 4 天的 TGF-β 与 COL1A1 基因表达分析;C–D:免疫组化检测及 Qupath 定量分析显示 COL1A1 与 α-SMA 表达差异,并附放大视图;E:免疫荧光结果显示各组中PDGFRα 与 α-SMA 的表达情况。结果提示 MP 能显著抑制类器官纤维化相关标志物的上调。
总结
Li 等团队的研究建立并表征了 MSC 衍生膜颗粒(MP),并在小鼠 IRI 模型中验证了其抗纤维化作用。结果显示,MP 并未显著改变巨噬细胞、T 细胞及 Tregs 等免疫细胞比例,而是通过抑制成纤维细胞活化,下调 TGF-β、FN1、PAI1 等纤维化相关基因表达,减少 ECM 沉积,从而有效缓解肾脏纤维化。进一步的人源 iPSC 肾类器官实验表明,MP 能在体外纤维化模型中显著降低 TGF-β、COL1A1 等标志物的上调,抑制 α-SMA 与 COL1A1 的沉积,并改善类器官结构。这一结果证明了 MP 的抗纤维化效应在人类系统中同样存在,强调了类器官在机制验证和临床转化研究中的重要作用。
参考文献:
Li S, Merino A, Korevaar S, van den Bosch TPP, Baan CC, Reinders MEJ, Hoogduijn MJ. Mesenchymal stromal cell-derived membrane particles suppress kidney fibrosis. Stem Cell Res Ther. 2025 Jul 26;16(1):405. doi: 10.1186/s13287-025-04522-z. PMID: 40713899; PMCID: PMC12297600.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

