
常染色体显性多囊肾病(ADPKD)是最常见的遗传性肾脏疾病,由 PKD1 或 PKD2 基因突变引起。突变导致肾小管上皮细胞功能异常,囊肿逐渐累积并扩张,最终损害肾功能。据统计,ADPKD可占到终末期肾病(ESRD)病例的约10%。尽管过去几十年研究取得了显著进展,但现有治疗(如托伐普坦)只能部分延缓疾病进展,仍无法彻底逆转病程。传统动物模型的临床转化效果有限,因此亟需更贴近人类的疾病模型,以深化对机制的理解并推动新疗法的开发。
本综述系统阐述了ADPKD的遗传学基础(如“两击假说”和部分细胞突变模式)、关键分子机制(包括cAMP信号、G蛋白调控、mTOR通路、Wnt通路以及液体分泌异常)、当前药物治疗的进展与局限(如生长抑素类似物、mTOR抑制剂、β3受体阻滞剂、AMPK 激活剂等),并重点探讨了多能干细胞(PSCs)衍生肾类器官在模拟疾病发生、解析异常信号通路(如代谢紊乱和炎症反应)以及药物筛选中的作用。已有多项研究利用这些类器官成功再现囊肿形成过程,为未来的临床转化提供了宝贵洞见。
综述还评估了现有类器官模型的不足(如缺乏间质纤维化、血管成分和免疫细胞),并提出了优化方向,例如引入间质祖细胞、免疫细胞共培养以及改进长期培养体系,以更真实地再现人类 ADPKD 的复杂微环境,从而推动个性化治疗的探索。
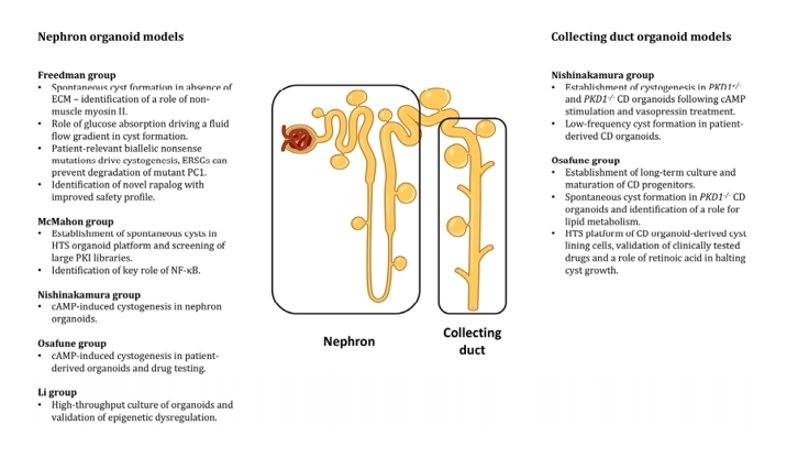
图1.概述目前已应用于ADPKD研究的hPSC衍生的肾单位和集合管类器官模型。肾脏类器官越来越多地用于再现人类囊肿发生和重要的疾病过程,以及鉴定候选药物。
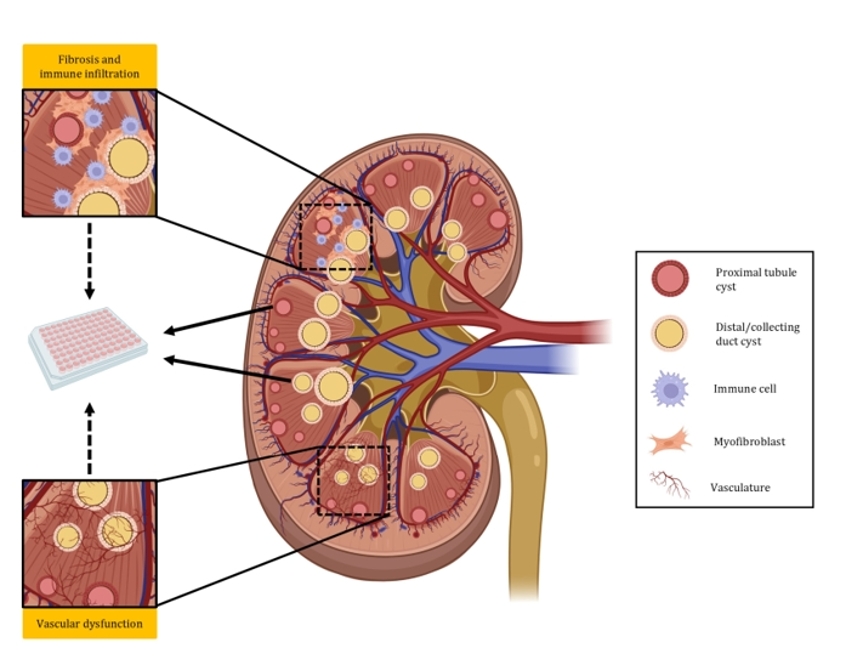
图2. ADPKD的主要病理特征和体外建模. hPSC衍生的肾脏类器官已被广泛用于研究ADPKD;然而,到目前为止,仅概述了近端和远端小管/集合管中的囊肿形成。为了更好地了解人ADPKD,hPSC衍生的肾脏类器官应用于研究纤维化、免疫细胞浸润和血管功能障碍,因为它们是在疾病进展中起重要作用的关键特征。
创新点
深入解析 ADPKD 的遗传机制,强调“两击假说”在细胞层面的作用,以及部分细胞突变在疾病进展中的重要影响。
评估现有药物治疗的局限性,并介绍了新兴靶点(如 mTOR 抑制剂、β3-肾上腺素受体阻滞剂、前列腺素 E2 受体调控、AMPK 激活剂)的潜在价值。
详述胚胎肾脏发育过程及多能干细胞分化为肾组织的方法,重点介绍肾单位类器官与集合管类器官在模拟囊肿形成中的应用。
总结现有肾类器官在囊肿机制研究、药物高通量筛选和自动化平台中的优势,并揭示了新发现(如葡萄糖吸收促进囊肿生长、脂质代谢异常)。
指出现有模型的局限(如纤维化、炎症、血管功能缺失),并提出改进策略,包括引入间质、免疫和血管成分,以及优化培养体系,以提升类器官的生理相似性和临床转化潜力。

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

