
今年2月,生物医学工程领域权威期刊 Nature Biomedical Engineering发表了题为 “Evolving adeno-associated viruses for gene transfer to the kidney via cross-species cycling of capsid libraries” 的研究论文。该研究通过跨物种循环进化AAV capsid库,开发出新型AAV变体AAV.k13和AAV.k20,这些变体在小鼠、猪、非人灵长类动物模型及人类肾类器官中均表现出显著的肾脏转导效率提升,尤其对近端小管具有选择性亲和力。该研究通过人类肾类器官模型,模拟真实肾脏环境,用于进化筛选和转导验证,揭示了变体在人类肾组织中的潜力。
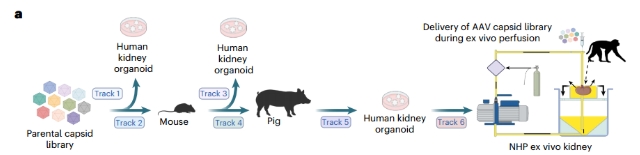
实验方法
跨物种进化策略:结合小鼠、猪、非人灵长类肾脏及人类肾类器官的多模型循环,筛选出高效肾靶向AAV变体,AAV.k20在人类肾类器官中的转导效率较AAV9提高12倍。
人类肾类器官应用:从iPSC生成3D肾类器官,用于体外进化循环和转导测试,揭示变体在近端肾小管上皮细胞的优先转导,支持肾脏疾病基因递送的优化。
多路径递送兼容:静脉注射、尿管和动脉递送均有效,尤其尿管路径在猪和非人灵长类模型中实现高效肾脏基因表达,支持单链和自互补载体基因组。
临床潜力:变体在猪肾移植模型中表现出广泛转导,支持免疫调节基因如PD-L1的表达,适用于肾脏疾病和移植基因治疗。
文献解读
背景与目的
慢性肾脏病影响全球8-16%人口,许多疾病如囊性肾病具有遗传基础,但基因递送到肾脏的挑战限制了治疗进展。本研究旨在通过多模型跨物种进化AAV capsid库,筛选肾靶向变体,并通过人类肾类器官模拟人类肾环境,评估变体在进化筛选和转导机制中的表现。
研究方法
动物实验:小鼠和猪静脉注射capsid库,非人灵长类肾脏体外机灌注。
检测指标:NGS分析富集序列、荧光成像、qPCR、荧光素酶活性、IHC染色。
体外验证:生成3D人类肾类器官(从iPSC在悬浮中分化,表达干细胞标志物如NANOG、OCT4和分化标志物如CUBN、HNF4A),用于进化库(体外感染循环富集变体)和转导实验(Day 14以1×10¹¹或1×10¹² vg转导AAV变体,5天后评估mCherry荧光、mRNA水平、荧光素酶活性、病毒基因组摄取,以及LTL标记的近端小管定位)。
结果
肾脏富集:变体在人类肾类器官中富集,AAV.k20在进化轨道中达20,000倍富集。
转导表现:人类肾类器官转导显示mCherry主要定位于LTL+近端小管,荧光强度提高12倍,mRNA和荧光素酶水平升高。
机制验证:人类肾类器官测试证实变体优于AAV9和AAV5,支持单链和自互补载体;TH1细胞(近端小管上皮)验证进一步强化。
类器官应用:人类肾类器官提供人类特异选择压力,经预进化后显示独特序列富集,揭示Arg残基偏好,并作为关键模型评估变体在人类肾环境中的转导机制和细胞特异性。
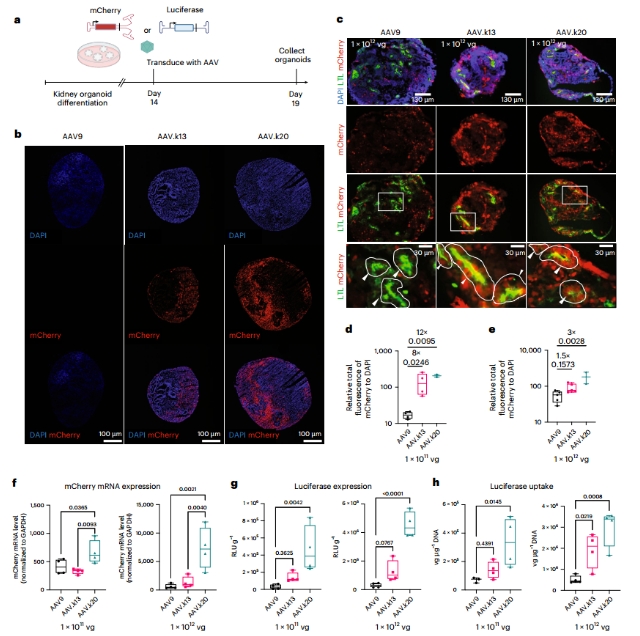
图3. AAV.K13和AAV.K20比AAV9更有效地转导人肾类器官
结论
新型AAV变体通过跨物种进化实现高效肾靶向转导,人类肾类器官在体外进化循环中施加人类相关选择压力,并在转导测试中揭示近端小管机制。该模型支持肾脏基因治疗载体开发,应关注其在疾病模拟中的潜力。
总结
这项研究通过“跨物种进化—肾靶向AAV变体—高效转导”的方式,并结合人类肾类器官的生成和应用,揭示了变体在模拟人类肾环境中的筛选和验证价值,并提示肾脏基因治疗新工具。未来需进一步评估变体在肾类器官疾病模型中的长期应用。
参考文献:
Rosales A, Blondel LO, Hull J, et al. Evolving adeno-associated viruses for gene transfer to the kidney via cross-species cycling of capsid libraries. Nature Biomedical Engineering. 2025;9(7):1086-1100. doi:10.1038/s41551-024-01341-0

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

