编者按:
2026年3月12日是第21个世界肾脏日。全球约有8.5亿人患有各类肾脏疾病,而器官捐献的缺口仍在持续扩大。如何在体外构建功能性肾脏组织,一直是再生医学的核心挑战。本文基于近期发表于《Nature Biotechnology》(IF 41.7)的综述,梳理肾脏发育的基本原理与高阶肾脏类器官的构建策略,带读者了解这一领域的前沿进展。

干细胞来源的肾脏组织为未来肾脏替代治疗带来希望,但由于结果变异性大、细胞类型不全、功能成熟度不足以及难以规模化生产,其临床转化仍面临挑战。解决这些问题需要借鉴胚胎肾脏的自然发育策略。
近期发表于Nature Biotechnology的综述《Developmentally inspired synthetic kidney engineering》系统梳理了该领域的科学进展与技术路径,提出“发育工程学”策略——通过模拟体内发育的时空信号,在体外引导细胞自组织形成复杂结构,为构建高阶肾脏类器官提供了新思路。
肾脏由三类祖细胞协同发育而来:肾单位祖细胞(形成肾单位)、输尿管芽(形成集合管)和间质祖细胞(形成支持组织)。现有类器官虽能重现部分肾脏结构,但过度依赖细胞自组织,无法实现体内发育的多项功能。发育工程学通过设定精确的初始条件和边界条件,引导细胞完成超越自组织的复杂构建。
01
肾脏发育原理
1.1
三类祖细胞谱系
肾脏发育起源于中间中胚层,其前部形成输尿管芽,后部形成肾单位祖细胞和间质祖细胞,这三类祖细胞谱系共同驱动肾脏器官发生。其中,肾单位祖细胞经历凝聚、间充质-上皮转化、极化、分段等过程,最终分化为远端小管、髓袢、近端小管、足细胞和肾小球。(图1d)
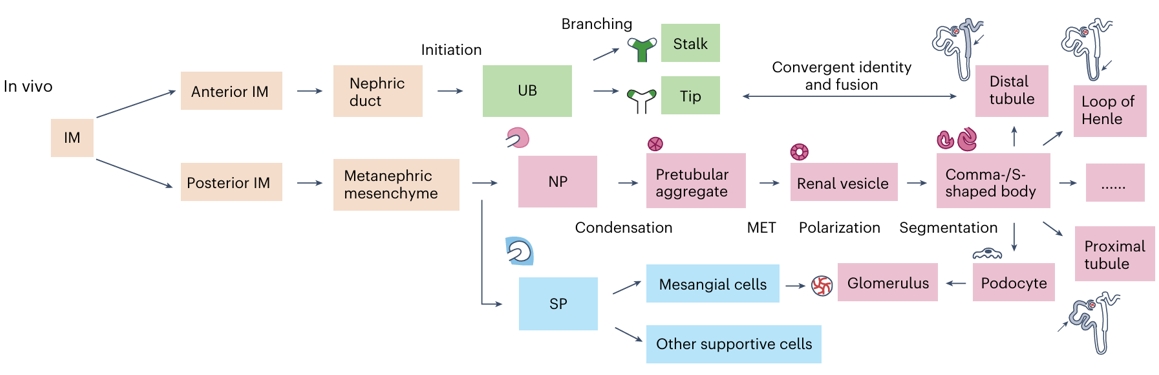
图1d(点击图片可放大)
肾脏谱系图以中间中胚层(IM,intermediate mesoderm)为起点,分为前部中间中胚层(Anterior IM)和后部中间中胚层(Posterior IM)。
前部中间中胚层形成肾管(Nephric duct),随后通过起始(Initiation)形成输尿管芽(UB),输尿管芽经过分支(Branching)分为柄(Stalk)和尖(Tip),最终与远端小管(Distal tubule)发生身份趋同与融合(Convergent identity and fusion)。
后部中间中胚层形成后肾间充质(Metanephric mesenchyme),进而分化为肾单位祖细胞(NP)和间质祖细胞(SP)。
肾单位祖细胞经过凝聚(Condensation)形成前小管聚集(Pretubular aggregate),随后通过间充质-上皮转化(MET,mesenchymal-to-epithelial transition)形成肾小囊(Renal vesicle),再经过极化(Polarization)、分段(Segmentation)形成逗号/S型小体(Comma-/S shaped body),最终分化为远端小管(Distal tubule)、髓袢(Loop of Henle)、近端小管(Proximal tubule)、足细胞(Podocyte)和肾小球(Glomerulus)。
间质祖细胞一部分分化为系膜细胞(Mesangial cells)参与肾小球构成,另一部分分化为其他支持细胞(Other supportive cells)。
1.2
肾源性生态位
输尿管芽末端的肾源性生态位是肾单位诞生的微环境。在这一生态位中,间质、肾单位祖细胞和输尿管芽通过FAT4、维甲酸、Wnt9b、GDNF、RET等信号通路相互调控。(图1a)
肾单位发育依次经过前小管聚集、肾小囊(伴随间充质-上皮转化)、逗号小体、S型小体,最终形成毛细血管襻期肾单位。(图1a)
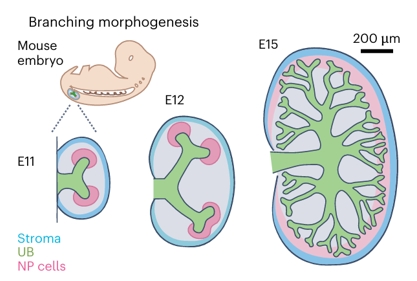
图1a (1)(点击图片可放大)
小鼠胚胎肾脏发育过程中,输尿管芽(UB)发生分支形态发生(Branching morphogenesis),并伴随迁移性肾单位祖细胞生态位(Traveling NP niches),图中标注了E11、E12和E15三个胚胎发育时间点。
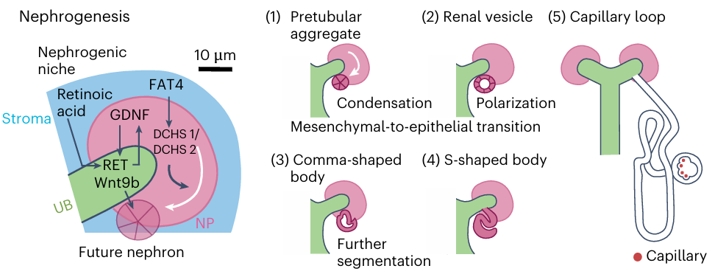
图1a (2)(点击图片可放大)
肾源性生态位(Nephrogenic niche)由间质(Stroma)、肾单位祖细胞(NP)和输尿管芽(UB)构成,三者通过FAT4、DCHS1/DCHS2、维甲酸(Retinoic acid)、Wnt9b、GDNF和RET等信号通路相互调控,其中肾单位祖细胞将形成未来的肾单位(Future nephron)。
肾单位发育从肾单位祖细胞开始,依次经历前小管聚集(Pretubular aggregate)过程中的凝聚(Condensation)、肾小囊(Renal vesicle)阶段的极化(Polarization)并伴随间充质-上皮转化(Mesenchymal-to-epithelial transition)、逗号小体(Comma-shaped body)阶段的进一步分段(Further segmentation)、S型小体(S-shaped body),最终形成毛细血管襻期肾单位(Capillary loop stage nephron)。
1.3
分支与并行化
输尿管芽通过反复分支实现并行化发育:在每个末端创建新的生态位,肾单位祖细胞在其中依次形成新肾单位。
这一分支与并行化机制使得集合管与肾单位能够同步生成,多个肾单位同时发育,并形成皮髓质分区。(图1c)
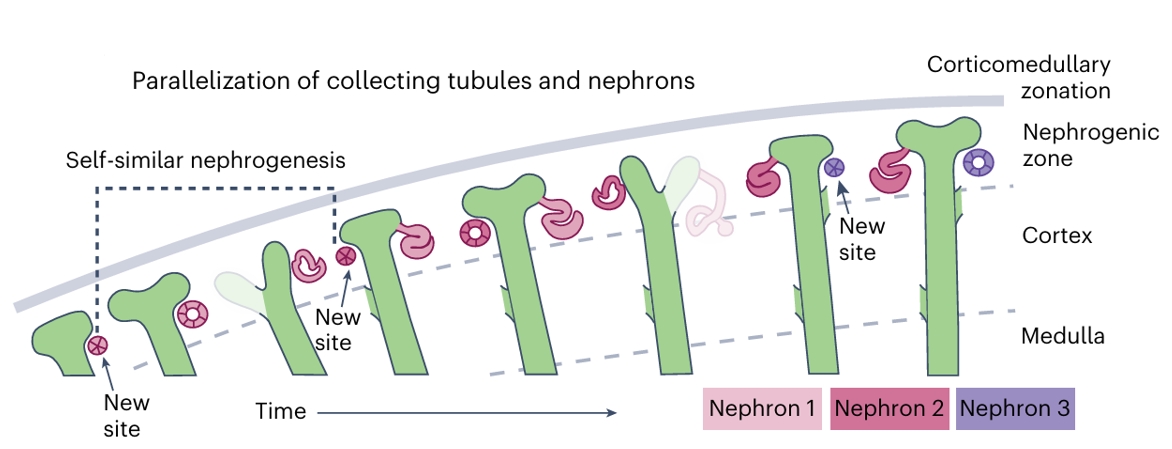
图1c(点击图片可放大)
自我相似分支与肾单位形成过程通过在每个生态位创建新的位点(New site),实现多轮肾单位形成,这一机制体现了集合管与肾单位的并行化(Parallelization of collecting tubules and nephrons)以及自我相似的肾发生过程(Self-similar nephrogenesis)。
随着时间推移(Time),依次形成肾单位1(Nephron 1)、肾单位2(Nephron 2)和肾单位3(Nephron 3),并呈现出皮髓质分区(Corticomedullary zonation),包括肾源性区(Nephrogenic zone)、皮质(Cortex)和髓质(Medulla)。
成熟肾单位由近端小管、髓袢、远端小管构成,最终连接至集合管。(图1b)
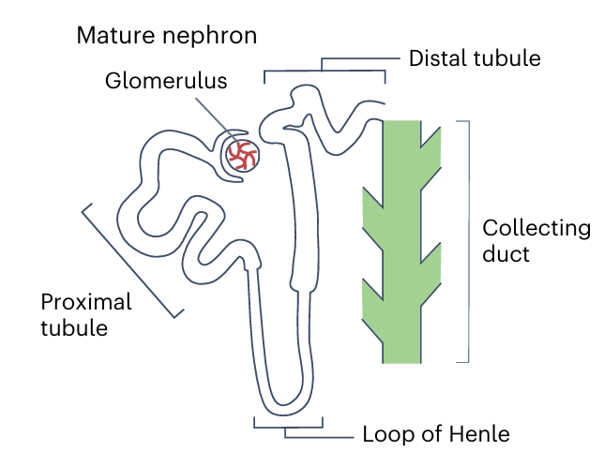
图1b(点击图片可放大)
成熟且分段的肾单位(Mature nephron)包含血管化的肾小球(Glomerulus),由近端小管(Proximal tubule)、髓袢(Loop of Henle)、远端小管(Distal tubule)等多个功能分段构成,最终连接至集合管(Collecting duct)。
02
现有肾脏类器官模型
各谱系的代表性类器官研究可归纳如下(图1e):
输尿管芽谱系中,Mae等建立了可重复分支的输尿管芽类器官;Howden等将远端肾小管诱导为输尿管芽尖和柄;Zeng等培育出重现集合管系统的类器官;Shi等开发了输尿管芽和集合管的定向分化方案。
肾单位祖细胞谱系方面,Taguchi等从多能干细胞中生成了复杂的肾脏结构;Takasato等构建了可自我组织的肾脏类器官及多谱系肾单位类器官;Morizane等利用肾单位类器官模拟肾脏发育与损伤过程;Freedman等应用CRISPR基因编辑技术构建类器官进行疾病建模。
嵌合体类器官(含小鼠间质祖细胞谱系)研究中,Taguchi和Nishinakamura成功培育出具有高阶结构的肾脏类器官;Uchimura等提升了集合管的成熟度;Tsujimoto等建立了模块化分化系统;Tanigawa等通过整合间质细胞生成了器官型结构;Shi等通过融合远端肾单位与输尿管芽,实现了收集系统的整合。

图1e(点击图片可放大)
针对肾脏各主要谱系已发表的类器官模型汇总
03
高阶肾脏类器官构建
3.1
发育工程学的核心概念
发育工程学的核心概念围绕发育基序的循环调控展开:自组织驱动形态建成,形态建成受细胞输入调控,细胞输入决定谱系与生物物理特性,后者反馈调节自组织(图2a)
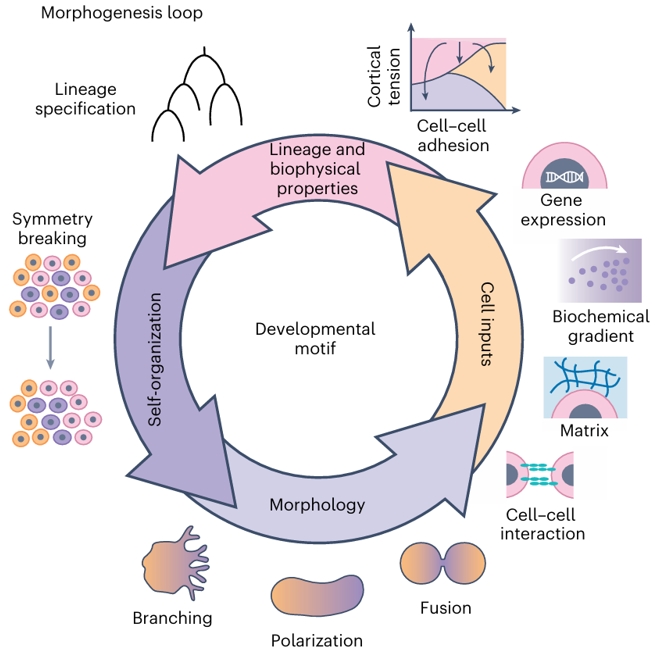
图2a(点击图片可放大)
形态发生环路(Morphogenesis loop)呈现了发育基序(Developmental motif)中四个关键要素的循环调控逻辑:自我组织(Self-organization)(包含对称性破缺)驱动形态建成(Morphology)(包含分支、极化、融合),形态建成受细胞输入(Cell inputs)(包含细胞间相互作用、基质、生化梯度、基因表达)调控,细胞输入进而决定细胞的谱系与生物物理特性(Lineage and biophysical properties)(由细胞间粘附和皮层张力共同决定谱系特化),而谱系与生物物理特性最终又反馈调节自我组织,从而形成闭环。
基于这一核心概念,发育工程学策略将体外组织的初始条件精确设定在发育“临界点”,利用目标基序内的自组织完成结构构建——肾脏发育即包含输尿管芽形成、肾单位祖细胞生态位建立、肾单位发育等连续基序。(图2b)
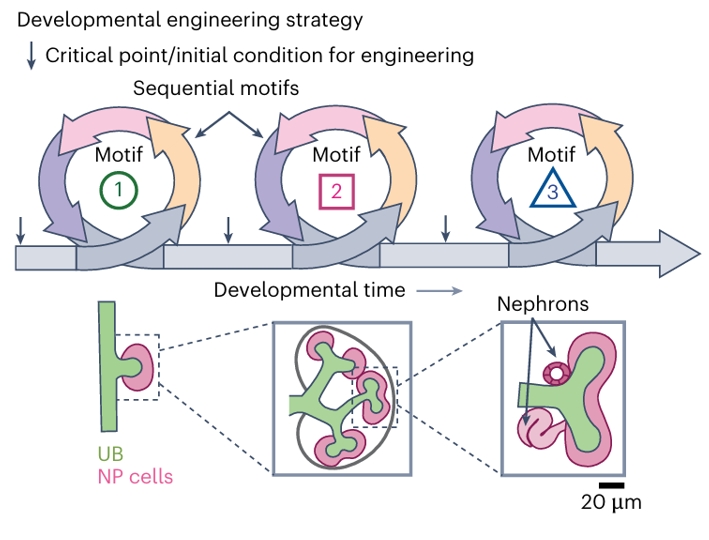
图2b (点击图片可放大)
发育工程学策略(Developmental engineering strategy)的核心在于将体外组织的初始条件靶向设定在临界点(Critical point/initial condition for engineering),利用目标基序内的自我组织来构建结构。
以肾脏发育为例,沿发育时间(Developmental time)顺序发生多个连续基序(Sequential motifs),包括基序1(Motif 1)、基序2(Motif 2)和基序3(Motif 3),分别对应输尿管芽(UB)、肾单位祖细胞(NP cells)和肾单位(Nephrons)的形成过程。
进一步延伸,“菊花链”策略允许不同基序不按顺序直接组装,通过DNA编程组装、生物打印等技术构建高阶功能性组织结构,并在生物反应器中实现规模放大。(图2c)
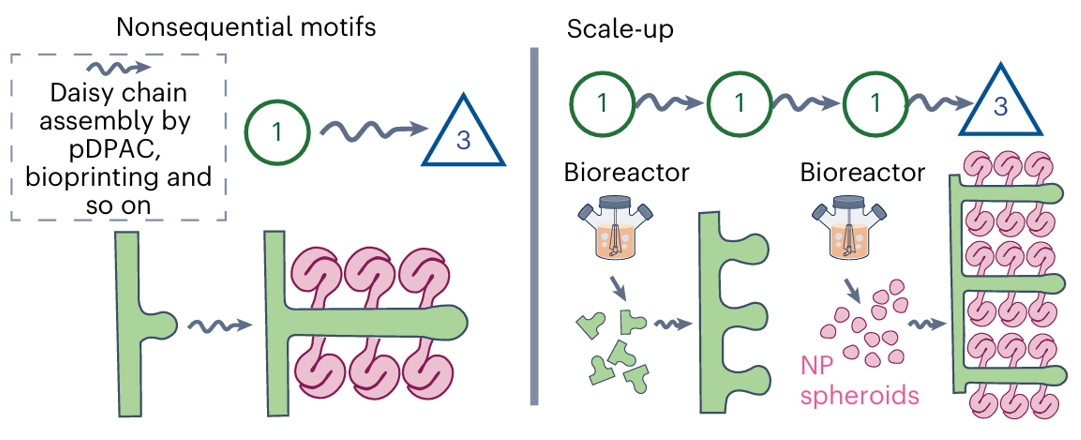
图2c(点击图片可放大)
“菊花链”策略(Daisy chain strategy)通过直接组装将不同发育基序构建的结构组合起来。
基序不必按顺序发生(Nonsequential motifs),例如可直接从基序1连接至基序3(1→3)。组装方式包括pDPAC(光刻DNA编程细胞组装技术)、生物打印(bioprinting)等。
通过这种非顺序性组装,可以构建高阶功能性组织结构(higher-order functional tissue structures),这些结构不一定与体内组织方式完全相同。
在规模放大(Scale-up)过程中,可采用多个基序1与基序3的组合(1→1→1→3)进行逐步整合,后续步骤可涉及生物反应器(Bioreactor)培养,例如将肾单位祖细胞球(NP spheroids)作为组件进行组装。
3.2
初始条件控制
通过DNA编程技术精确调控输尿管芽与肾单位祖细胞的接种比例,实现对初始条件的控制,进而影响类器官大小、谱系组成及肾单位节段比例(远端与近端)。(图3b)
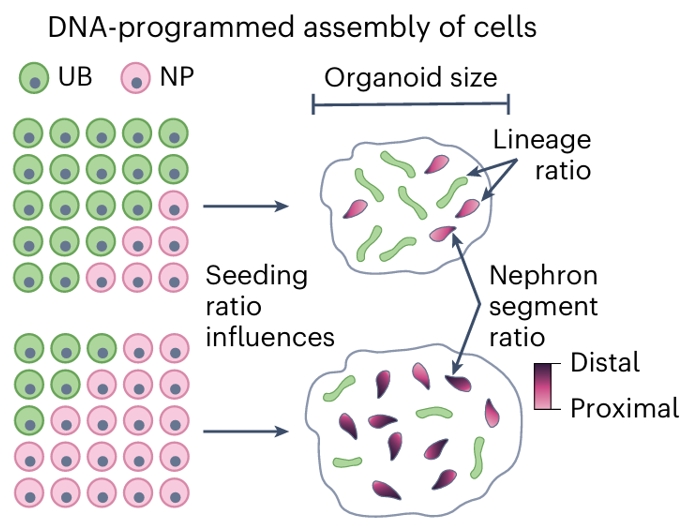
图3b(点击图片可放大)
通过嵌合体干细胞来源类器官中的初始细胞比例(initial cell ratio),可以实现对谱系组成和肾单位分段(Controlled lineage composition and nephron segmentation)的调控。
利用DNA编程的细胞组装(DNA-programmed assembly of cells)技术,精确控制输尿管芽(UB)和肾单位祖细胞(NP)的接种比例(Seeding ratio),进而影响类器官大小(Organoid size)、谱系比例(Lineage ratio)以及肾单位节段比例(Nephron segment ratio),包括远端(Distal)和近端(Proximal)分段。
3.3
生物打印与自组织尺度匹配
在生物打印过程中,细胞固有的自组织长度尺度常覆盖预设的打印尺度,导致实际结构偏离设计,这一挑战凸显了生物打印与自组织尺度匹配的重要性。(图3c)
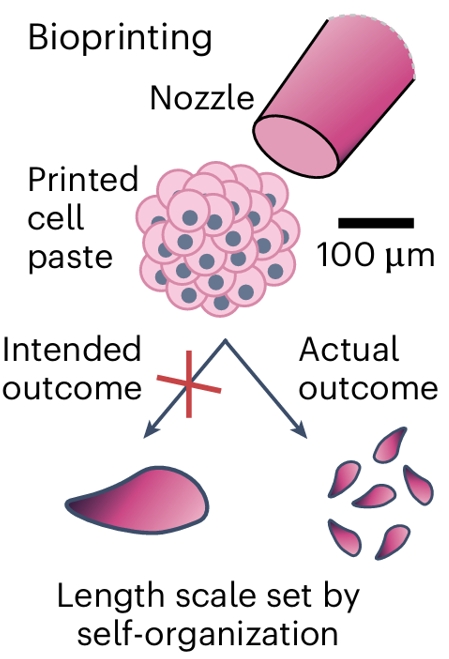
图3c(点击图片可放大)
在生物打印(Bioprinting)过程中,通过打印喷嘴(Nozzle)挤出细胞糊剂(Printed cell paste)进行图案化。
尽管预设了预期的打印结果(Intended outcome),但由于细胞内在的自组织长度尺度(Length scale set by self-organization)的调控,实际结果(Actual outcome)会覆盖预设的图案化长度尺度,导致最终形成的结构不同于原始设计。
为解决这一问题,“动态形态”方法先用DNA“魔术贴”将细胞精确图案化,再嵌入基质凝胶,利用细胞驱动的全局应变引导自组织形成极化的肾小管网络。(图3d)
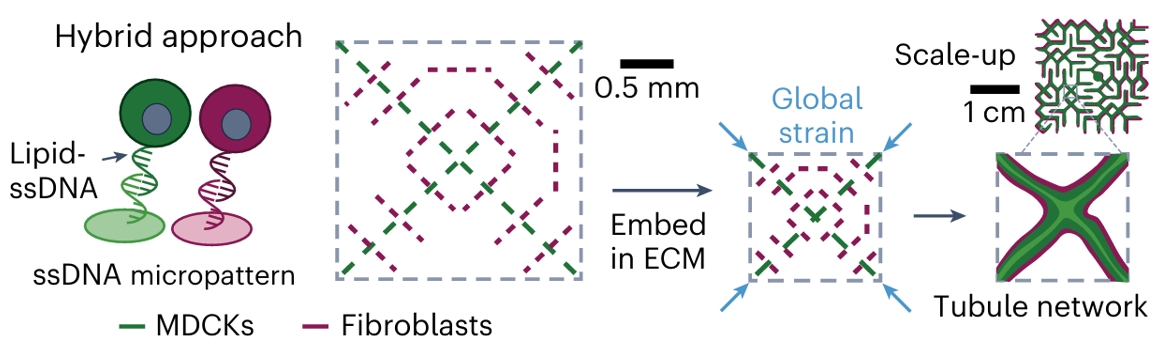
图3d(点击图片可放大)
“动态形态”方法(Kinomorph approach)用于匹配组织尺度的生物打印与自组织长度尺度。
该混合方法(Hybrid approach)首先在二维基底上,通过细胞结合和基底结合的单链DNA(ssDNA)之间的“魔术贴”样碱基配对创建细胞图案,其中脂质单链DNA(Lipid ssDNA)参与介导,基底上设有单链DNA微图案(ssDNA micropattern)。
在这一过程中,以绿色线条标注MDCK细胞(MDCKs),以红色线条标注成纤维细胞(Fibroblasts)。
细胞图案形成后(尺度约0.5 mm),被嵌入细胞外基质凝胶中(Embed in ECM)。
随后,在细胞驱动的全局应变(Global strain)作用下,系统发生自组织,最终扩增形成顶底极化的肾小管网络(Tubule network),尺度可达1厘米(Scale-up 1 cm)。
3.4
肾单位祖细胞工程
在肾单位祖细胞工程中,“传送带”生态位内肾单位祖细胞从皮质向髓质迁移时,细胞张力与粘附力逐渐增加,推动其进入分化状态并形成前小管聚集,分化与自我更新的平衡受Wnt–β-catenin、FGF–EGF–MAPK、Notch、Hippo等多条通路调控。(图4a)
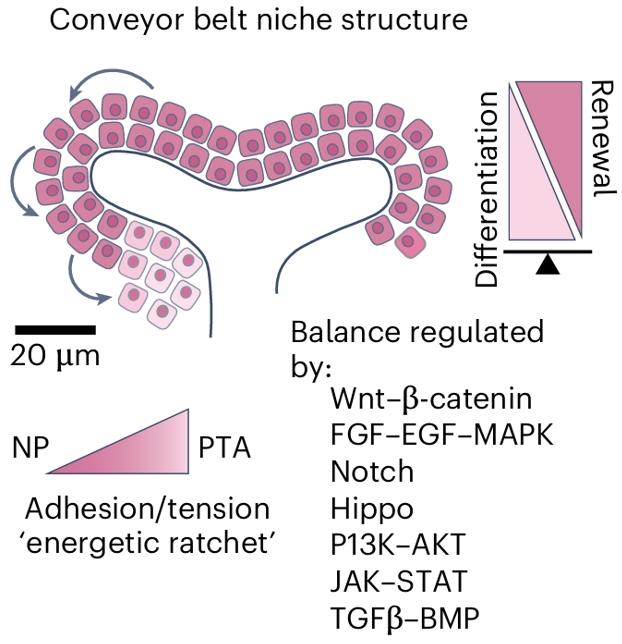
图4a(点击图片可放大)
输尿管芽尖端局部存在肾单位祖细胞的“传送带”生态位结构(Conveyor belt niche structure)。
当肾单位祖细胞(NP)从皮质区向髓质区肾源性区迁移时,其细胞张力与细胞间粘附(Adhesion/tension)逐渐增加,如同“能量棘轮”(energetic ratchet)般推动其进入分化状态,形成前小管聚集(PTA)。
调控肾单位祖细胞分化(Differentiation)与自我更新(Renewal)平衡的关键信号通路包括Wnt–β-catenin、FGF–EGF–MAPK、Notch、Hippo、P13K–AKT、JAK–STAT和TGFβ–BMP。
SynNotch技术可远程控制分化和细胞粘附,通过调控基因表达和钙粘蛋白影响细胞分选,为肾单位祖细胞工程提供了精准工具。(图4b)
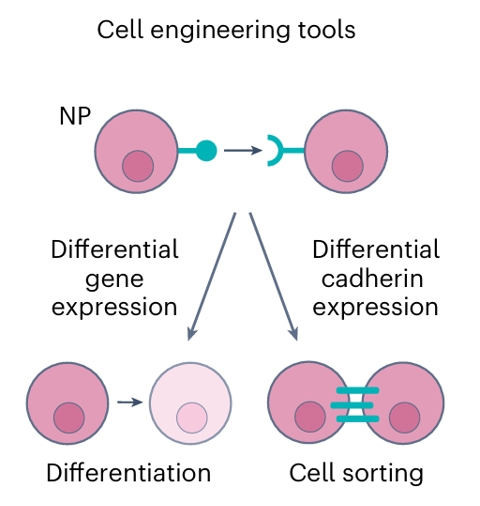
图4b(点击图片可放大)
通过SynNotch及相关技术,可以实现对分化和细胞间粘附进行远程控制的细胞工程(Cell engineering for remote control over differentiation and cell–cell adhesion via SynNotch and related techniques)。
这些细胞工程工具(Cell engineering tools)可应用于肾单位祖细胞(NP),通过调控差异基因表达(Differential gene expression)和差异钙粘蛋白表达(Differential cadherin expression),进而影响分化(Differentiation)和细胞分选(Cell sorting)行为。
此外,体内Wnt–β-catenin梯度诱导肾单位分段,体外则可通过分泌Wnt的“合成组织者”细胞团诱导肾单位方向性与分段,进一步拓展了肾单位祖细胞工程的应用边界。(图4c)
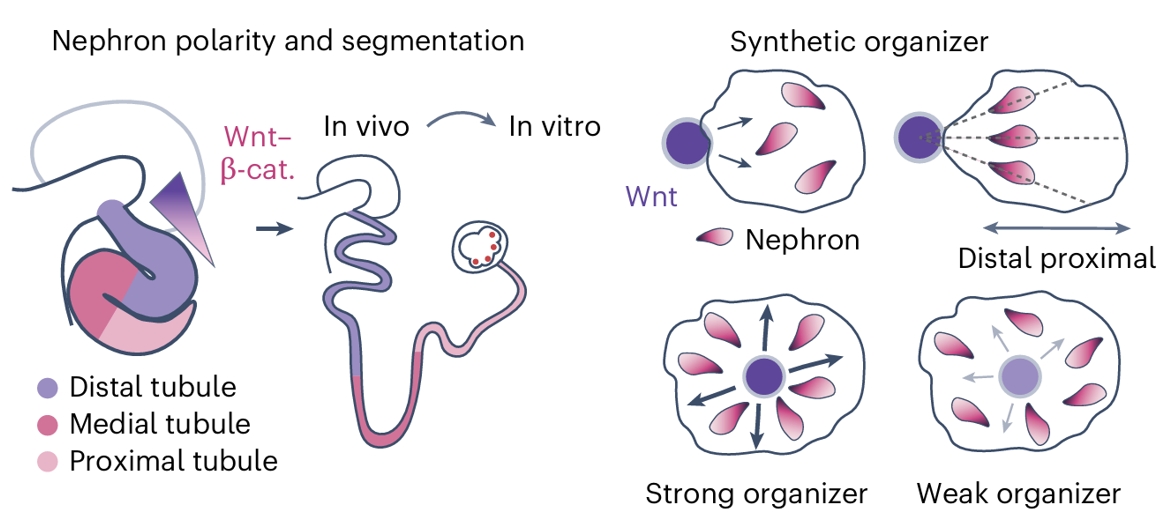
图4c(点击图片可放大)
肾单位极性与分段(Nephron polarity and segmentation)的调控机制体现在体内和体外两种情境中。
在体内(In vivo),沿早期肾单位存在的Wnt–β-catenin(Wnt–β-cat.)梯度诱导分段形成,分别产生远端小管(Distal tubule)、中间小管(Medial tubule)和近端小管(Proximal tubule)。
在体外(In vitro),通过构建分泌Wnt的工程细胞团即合成组织者(Synthetic organizer),可以诱导邻近肾单位谱系细胞产生肾单位方向性与分段(nephron directionality and segmentation)。
强组织者(Strong organizer)和弱组织者(Weak organizer)对远端–近端(Distal proximal)分化的影响也存在差异。
水凝胶的应力松弛特性同样在肾单位祖细胞工程中发挥重要作用,影响肾单位类器官的分段形态、迂曲度和空间分布。(图4d)
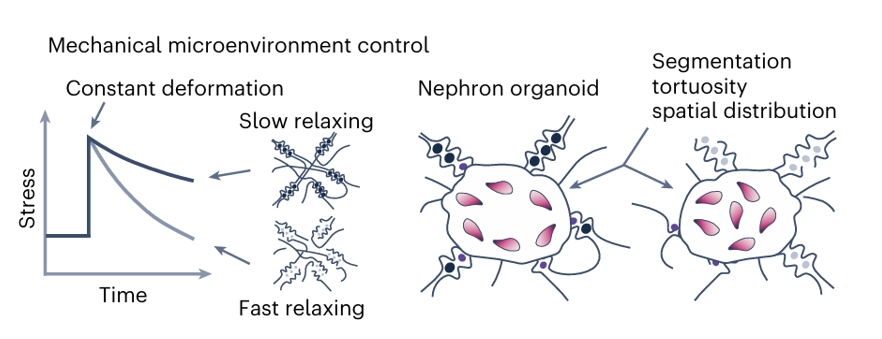
图4d(点击图片可放大)
水凝胶中应力松弛工程(stress relaxation engineering in hydrogels)对肾单位形态与定位的影响可通过力学微环境控制(Mechanical microenvironment control)来阐释。
以应力(Stress)为纵坐标、时间(Time)为横坐标,在恒定形变(Constant deformation)条件下,慢松弛(Slow relaxing)与快松弛(Fast relaxing)水凝胶的应力衰减曲线呈现明显差异。
不同水凝胶力学特性对肾单位类器官(Nephron organoid)形态的影响体现在分段情况(Segmentation)、迂曲度(tortuosity)和空间分布(spatial distribution)等方面。
3.5
输尿管芽工程
在输尿管芽工程研究中,GDNF–RET信号轴驱动输尿管芽分支形态发生(图4e)。
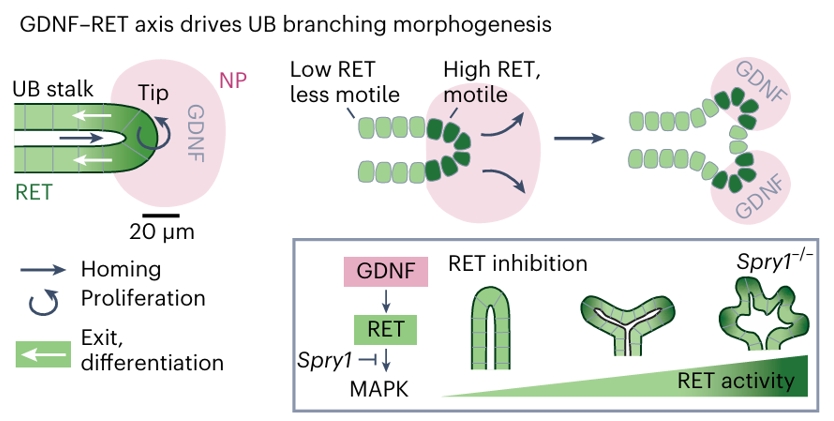
图4e(点击图片可放大)
RET活性对输尿管芽尖端细胞行为的调控体现在多个方面。
GDNF–RET信号轴(GDNF–RET axis)驱动输尿管芽分支形态发生,其中GDNF作用于输尿管芽尖端(Tip)的RET,调控肾单位祖细胞归巢(Homing)、尖端细胞增殖(Proliferation)以及退出与分化(Exit, differentiation),而输尿管芽柄部(UB stalk)细胞RET活性较低。
此外,有假说提出RET通过空间限制性运动驱动尖端细胞发生流体化(tip fluidization by spatially restricted motility),这一过程涉及RET活性、MAPK通路及Spry1的调控关系,包括RET抑制(RET inhibition)和Spry1缺失(Spry1–/–)对RET活性的影响。
光遗传学技术可用于控制RET活性,通过调节光照时间频率和空间模式产生不同分支表型,为输尿管芽工程提供了精准调控工具。(图4f)
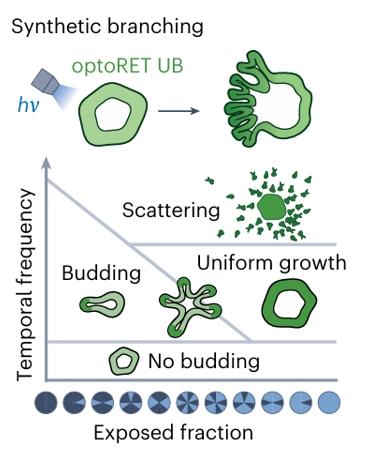
图4f(点击图片可放大)
通过光遗传学控制RET活性(optogenetic control of RET activity)的方案可用于解析细胞集体行为并控制分支形态发生(control over branching morphogenesis)。
该方案利用光照(hν)调控光遗传学修饰的输尿管芽细胞(optoRET UB),并通过调节光照时间频率(Temporal frequency)和暴露模式的空间比例/各向异性(spatial fraction/anisotropy of the exposed pattern)来控制光剂量。
以时间频率为纵坐标、暴露比例为横坐标,不同光照参数下可产生多种分支表型,包括无出芽(No budding)、出芽(Budding)、均匀生长(Uniform growth)和散射(Scattering)。
此外,通过工程化细胞间连接收缩力的各向异性,可合成性控制细胞重排与小管伸长,进一步拓展了输尿管芽工程的调控维度。(图4g)
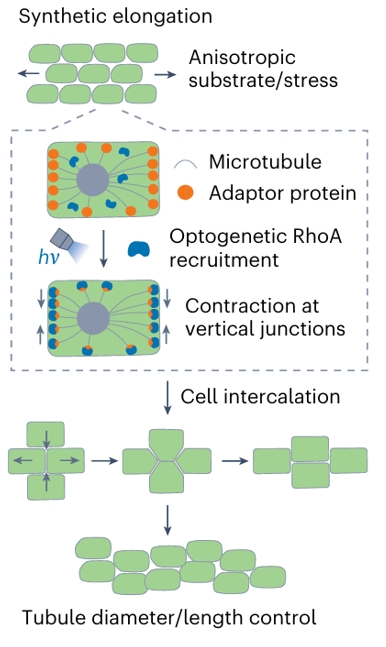
图4g(点击图片可放大)
通过工程化细胞间连接收缩力的各向异性(engineered anisotropy of cell–cell junction contractility),可以实现对细胞顶点操作(cell vertex operations)、细胞重排(cell intercalation)和上皮小管伸长(epithelial tubule elongation)的合成性控制。
这一合成性伸长(Synthetic elongation)策略利用各向异性基底/应力(Anisotropic substrate/stress),通过微管(Microtubule)和衔接蛋白(Adaptor protein)介导,并结合光遗传学RhoA招募(Optogenetic RhoA recruitment),实现垂直连接处的收缩(Contraction at vertical junctions),进而驱动细胞重排,最终对小管直径和长度进行调控(Tubule diameter/length control)。
3.6
输尿管芽–肾单位融合
输尿管芽与肾单位的融合通过细胞身份与生物物理特性的趋同实现。当二者特性匹配时,可发生混合与吻合,形成连续管腔,建立功能性连接。(图4h)
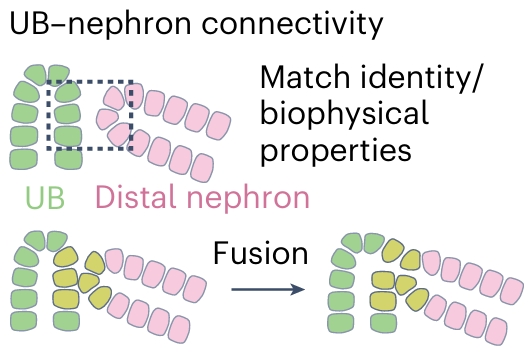
图4h(点击图片可放大)
输尿管芽–肾单位融合(UB–nephron fusion)通过细胞身份与生物物理特性的趋同(convergence of cell identity and biophysical properties)实现。
当输尿管芽(UB)和远端肾单位(Distal nephron)的身份与生物物理特性相匹配时(Match identity/biophysical properties),二者能够发生混合(mixing)、吻合(anastomosis),并在两者之间形成连续管腔(formation of a continuous lumen between the two),最终建立输尿管芽–肾单位连接(UB–nephron connectivity)。
04
间质与血管化
4.1
间质调控
在间质调控方面,间质“传送带”与肾单位形成同步化,通过多种信号分子协调其他谱系:作用于肾单位祖细胞的包括FGF7、YAP/TAZ、FAT4等;作用于输尿管芽的包括维甲酸、肾素/血管紧张素;作用于血管的包括PBX1/PDGFRβ、Netrin、Ephrins等。(图5a)
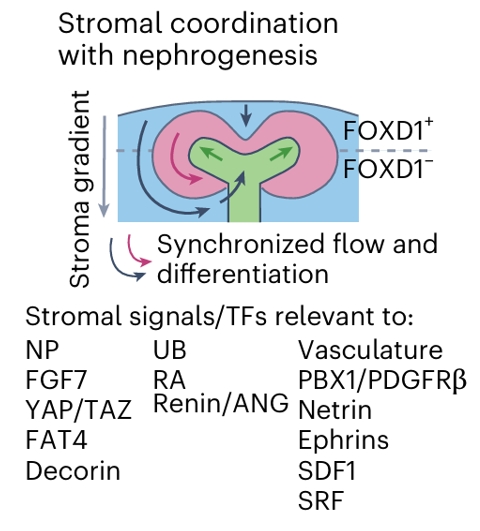
图5a(点击图片可放大)
与肾单位形成同步化的间质“传送带”(The stromal ‘conveyor belt’ synchronized with nephron formation)在肾源性生态位中与其他谱系发生相互作用。间质与肾发生之间存在协调关系(Stromal coordination with nephrogenesis),包括间质梯度(Stroma gradient)以及同步化的低表达与分化(Synchronized low and differentiation),涉及FOXD1阳性(FOXD1+)和FOXD1阴性(FOXD1-)间质细胞。
间质通过多种信号分子/转录因子(Stromal signals/TFs)作用于不同谱系:作用于肾单位祖细胞(NP)的包括FGF7、YAP/TAZ、FAT4、Decorin;作用于输尿管芽(UB)的包括维甲酸(RA)、肾素/血管紧张素(Renin/ANG);作用于血管(Vasculature)的包括PBX1/PDGFRβ、Netrin、Ephrins、SDF1和SRF。
4.2
间质促进高阶结构
关于间质促进高阶结构,仅含肾单位祖细胞和输尿管芽的类器官结构简单,加入间质祖细胞后形成更复杂的高阶类器官。(图5b)
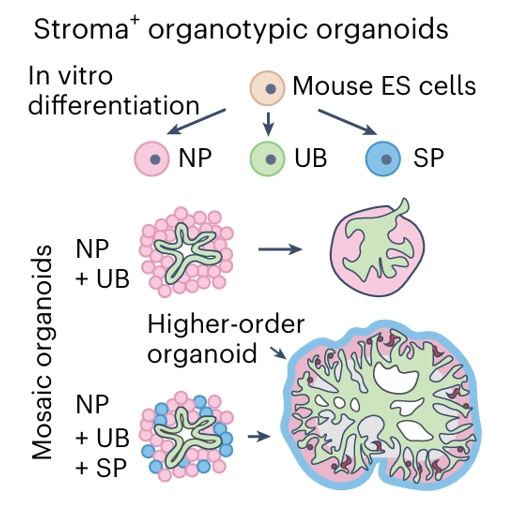
图5b(点击图片可放大)
在嵌合体类器官中引入间质祖细胞(SP cells)可促进高阶结构形成(higher-order structure formation)。
研究通过体外分化(In vitro differentiation)小鼠胚胎干细胞(Mouse ES cells),分别构建了不同组合的嵌合体类器官(Mosaic organoids):一类仅含肾单位祖细胞(NP)和输尿管芽(UB),另一类同时包含肾单位祖细胞(NP)、输尿管芽(UB)和间质祖细胞(SP)。
结果显示,加入间质祖细胞后形成了具有更复杂结构的高阶类器官(Higher-order organoid)。
4.3
血管化策略
在血管化策略方面,微流控芯片可将类器官与促血管生成流动整合,实现血管连接。(图5c)
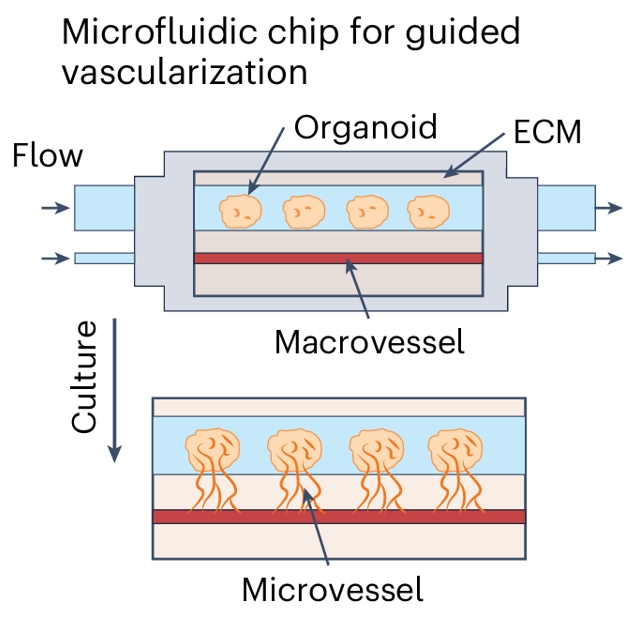
图5c(点击图片可放大)
用于引导血管化的微流控芯片(Microfluidic chip for guided vascularization)通过将类器官(Organoid)与促血管生成流动(proangiogenic flows)进行微流体整合(Microfluidic integration),实现血管连接(vascular connectivity)。
芯片中设有流动(Flow)通道,类器官包埋于细胞外基质(ECM)中,与宏血管(Macrovessel)和微血管(Microvessel)共培养(Culture),最终形成连通的血管网络。
将类器官移植至肾包膜下,可实现宿主血管长入整合,并与宿主集合管建立连接,最终完成血管化与成熟。(图5d)
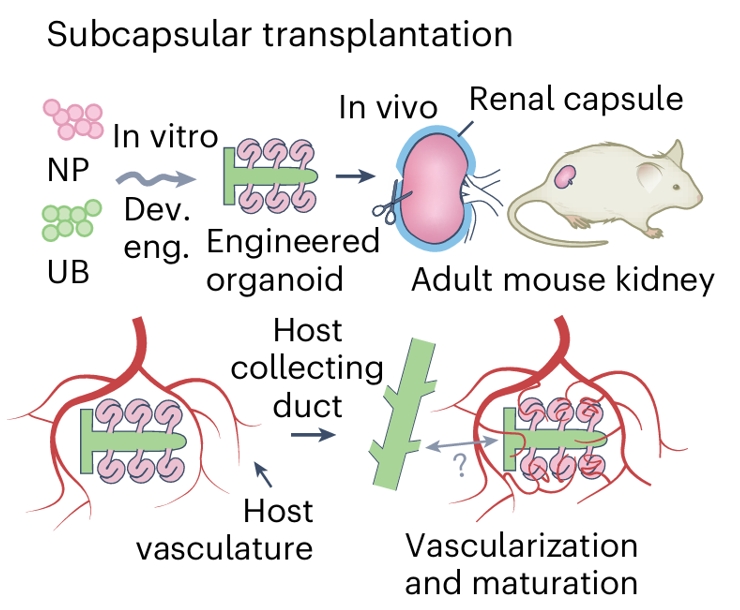
图5d(点击图片可放大)
将体外发育工程(Dev. eng.)构建的工程化类器官(Engineered organoid)移植至肾包膜下(Subcapsular transplantation)是一种有效的体内成熟策略。
工程化类器官包含肾单位祖细胞(NP)和输尿管芽(UB),移植部位为成年小鼠肾脏(Adult mouse kidney)的肾包膜(Renal capsule)下。
在体内(In vivo)环境中,移植物能够实现宿主血管(Host vasculature)的长入整合(integration of host vasculature),并与宿主集合管(Host collecting duct)建立连接,最终完成血管化与成熟(Vascularization and maturation)。
05
未来方向
发育工程学的未来发展需要同步深化对肾脏发育机制的理解,包括自我维持的输尿管芽尖端生态位、肾单位分段调控、分支终止信号及肾单位-输尿管芽吻合机制。
在这一过程中,整合间质、血管和神经结构将进一步提升组织成熟度与功能多样性。
同时,发育工程学可与分化方法改进相结合,包括增强肾单位祖细胞特化、多谱系组装、优化内皮分化等。
合成肾脏组织还可与可穿戴人工肾结合,拓展电解质平衡、血压调节、激素分泌等功能,并为患者来源iPS细胞的无动物疾病建模提供平台,尤其适用于先天性疾病研究。
结语
从解读发育蓝图到再造肾脏组织,发育工程学正推动肾脏类器官研究从“被动自组织”走向“主动引导”的新范式。深入理解三类祖细胞的分化调控、肾源性生态位的信号整合及分支并行化机制,是构建高阶类器官的理论基础。尽管自我维持的生态位、管道吻合与血管整合等挑战仍待突破,但发育工程学正在为肾脏再生医学开辟新的技术路径。
参考文献:
Warrner E, Huang AZ, Hughes AJ. Developmentally inspired synthetic kidney engineering. Nat Biotechnol. 2026 Feb 10.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

