脓毒症相关急性肾损伤(SA-AKI)是危重症常见并发症,病死率高且治疗手段有限,其机制涉及炎症、代谢重编程及多型细胞死亡的复杂交互作用,目前尚未完全阐明。传统动物模型和二维培养难以复现人类肾脏复杂结构与功能。
近年来,人诱导多能干细胞来源的肾脏类器官可在体外模拟肾脏三维微环境与损伤应答,为SA-AKI研究开辟了新路径。本文梳理了近年利用肾脏类器官构建SA-AKI模型的研究进展,从炎症调控、铁死亡、lncRNA保护机制、氧化应激及细胞特异性凋亡等维度,展现该平台在机制探索和治疗靶点筛选中的应用前景。
文献名称:Effect of lipopolysaccharide on ganglioside expression in human induced pluripotent stem cell-derived kidney organoids
发表期刊:Enzyme and Microbial Technology
发表日期:2025年12月刊
研究团队:韩国圆光大学Young-Kug Choo团队
研究概要:
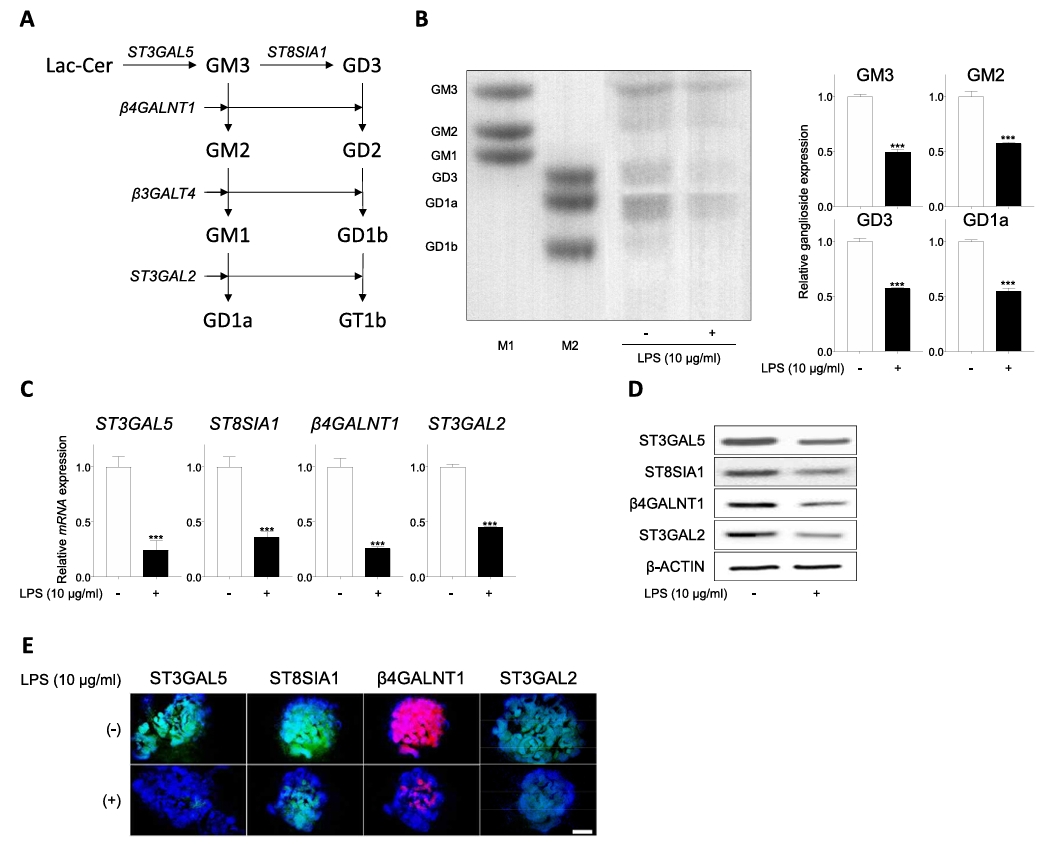
本研究利用人诱导多能干细胞(iPSCs)成功生成了肾脏类器官,并通过脂多糖(LPS)处理建立了脓毒症相关(SA-AKI)急性肾损伤模型。研究发现,LPS处理后,肾脏类器官中炎症相关标志物和活性氧水平显著升高,而线粒体膜电位显著降低。值得注意的是,神经节苷脂GM3、GM2、GD3和GD1a的表达及其生物合成在LPS处理的肾脏类器官中显著下降。这些发现提示神经节苷脂在炎症反应中发挥关键作用,可能参与SA-AKI的病理生理过程,同时证明了肾脏类器官作为研究肾损伤及相关炎症反应模型系统的价值。
文献名称:USP18 promotes ferroptosis in lipopolysaccharide-induced human kidney organoids by stabilizing STING1
发表期刊:Cell Biology and Toxicology
发表日期:2025年8月20日
研究团队:浙江大学医学院附属第一医院肾脏病中心杨浩团队
研究概要:
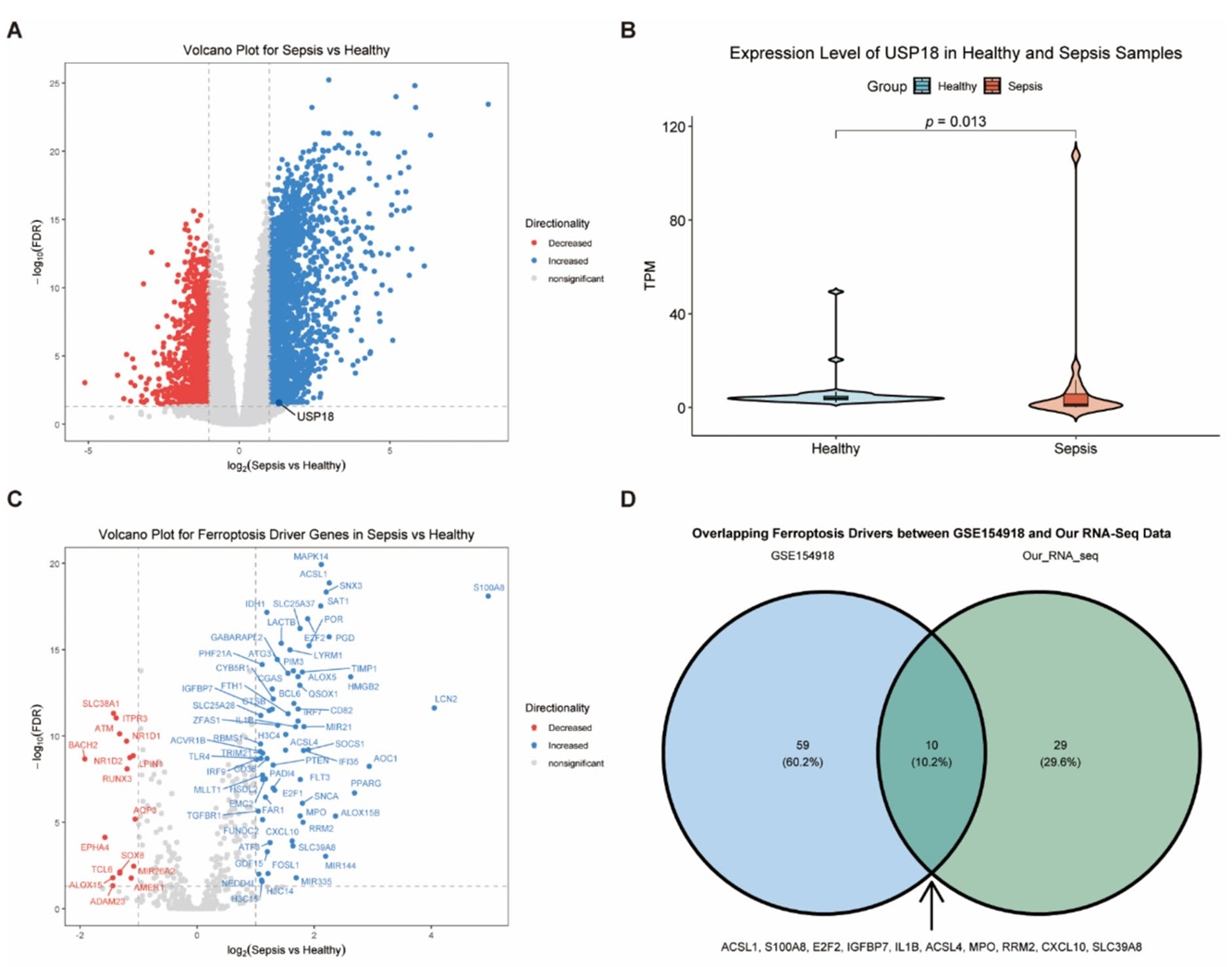
脓毒症诱导的急性肾损伤是一种预后较差的严重疾病。铁死亡可加重脓毒症相关(SA-AKI)损伤,但其调控机制尚不清楚。本研究利用脂多糖(LPS)诱导的人肾脏类器官模型(HKO),通过RNA测序发现USP18是LPS应答中唯一上调的去泛素化酶。进一步研究表明,敲低USP18可显著减少LPS诱导的HKO中的铁死亡。机制上,USP18直接与STING1结合,使其去泛素化并阻止其蛋白酶体降解。在USP18缺陷的HKO中过表达STING1会加剧铁死亡,表明STING1是介导USP18促铁死亡功能的关键分子。该研究揭示了USP18-STING1轴在LPS诱导的HKO铁死亡中的作用,提示靶向USP18-STING1可能为SI-AKI治疗提供新策略。
文献名称:LncRNA AP001007 protects human renal tubular epithelial HK-2 cells and kidney organoids from LPS-induced injury
发表期刊:Scientific Reports
发表日期:2024年11月19日
研究团队:福建省妇幼保健院叶红团队
研究概要:
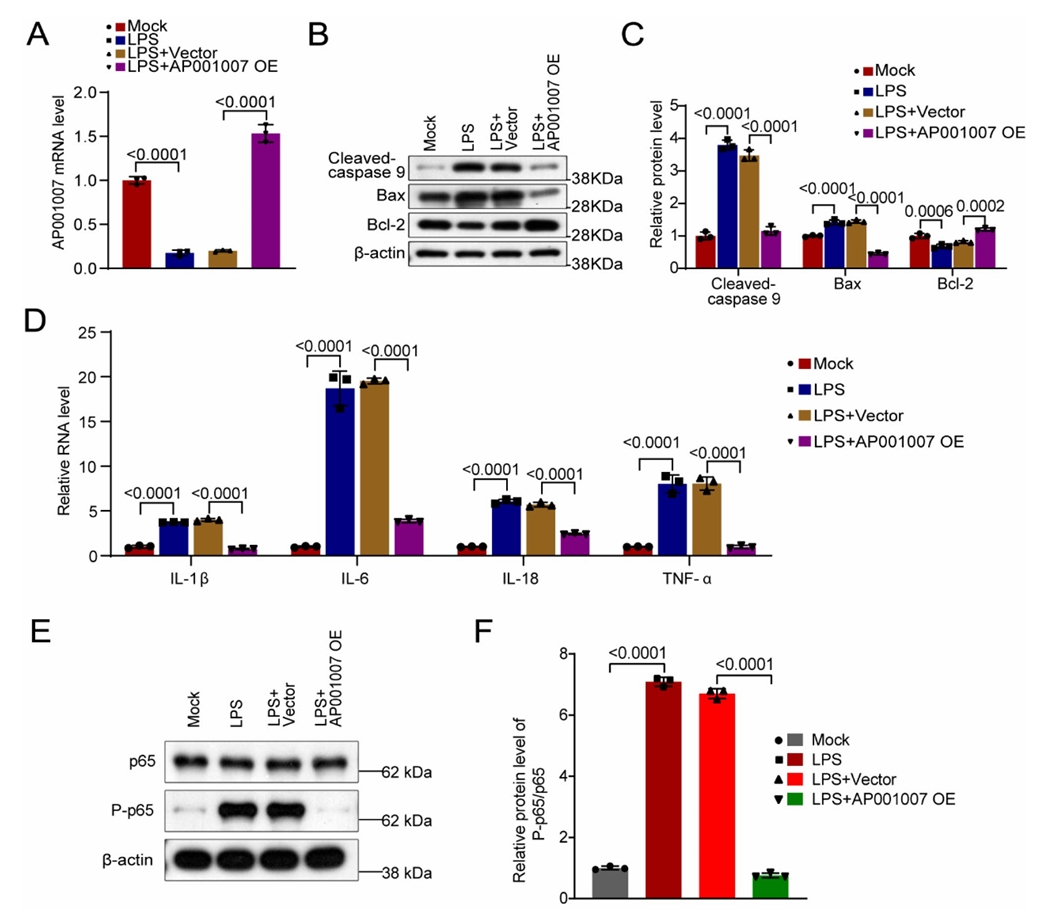
长链非编码RNA的调控与脓毒症相关(SA-AKI)的发病机制相关。本研究检测了脂多糖(LPS)诱导的HK-2细胞和脓毒症患者外周血中lncRNA AP001007的表达。结果显示,LPS处理下调了HK-2细胞中AP001007的表达,且脓毒症患者循环中AP001007水平较低。在HK-2细胞中过表达AP001007可提高LPS暴露下的细胞活力、线粒体活性和存活率,并减少促炎细胞因子的分泌。在LPS处理的人肾脏类器官模型(HKO)中也观察到了类似的保护作用。这些发现表明AP001007对LPS诱导的HK-2细胞和HKO损伤具有保护作用,提示其作为SI-AKI调控因子的潜力。
文献名称:Ascorbate protects human kidney organoids from damage induced by cell-free hemoglobin
发表期刊:Disease Models & Mechanisms
发表日期:2023年12月1日
研究团队:美国范德比尔特大学医学中心Lauren E. Woodard团队
研究概要:
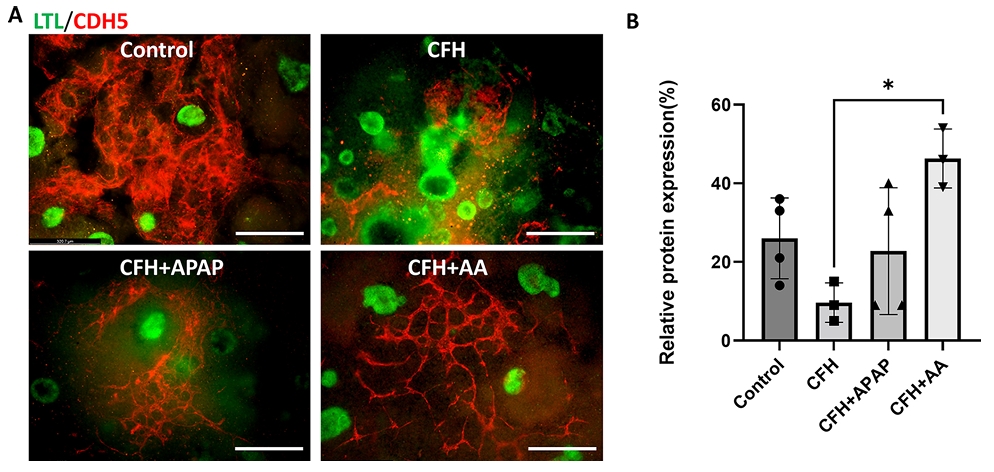
脓毒症相关急性肾损伤与危重患者的高发病率和死亡率相关。游离血红蛋白在重症脓毒症患者血液循环中释放,其水平与死亡率独立相关。本研究利用诱导多能干细胞来源的人肾脏类器官,用细胞游离血红蛋白(CFH)处理48小时,发现与未处理对照组相比,肾小管毒性、氧化应激、线粒体碎片化、内皮细胞损伤和损伤相关转录本均增加。为评估临床可用小分子的保护作用,研究将CFH损伤的类器官与抗坏血酸(AA)或对乙酰氨基酚共同处理48小时。结果显示,AA处理组显著降低了毒性,保护了内皮细胞并减少了线粒体碎片化。该研究提供了AA保护人肾脏细胞免受CFH诱导损伤的直接证据。
文献名称:Kidney Organoids as a Novel Platform to Evaluate Lipopolysaccharide-Induced Oxidative Stress and Apoptosis in Acute Kidney Injury
发表期刊:Frontiers in Medicine
发表日期:2021年11月29日
研究团队:复旦大学附属中山医院泌尿外科朱同玉、许明团队
研究概要:
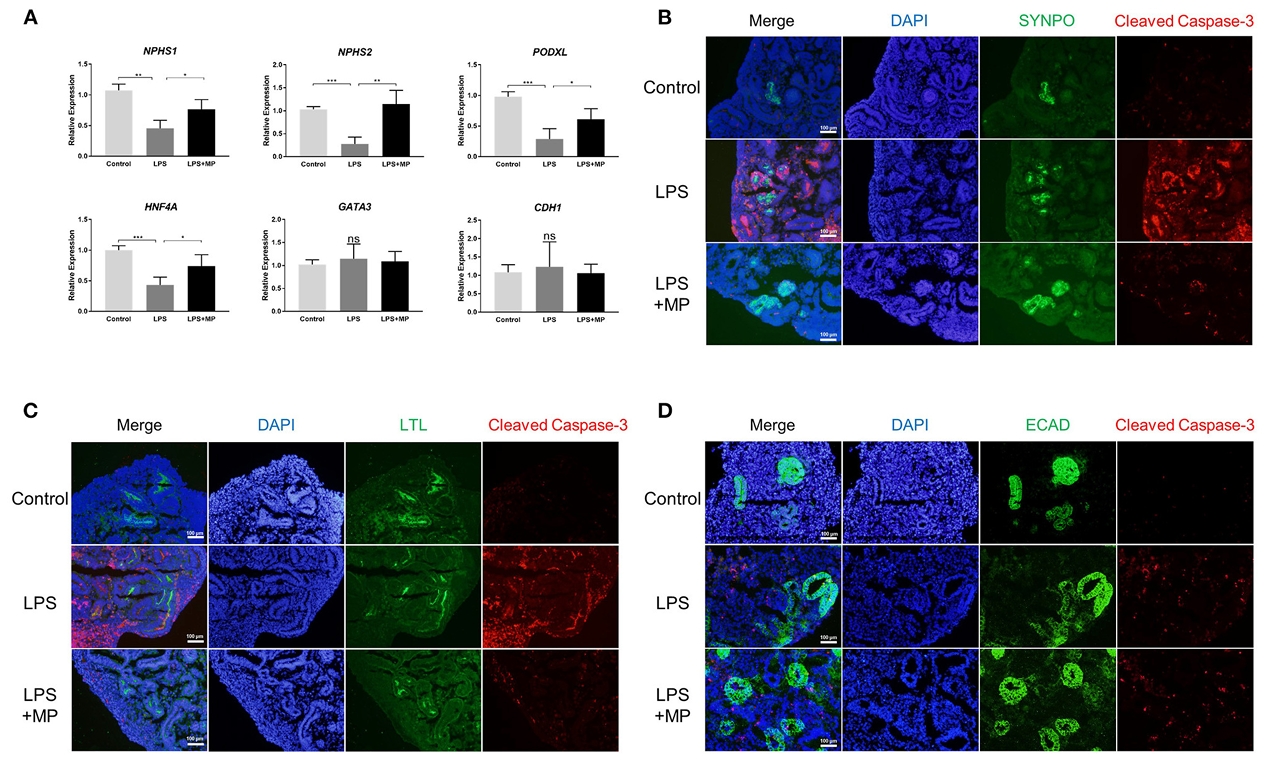
脓毒症相关(SA-AKI)是一种危及生命的综合征。脂多糖(LPS)是体内外模拟SA-AKI的常用诱导剂。本研究在体内和人类肾脏类器官中建立了LPS诱导的肾损伤模型,评估了甲泼尼龙(MP)处理前后肾功能、病理变化和氧化应激标志物,并进一步研究了LPS诱导的肾脏类器官氧化应激和凋亡程度。LPS诱导的小鼠急性肾损伤表现为病理改变、氧化应激增加和肾细胞凋亡增强,而MP治疗可改善这些现象。肾脏类器官实验表明,LPS诱导的凋亡效应主要发生在足细胞和近端小管细胞。该研究证明肾脏类器官可作为研究LPS诱导肾损伤的可靠平台,LPS可独立于灌注变化或免疫细胞浸润诱导肾细胞氧化应激和凋亡,而MP治疗可通过减少肾细胞氧化应激和凋亡来减轻LPS诱导的损伤。
传统模型难以完全模拟脓毒症引起的人类肾脏复杂病理改变。肾脏类器官作为三维人源微组织,为SA-AKI研究提供了更具生理相关性的实验平台。前述五项研究展示了肾脏类器官在SA-AKI领域的应用价值:
机制解析:在LPS或CFH诱导的损伤模型中,揭示神经节苷脂表达下调、USP18-STING1轴促铁死亡、LPS诱导凋亡的细胞类型特异性等新机制。
药物评估:利用损伤类器官筛选潜在治疗分子,如抗坏血酸保护内皮细胞、甲泼尼龙减轻氧化应激与凋亡、AP001007过表达抑制炎症与凋亡。
靶点发现:结合转录组测序,鉴定USP18等关键调控分子,为SA-AKI治疗提供新靶点。
将具备关键肾脏结构与细胞特征的类器官与LPS诱导的损伤模型相结合,为SA-AKI机制研究和药物筛选提供了可设计、可验证的创新平台。
华津肾脏类器官Kidnioid®平台在此领域提供专业支持:
方案咨询:针对类器官构建、损伤模型建立及检测策略提供专业建议。
实验实施:承接肾脏类器官培养、损伤诱导及药物干预实验。
数据支持:提供规范的实验流程与可验证的多维度数据结果。
基于华津Kidnioid®平台在肾脏类器官培养和疾病模型构建领域的技术积累,华津Kidnioid®平台能够确保模型构建的规范性和实验结果的可靠性。
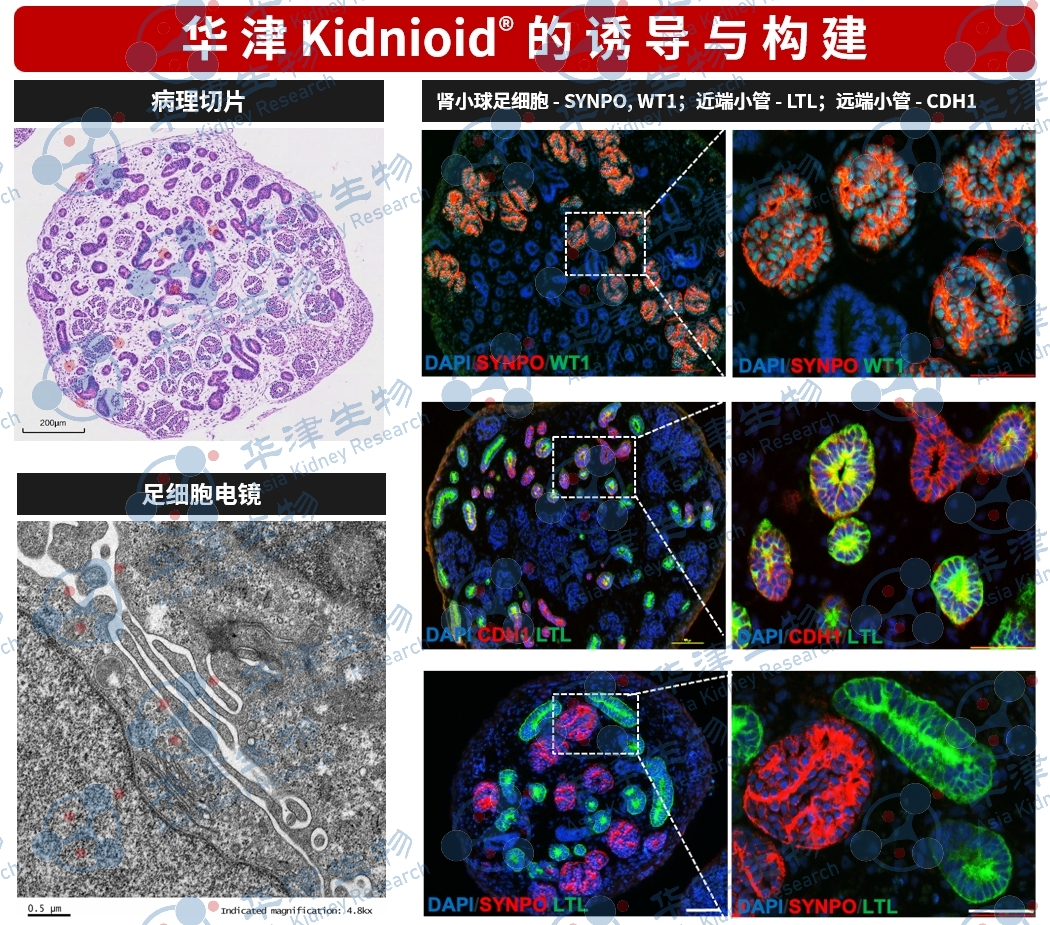
基于人源肾脏类器官构建,包含近端小管、足细胞等功能结构,可呈现SA-AKI相关的病理变化,如炎症、氧化应激、细胞凋亡与铁死亡。
该模型可支持药物作用机制研究、多信号通路协同分析及细胞类型特异性损伤评估。
适用于SA-AKI机制研究、药物筛选及药效评估。
周期较短:相比部分动物实验,模型构建与评估时间有所缩短。
模型稳定性较好:在标准化培养条件下,模型稳定性较高。
灵活性较强:可根据研究需求进行定制化调整。
检测体系适配性高:与常规分子生物学/细胞生物学方法高度兼容,可直接开展qPCR、Western blot、免疫荧光等检测,便于机制研究与多指标评价。
感谢您对本文的浏览。肾脏类器官作为前沿生物技术,不仅在疾病模拟、药物筛选和再生医学研究中展现出巨大潜力,也为精准医疗和新药研发提供了更可靠的平台。目前全球多家监管机构已将其纳入药物评价体系,标志着该技术正逐步走向标准化与应用化。如果您希望进一步了解肾脏类器官的技术细节、合作研究或商业应用,欢迎随时联系咨询:
商务支持 - 李老师 17276665437
技术支持 - 田老师 18843183823
我们期待为您提供专业服务与合作支持。

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

