
近日,澳大利亚莫纳什大学Jay C. Jha团队在 Biomedicines 期刊发表了题为“Technological Innovations and the Translational Path of Kidney Organoids”的系统性综述,梳理了肾脏类器官在分化策略、培养体系、疾病模型构建及再生医学应用方面的研究进展。
肾脏类器官由人多能干细胞或成体干细胞衍生,可模拟人肾单位的细胞异质性、空间构型及部分生理功能。血管化不足、功能成熟度低、标准化生产困难等问题仍制约其临床转化。本文基于该综述的框架,整理肾脏类器官的关键技术进展与主要瓶颈。
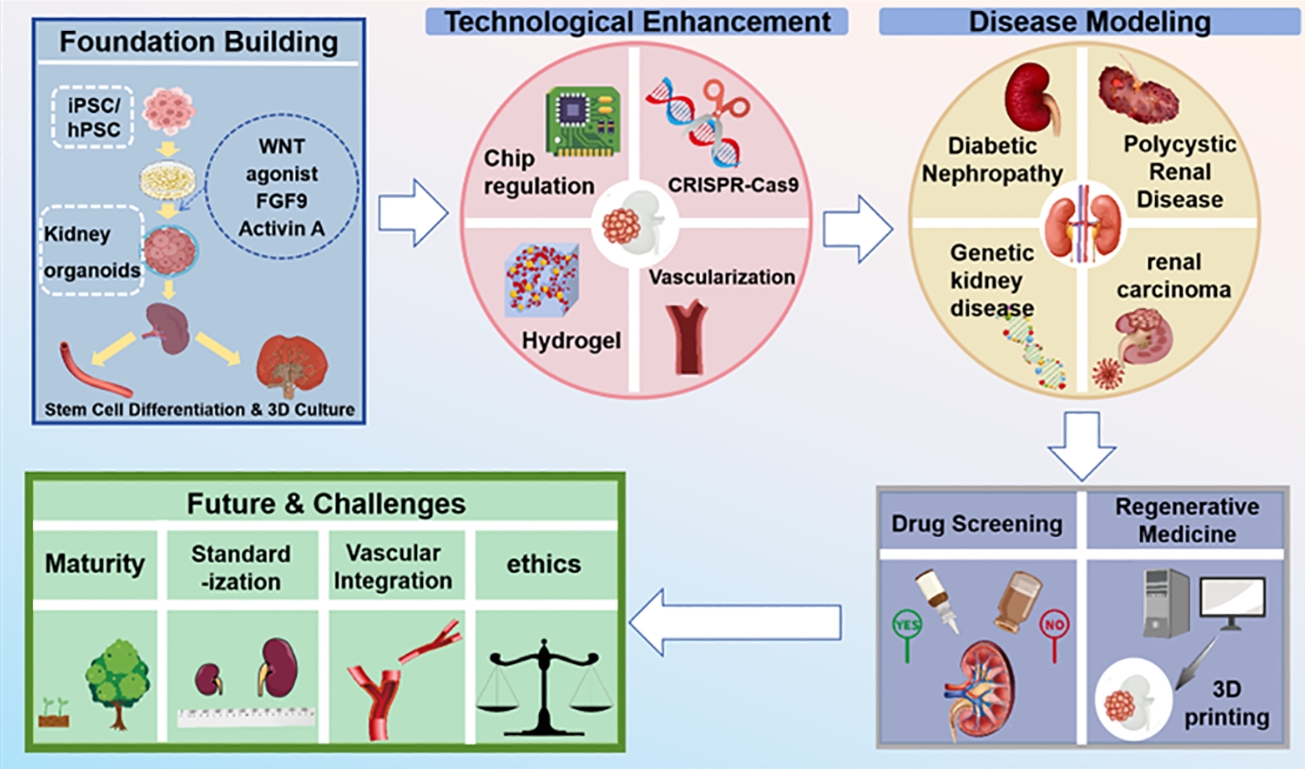
图形摘要
技术进展
1.1 干细胞分化策略
自2014年Taguchi等建立人类多能干细胞(hPSC)来源肾脏类器官的基础方案后,研究者围绕多个方向进行了优化。Vanslambrouck等通过延长Wnt信号激活时间并时序性添加FGF9,提升了近端肾小管细胞的成熟度,使其具备白蛋白吸收和有机阳离子转运能力。Huang等通过小分子调控p38和YAP信号通路,实现了肾祖细胞的长期二维扩增,进而生成高纯度足细胞类器官。
1.2 培养体系的工程化
合成水凝胶正逐步替代动物源基质胶。Clerkin等使用半合成甲基丙烯酰化明胶(GelMA)水凝胶培养肾脏类器官,发现其硬度(约5000-10000 Pa)更接近成人肾脏组织,与较软基质(约400 Pa)相比,可改善足细胞成熟度。
血管化策略方面,Homan等通过微流控芯片施加流体剪切应力,促进类器官内形成可灌注的血管网络。Garreta等利用鸡胚绒毛尿囊膜移植技术,诱导了肾小囊和肾单位结构的形成。
1.3 质量评估技术
单细胞转录组学显示,早期类器官中常存在脱靶的神经元样细胞,优化后的分化方案可将目标肾脏细胞比例提升至90%以上。高内涵成像技术结合深度学习算法,已能实现类器官形态和功能成熟度的自动化定量分析。
(点击可放大)
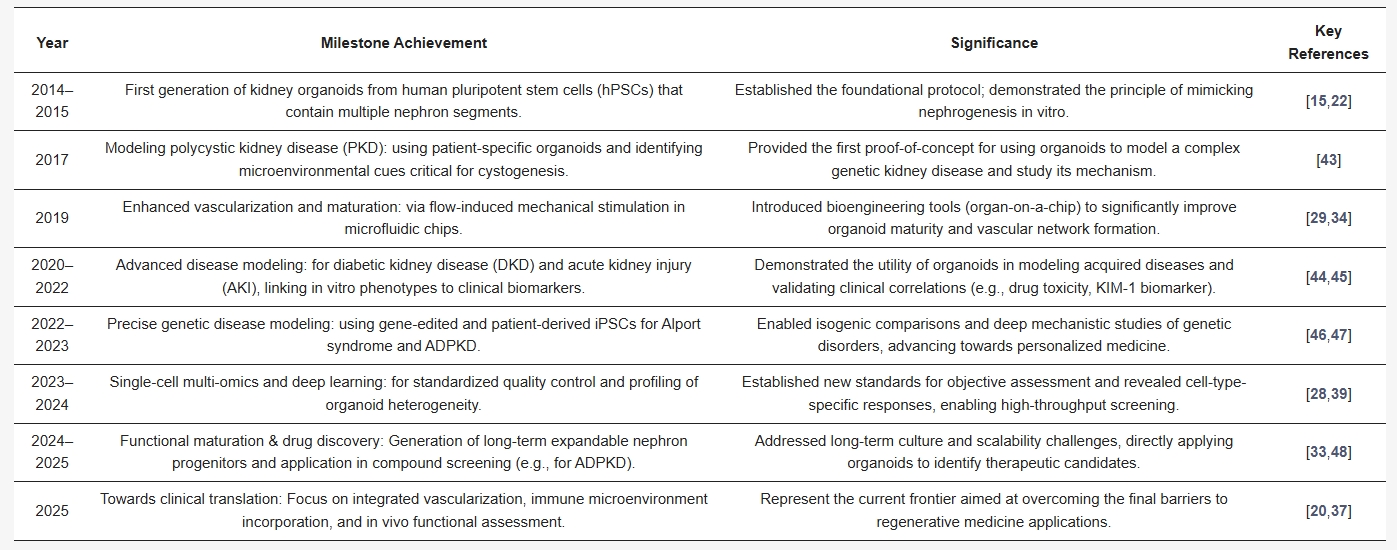
表1. 肾脏类器官模型的主要进展时间线。该时间线总结了2014年至2025年肾脏类器官研究领域的关键方法学突破与疾病建模应用。所选里程碑代表了奠定基础方案、推动新型疾病建模或应对成熟度与可扩展性核心挑战的重要研究。这一进展展示了该领域从体外肾单位生成向功能评估与临床转化演进的历程。
主要应用
2.1 疾病模型
糖尿病肾病:在糖尿病肾病领域,足细胞与系膜基质之间的相互作用是类器官相较于传统细胞模型的显著优势。Garreta等证明,糖尿病微环境可增加肾小管细胞中ACE2的表达,显示了肾脏类器官在模拟糖尿病特异性分子病理方面的应用价值。Clerkin等利用肾脏类器官中的TGFβ诱导的DKD损伤模型,研究机械环境对早期纤维化样特征传播的影响。在较软基质中培养可降低pSMAD3表达,改善α-SMA等肌成纤维细胞标志物。
遗传性肾病:利用CRISPR-Cas9构建携带NPHS1或COL4A5突变的人多能干细胞,其分化的类器官可复现足细胞裂孔隔膜缺陷或基底膜IV型胶原异常结构,为基因型-表型关联研究提供了平台。
急性肾损伤:顺铂处理的肾脏类器官中,近端肾小管细胞凋亡标志物BAX/BAK上调,刷状缘脱落,损伤程度与临床给药剂量呈正相关。
多囊肾病:Mae等建立了hiPSC来源的输尿管芽尖端细胞扩增培养体系,PKD1突变来源的集合管类器官可自发形成多发性囊肿。Vishy等利用碱基编辑技术构建携带PKD1-R2430X无义突变的类器官,用于药物筛选,如评估通过通读无义突变恢复多囊蛋白表达的化合物。
肾纤维化:Yang等通过外源性TGF-β1长期刺激,在iPSC来源肾脏类器官中成功诱导细胞外基质成分生成,并上调α-SMA等纤维化标志物。胆汁酸受体激动剂可通过调控下游SMAD3和TAZ通路,显著减轻TGF-β1诱导的纤维化。
(点击可放大)
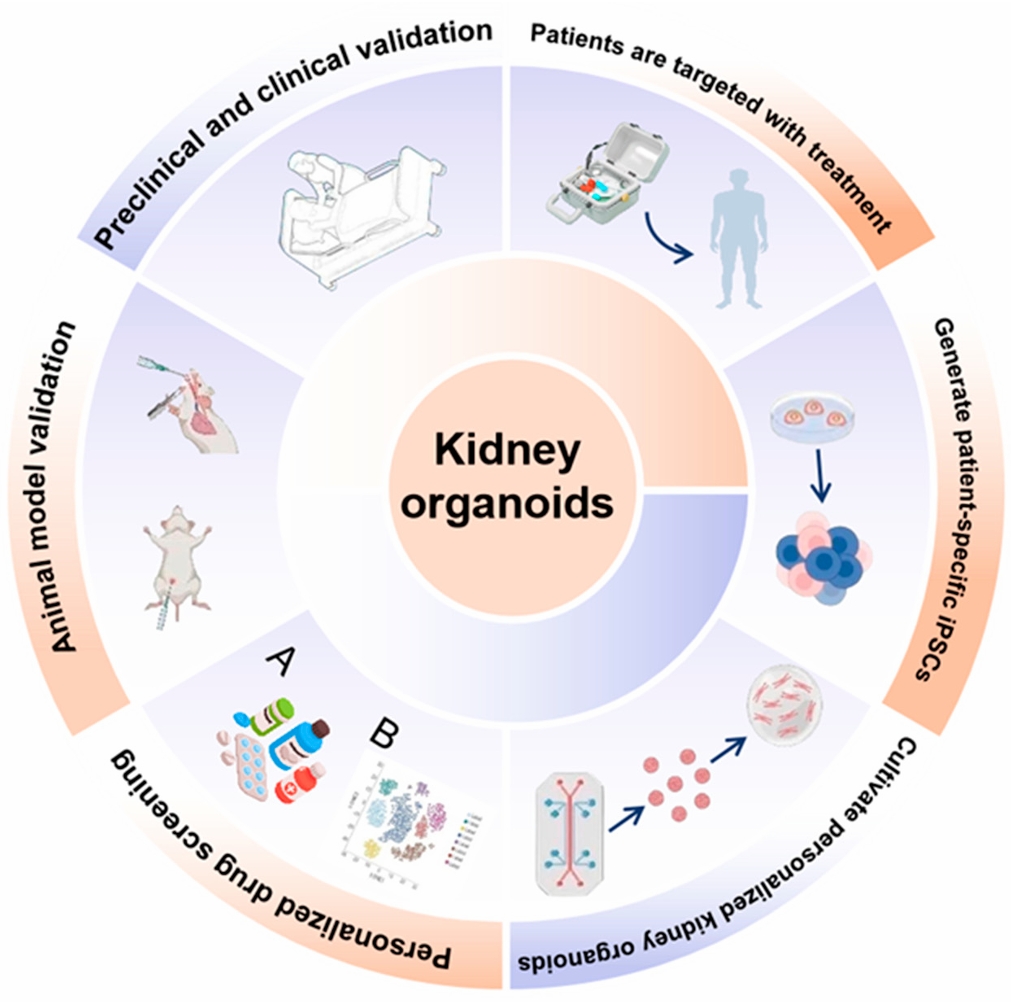
图1. 肾脏类器官的应用与转化框架。该示意图概述了肾脏类器官的生成、应用及临床转化路径。人类多能干细胞或患者特异性诱导多能干细胞(iPSC)分化为肾脏类器官,可重现人肾脏的关键结构与细胞特征。这些类器官可用于个性化药物筛选与毒性测试、疾病建模以及分子与细胞水平的机制研究。肾脏类器官与组学分析(A、B)、微流控及血管化平台、功能检测相结合,用于评估发育、损伤与修复过程。通过动物模型验证及临床前与临床研究,支持其在转化研究中的应用。最终,肾脏类器官可推动患者特异性建模、靶向治疗发现及精准医学策略,连接基础研究与临床应用。
(点击可放大)
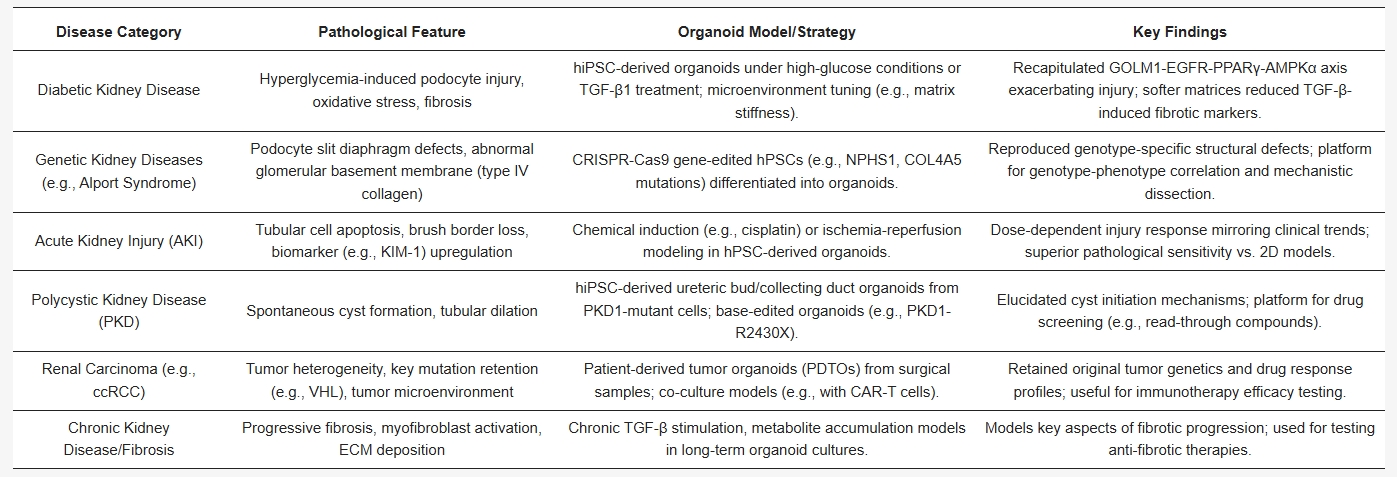
表2. 类器官平台中的肾脏疾病模型。该表展示了人多能干细胞来源及患者来源的肾脏类器官在多种肾脏疾病中重现关键病理特征的能力。通过基因编辑、微环境调控、慢性因子暴露等策略,这些体外模型能够忠实模拟人类特异性疾病表型,涵盖遗传性疾病的结构缺陷、功能性损伤及纤维化进展等不同类型。它们为机制解析与治疗探索提供了重要平台。
2.2 药物开发
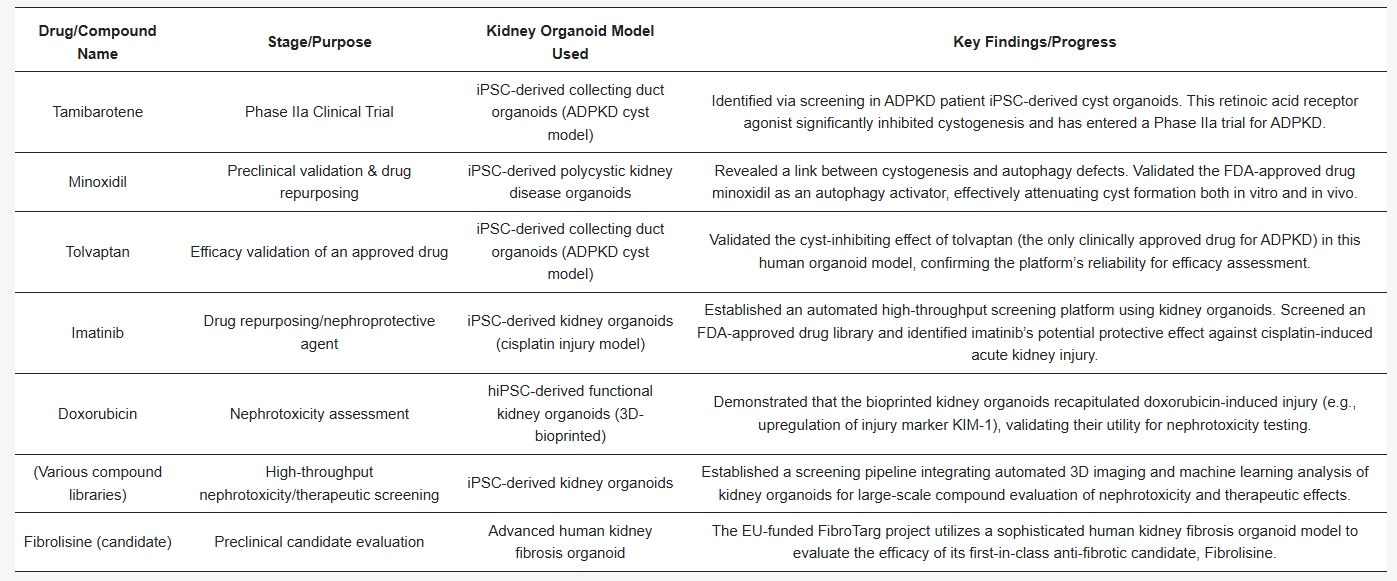
在ADPKD患者来源的集合管类器官中,筛选出维甲酸受体激动剂tamibarotene可抑制囊肿形成,目前已进入IIa期临床试验。基于类器官建立的高通量筛选平台,从FDA批准药物库中鉴定出伊马替尼对顺铂诱导的急性肾损伤具有保护作用。
(点击可放大)
表3. 肾脏类器官模型在药物发现与评估中的应用。该表展示了人肾脏类器官模型在药物发现与毒性评估各阶段的应用价值。所列研究涵盖了从高通量筛选、药物重定位到临床候选药物验证及肾毒性评价等应用场景。这些模型提供了一个具有生理相关性的人类平台,能够重现疾病特异性表型,填补了传统体外实验与肾脏疾病药物临床试验之间的空白。
2.3 再生医学
Homan等发现,体外发育过程中施加高流体剪切应力可增强肾小管和肾小球区室血管系统的丰度与成熟度。Wang等利用SIX1和SALL1缺陷的肾缺陷猪胚胎,成功形成了具有组织结构的人-猪嵌合中肾结构,提示在器官发育障碍的猪体内生成人源化原始器官的潜力。
主要瓶颈
3.1 功能成熟度
目前肾脏类器官的上皮细胞仅成熟至中晚期胎儿阶段,影响其转运功能。代谢重编程策略(如时序性添加缺氧敏感因子模拟肾髓质氧梯度、激素脉冲刺激增强尿素浓缩能力)尚处于探索阶段。
3.2 血管网络整合
现有类器官中功能性微血管形成率低,且缺乏与大血管的整合,导致肾小球发育延迟和滤过效率下降。当前方法(如流体剪切应力、鸡胚移植)尚未解决大血管吻合问题。
3.3 标准化生产
批次间细胞异质性和基质胶成分波动限制了标准化生产。光图案化水凝胶虽可通过动态调控形态发生素梯度(如BMP7/WNT)提高肾单位空间排列精度,但血管整合不足和长期功能维持仍是深层瓶颈。
展望
肾脏类器官技术正从静态结构仿生向动态功能模拟推进。未来研究需聚焦血管化这一核心瓶颈,同时整合器官芯片、人工智能驱动的功能分析、生物材料介导的微环境调控等工具,以构建更具预测性的模型,推动肾脏类器官向临床转化。
(点击可放大)
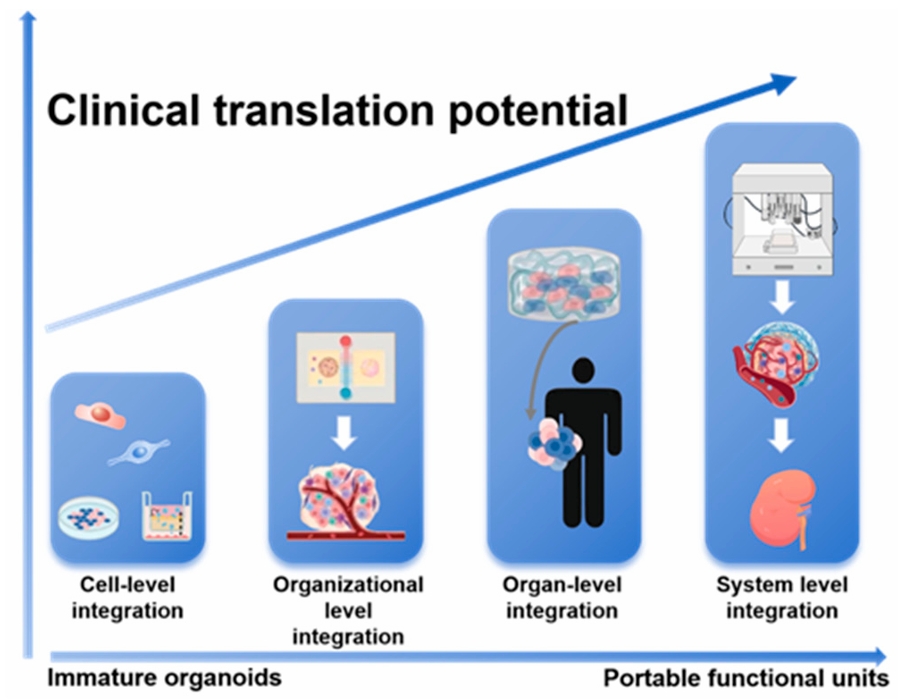
图2. 推动肾脏类器官向临床应用的层级整合范式。该示意图概述了一种分阶段工程化策略,旨在克服类器官成熟度与功能方面的局限。该范式通过依次提升复杂度——从细胞层面、组织层面整合,到器官层面,最终实现系统层面整合——逐步推进。这一递进式方法推动未成熟类器官向功能性、可移植单元转化,增强其在再生医学中的转化潜力。
总 结
肾脏类器官技术已在分化策略、培养体系、疾病建模及药物筛选等方面取得进展,但血管化不足、功能成熟度低、标准化生产困难仍是制约其临床转化的主要瓶颈。当前研究已识别出流体剪切应力、内皮定向诱导等血管化路径,以及代谢重编程、时序性因子添加等成熟度提升策略,并在多种疾病模型中验证了类器官的应用价值。然而,如何将这些机制认知转化为稳定、可重复的技术方案,实现血管网络整合与功能成熟度的协同提升,仍有待多学科交叉的进一步探索。
参考文献:
Li A, Chai Z, Jandeleit-Dahm K, Jha JC. Technological Innovations and the Translational Path of Kidney Organoids. Biomedicines. 2026 Jan 31;14(2):327. doi: 10.3390/biomedicines14020327.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

