近年来,人诱导多能干细胞(iPSC)来源的肾脏类器官能够在体外形成具有多种肾单位节段和细胞类型的三维结构,为药物开发提供了兼具人类遗传背景与组织复杂性的实验模型。与传统二维细胞培养和动物模型相比,肾脏类器官在药物发现、肾毒性评价、药效评估及药物递送等方面展现出独特价值。
本文围绕肾脏类器官在药物开发平台中的应用进展进行梳理,从药物发现、肾毒性评价、药效评估及药物递送四个维度,总结了该领域的主要技术进展与研究成果。
1
基于附加型DNA载体工程化肾脏类器官实现促红细胞生成素递送
文献名称:Erythropoietin delivery through kidney organoids engineered with an episomal DNA vector
发表期刊:Stem Cell Research & Therapy (IF: 7.3)
发表日期:2025年4月12日
研究团队:荷兰伊拉斯姆斯大学医学中心Martin J. Hoogduijn团队
研究概要:
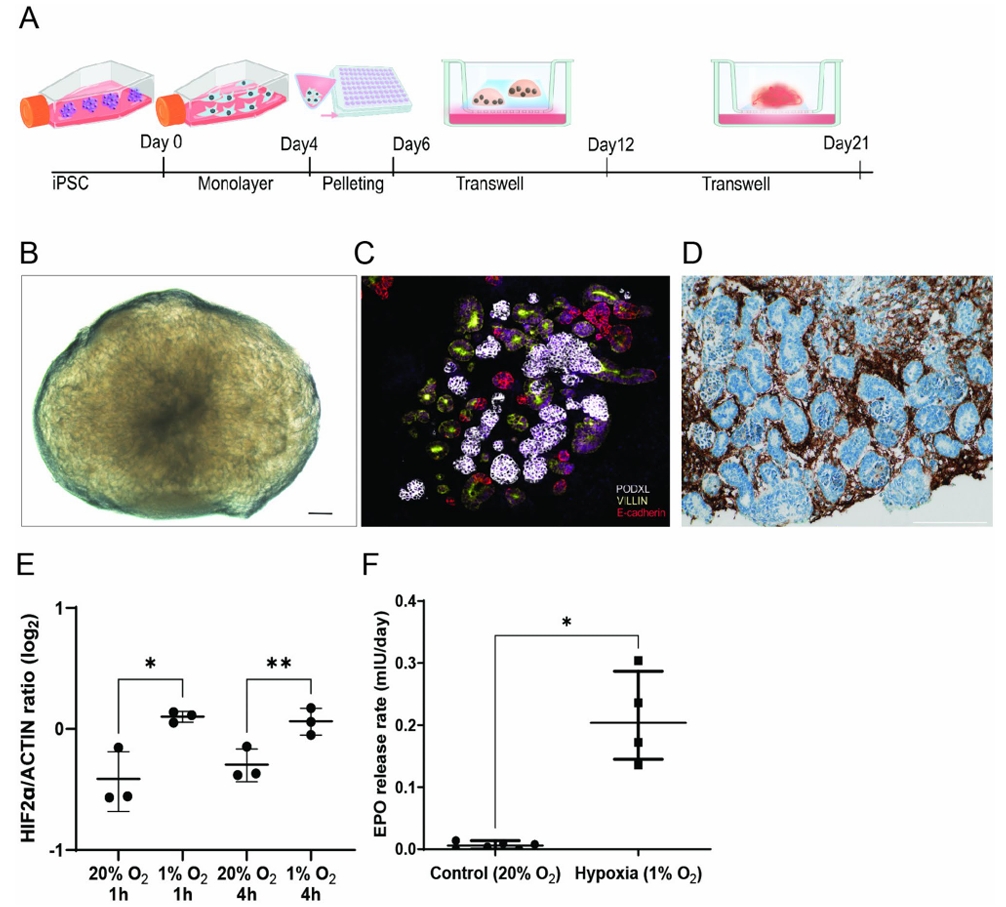
本研究探索了利用人诱导多能干细胞(iPSC)来源的肾脏类器官恢复促红细胞生成素(EPO)产生的潜力。通过非整合型S/MAR DNA载体将EPO基因导入iPSC,构建了EPO过表达的肾脏类器官。将该类器官植入免疫缺陷小鼠皮下后,EPO mRNA水平持续升高,内皮细胞数量显著增加,小鼠血细胞比容水平呈类器官数量依赖性升高,并观察到骨稳态的改变。研究表明,经EPO S/MAR DNA载体修饰的肾脏类器官可实现EPO的稳定长期递送,为内分泌替代疗法提供了新策略。
(点击图片可放大)
图1. 工程化EPO过表达肾脏类器官的体内植入效果。植入后1个月,EPO过表达类器官在体内持续维持高水平的EPO mRNA表达,并显著增加植入部位的内皮细胞数量。小鼠血细胞比容水平呈类器官数量依赖性升高,同时骨小梁组成发生改变,证实工程化肾脏类器官可实现稳定的EPO长期递送并产生系统性生理效应。
2
通过自动化3D成像实现基于肾脏类器官的高通量筛选以推进临床前药物评价
文献名称:Advancing preclinical drug evaluation through automated 3D imaging for high-throughput screening with kidney organoids
发表期刊:Biofabrication (IF: 8.0)
发表日期:2024年4月8日
研究团队:美国麻省总医院、哈佛大学Ryuji Morizane团队
研究概要:
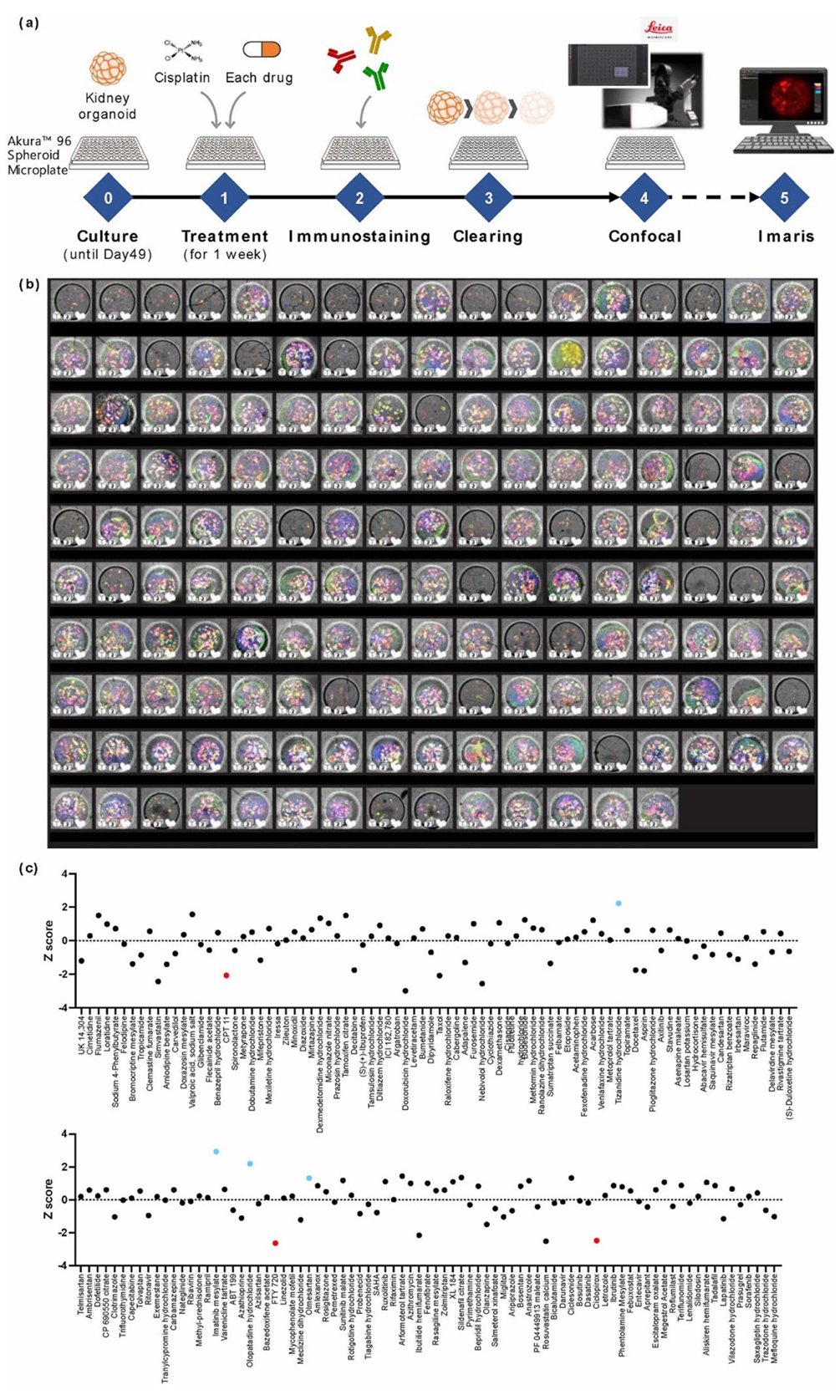
本研究针对肾脏类器官三维结构复杂性限制其用于高通量药物筛选的技术瓶颈,开发了全自动3D成像结合机器学习的方法,实现对肾单位节段特异性上皮形态学的自动分析。利用肾毒性药物顺铂诱导类器官发生急性肾损伤,并使用FDA批准的药物库进行治疗和肾毒性筛选。自动化3D图像采集与分析流程成功识别出顺铂化疗期间具有肾毒性或治疗作用的药物,其中伊马替尼被鉴定为潜在的顺铂肾损伤预防药物。该研究建立了基于肾脏类器官3D形态学的高通量筛选平台,可用于肾毒性评估和治疗药物筛选。
(点击图片可放大)
图2-1. 基于肾脏类器官与体积分析的高通量药物筛选。通过建立自动化筛选流程,对每孔单个肾脏类器官进行明场与共聚焦荧光成像,并基于近端小管标志物LTL阳性结构的总体积计算Z评分,成功从FDA批准药物库中筛选出具有潜在肾保护作用或肾毒性作用的候选药物。

(点击图片可放大)
图2-2. 通过建立顺铂诱导的肾损伤模型,结合免疫荧光染色与机器学习辅助的物体分类分析,对候选化合物进行肾保护作用评估。结果显示,特定化合物处理组中LTL阳性结构的总体积显著高于顺铂损伤对照组,表明这些化合物可有效减轻顺铂诱导的肾小管损伤。
3
肾脏类器官模型揭示纤毛-自噬代谢轴作为多囊肾病治疗靶点
文献名称:Kidney organoid models reveal cilium-autophagy metabolic axis as a therapeutic target for PKD both in vitro and in vivo
发表期刊:Cell Stem Cell (IF: 20.4)
发表日期:2024年1月4日
研究团队:新加坡南洋理工大学夏云等团队
研究概要:
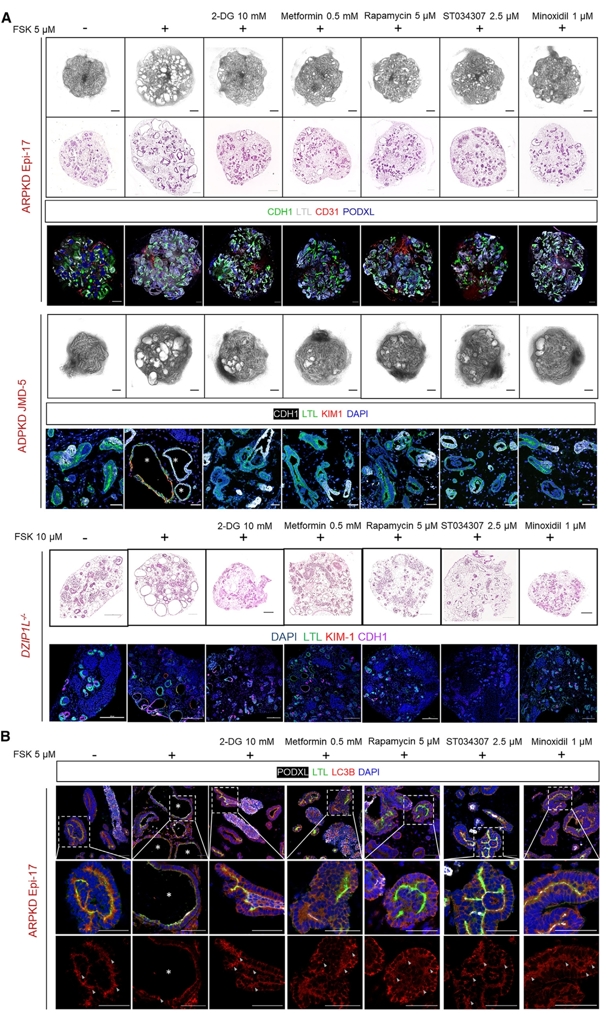
本研究利用人胚胎干细胞来源的肾脏类器官,建立了体外和体内的多囊肾病(PKD)模型,该模型表现出肾小管损伤和肾素-血管紧张素-醛固酮系统的异常上调。单细胞分析揭示囊肿发生过程中发生多种代谢改变,包括自噬缺陷。通过ATG5过表达或纤毛消融实验性激活自噬,可显著抑制PKD类器官的囊肿形成。利用自发形成肾小管囊肿的PKD类器官异种移植模型,研究发现FDA批准的自噬激活剂米诺地尔(Minoxidil)在体内可有效减轻囊肿形成。该研究为PKD的发病机制和药物验证提供了新平台。
(点击图片可放大)
图3. 在毛喉素诱导的囊肿形成模型中,分别对ARPKD、ADPKD及H9 DZIP1L-/-肾脏类器官进行候选药物处理。结果显示,特定药物处理可显著抑制囊肿形成,同时伴随自噬体标志物LC3B表达的升高,提示激活自噬可能是抑制囊肿形成的潜在作用机制。
4
人iPSC来源的肾集合管类器官模型用于ADPKD囊肿发生研究
文献名称:Human iPSC-derived renal collecting duct organoid model cystogenesis in ADPKD
发表期刊:Cell Reports (IF: 6.9)
发表日期:2023年12月26日
研究团队:日本京都大学iPS细胞研究与应用中心长船健二团队
研究概要:
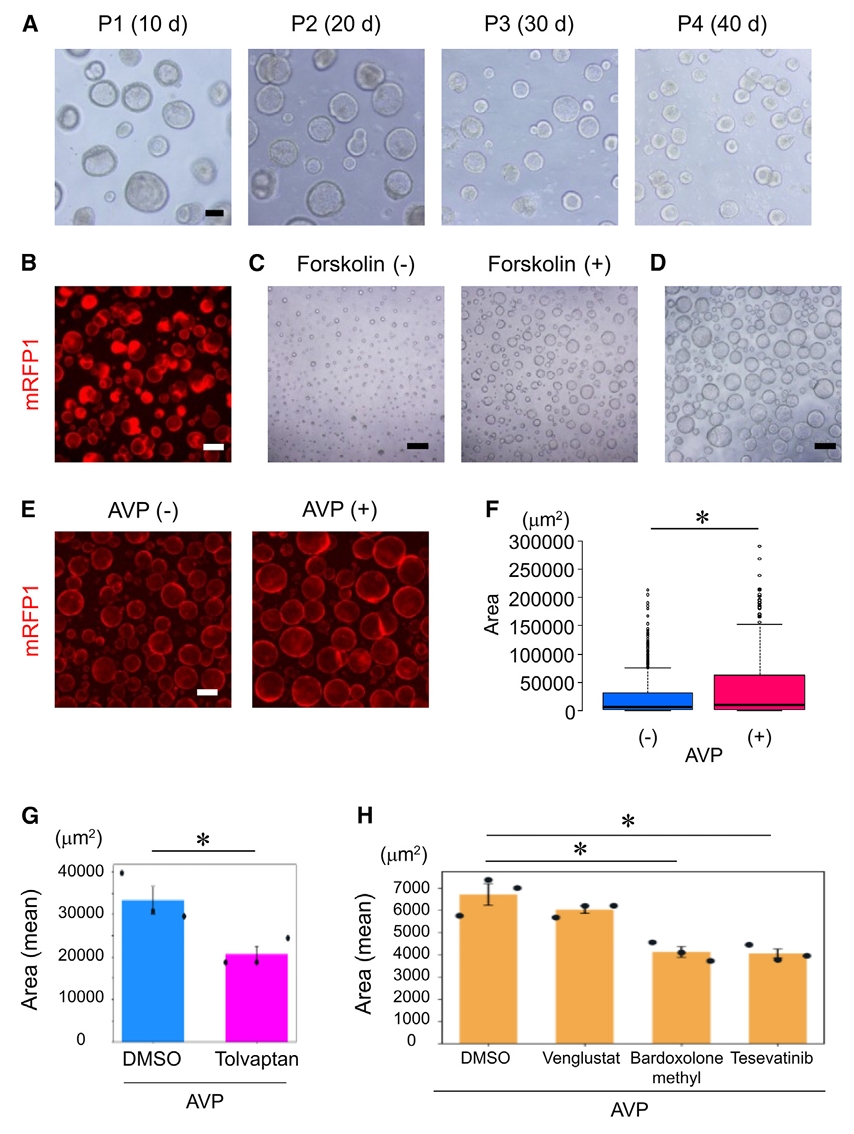
本研究针对常染色体显性多囊肾病(ADPKD)中囊肿主要起源于集合管的特点,通过建立人iPSC来源的输尿管芽尖端细胞(集合管胚胎前体)的扩增培养体系,成功推进了集合管类器官的发育阶段。研究表明,源自PKD1-/- iPSC的所有集合管类器官均自发形成多个囊肿,阐明了囊肿发生的起始机制。进一步鉴定出视黄酸受体(RAR)激动剂作为候选药物,在体外抑制囊肿形成,并在ADPKD小鼠模型中验证了其治疗效果。该集合管囊肿模型为理解ADPKD疾病机制和药物研发提供了重要工具。
(点击图片可放大)
图4-1. 抑制囊肿增大的化合物高通量筛选平台的建立。通过建立集合管囊肿传代培养体系,实现了囊肿的稳定扩增与高通量筛选。利用该平台验证了精氨酸加压素可显著诱导囊肿增大,而ADPKD临床用药托伐普坦可有效抑制该效应。进一步对多种候选化合物进行筛选,鉴定出具有抑制囊肿增大潜力的化合物,为ADPKD药物发现提供了可靠的高通量筛选平台。
(点击图片可放大)
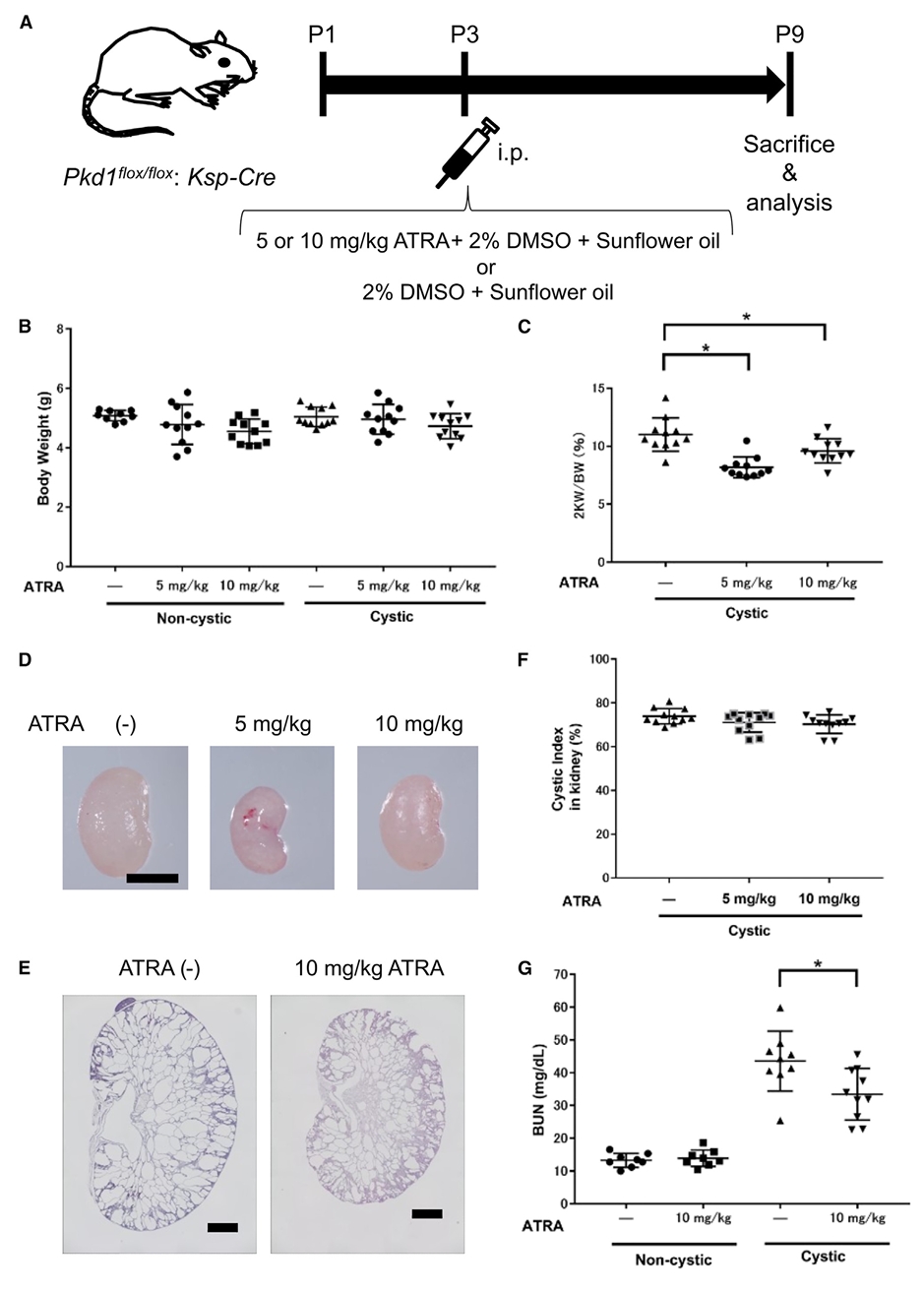
图4-2. 全反式维甲酸对ADPKD模型小鼠的治疗效果。在Pkd1条件性敲除的ADPKD小鼠模型中,腹腔注射全反式维甲酸可剂量依赖性地降低双肾重量与体重比值、减轻肾囊肿严重程度并改善肾功能指标血尿素氮水平,证实视黄酸受体激动剂在体内具有治疗ADPKD的潜力。
5
人常染色体隐性多囊肾病的器官芯片模型揭示药物发现的机械感应病理机制
文献名称:Organoid-on-a-chip model of human ARPKD reveals mechanosensing pathomechanisms for drug discovery
发表期刊:Science Advances (IF: 12.5)
发表日期:2022年9月23日
研究团队:美国麻省总医院、哈佛大学Ryuji Morizane团队
研究概要:
本研究将肾脏类器官与器官芯片技术相结合,构建了人常染色体隐性多囊肾病(ARPKD)模型。在流体流动条件下,PKHD1突变型类器官表现出临床相关的远端肾单位扩张表型。转录组学揭示了229条信号通路的变化,而静态模型无法检测到这些变化。研究鉴定出机械感应分子RAC1和FOS作为潜在治疗靶点,并经患者肾样本验证。基于此发现,在类器官芯片模型中测试了靶向RAC1和FOS的药物(包括两种FDA已批准药物和一种研究性新药),均可抑制囊肿形成。该研究强调了类器官芯片模型在阐明复杂疾病机制及药物发现中的巨大潜力。
(点击图片可放大)
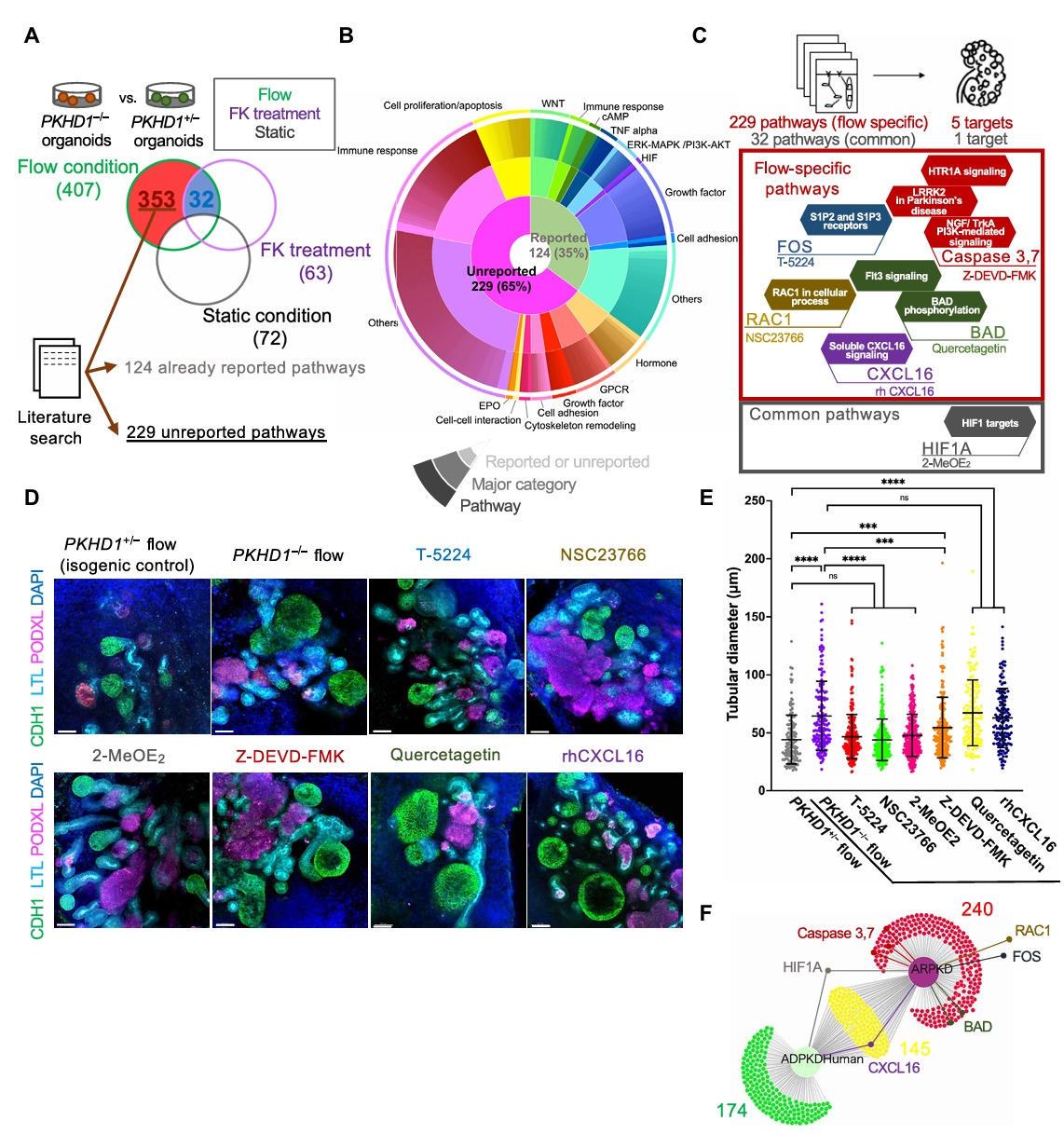
图5. ARPKD新型治疗靶点的鉴定及商业化化合物药物筛选。通过比较PKHD1突变型类器官在流体与非流体条件下的信号通路变化,筛选出与囊肿发生密切相关的机械感应通路。基于此筛选策略,鉴定出RAC1和FOS等作为ARPKD的潜在治疗靶点,并验证了靶向这些通路的多款商业化化合物可有效抑制远端肾小管的异常扩张,为ARPKD的药物发现提供了新的治疗靶点和候选药物。
6
细胞挤出式生物打印提高肾脏类器官的可重复性和结构可控性
文献名称:Cellular extrusion bioprinting improves kidney organoid reproducibility and conformation
发表期刊:Nature Materials (IF: 38.5)
发表日期:2021年2月刊
研究团队:澳大利亚默多克儿童研究所Melissa H. Little团队
研究概要:
针对目前肾脏类器官在应用中存在的变异性大、肾单位不成熟、通量低、规模有限等瓶颈,本研究应用挤出式三维细胞生物打印技术,实现了快速、高通量生成具有高度细胞数目和活力可重复性的肾脏类器官。研究证明,6孔或96孔板类器官生物打印可替代手工制备,并以氨基糖苷类药物相对毒性评价作为药物测试的概念验证。此外,三维生物打印能够精确调控类器官的生物物理特性,包括大小、细胞数目和构型,通过改变类器官构型显著提高了单位起始细胞数的肾单位产量,并可实现具有功能性近端肾小管节段的均匀肾组织片层的制造。该技术为干细胞来源的人肾组织的体外和体内应用提供了通量、质控、规模和结构上的改进。
(点击图片可放大)
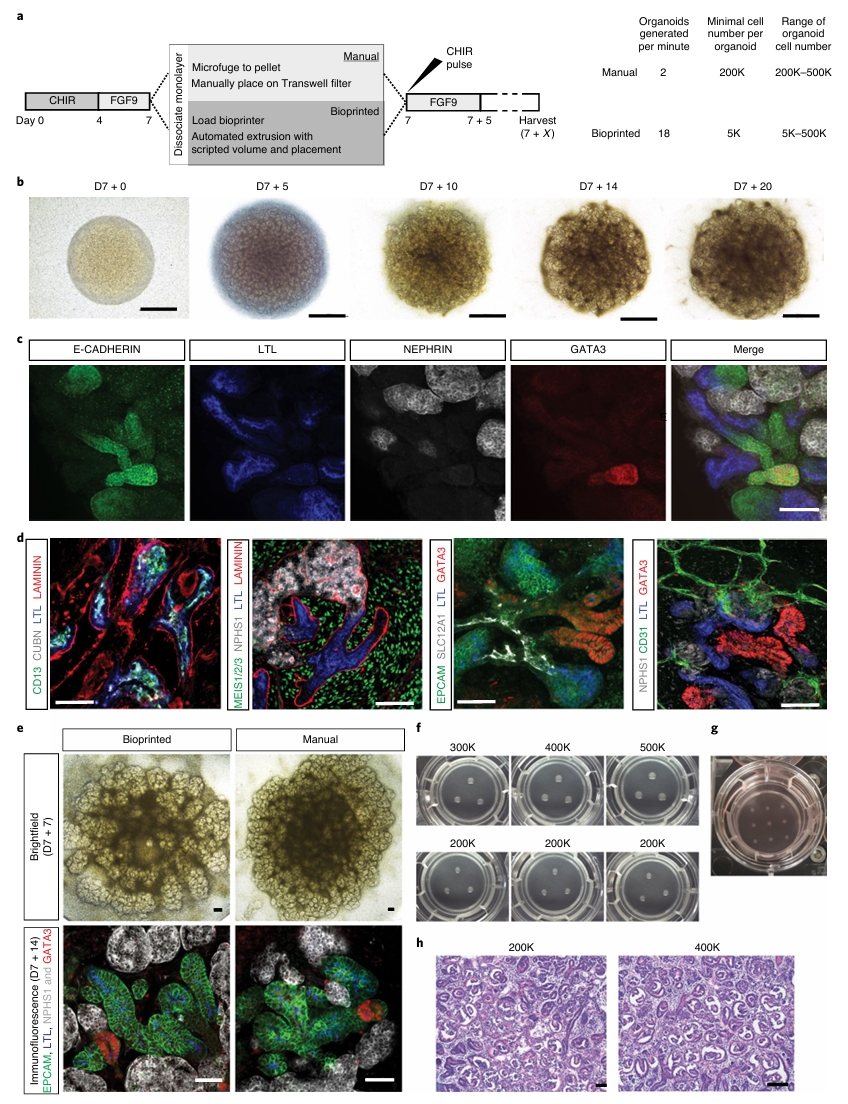
图6. 基于挤出式生物打印的高重复性人iPSC来源肾脏类器官的构建。通过在第7天中间中胚层细胞阶段进行自动化挤出式生物打印,可在数分钟内生成数百个细胞数目一致、活力均一的肾脏类器官。与手工制备相比,该技术显著提高了类器官的产量和可重复性。打印后的类器官经分化培养,可形成具有肾单位各节段(足细胞、近端小管、远端小管、集合管)及周围间质和内皮细胞的成熟肾组织,且通过精确调控起始细胞数目可实现类器官尺寸的标准化和规模化生产。
Part 01
肾脏类器官作为药物开发平台
的应用价值
传统模型在模拟人类肾脏药物反应和疾病进程方面存在局限。人诱导多能干细胞来源的肾脏类器官为药物开发提供了兼具人类遗传背景与组织复杂性的实验平台。前述研究展示了肾脏类器官在药物开发中的应用主要体现在以下几个方向:
药物发现:利用iPSC来源的集合管类器官和类器官芯片模型,成功构建了ADPKD和ARPKD的体外病理模型,有助于发现RAC1、FOS、自噬通路及视黄酸受体等治疗靶点,并筛选出多种抑制囊肿形成的候选化合物。
肾毒性评价:通过自动化3D成像与机器学习技术,建立了基于肾脏类器官形态学定量分析的高通量筛选体系,可用于药物肾毒性的高效评估。
药效评估:基于类器官体积分析的方法,能够从药物库中高效识别具有潜在肾保护作用的候选化合物,并在动物模型中验证了全反式维甲酸、米诺地尔等药物的体内疗效。
药物递送:通过非整合型DNA载体对iPSC进行基因修饰,构建了EPO过表达的肾脏类器官,实现了治疗性蛋白的稳定长期递送,为肾脏靶向药物递送策略的研发提供了新的技术路径。
Part 02
研究支持与服务
肾脏类器官作为药物开发平台,在药物发现、肾毒性评价、药效评估及药物递送等方面展现出独特价值,为药物研发提供了兼具人类遗传背景与组织复杂性的实验系统。
华津肾脏类器官Kidnioid®平台在此领域提供专业支持:
方案咨询:针对药物发现、肾毒性评价、药效评估及药物递送等研究需求,提供专业的技术方案建议。
实验实施:承接肾脏类器官培养、疾病模型构建、候选药物筛选、药效评价及体内验证等实验服务。
数据支持:提供完整的实验流程记录与标准化检测数据。
Part 03
平台优势
基于华津Kidnioid®平台在肾脏类器官培养及药物开发应用领域的技术积累,可为药物发现、肾毒性评价、药效评估及药物递送等相关研究提供标准化的实验模型和技术支持。
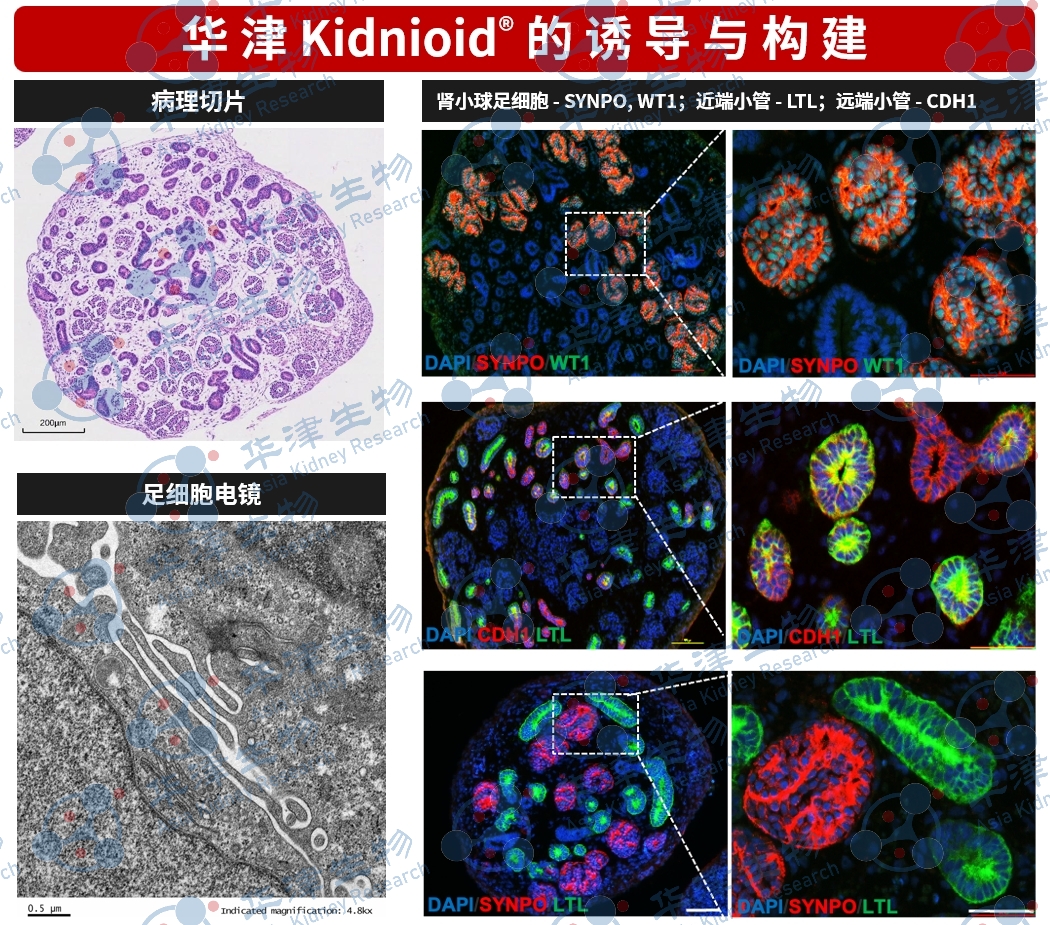
图注:经病理切片、电镜及免疫荧光鉴定,该肾脏类器官可观察到肾小球与肾小管结构,电镜下可见足细胞足突形态,免疫荧光染色显示足细胞、近端小管及远端小管的定位特征。
一、模型特点
基于人源细胞构建的肾脏类器官包含足细胞、近端小管和远端小管等细胞类型,能够在一定程度上保留人类肾脏的结构特征和基因调控网络。
该模型可用于肾毒性评价、药效评估、药物筛选及药物递送等药物开发关键环节,支持候选化合物的多维评估。
可用于肾脏疾病机制探索、候选药物筛选、药效与毒性评价以及新型递送策略验证等研究场景。
二、技术优势
周期较短:相比传统动物实验,类器官模型的构建与药物评价周期有所缩短。
模型稳定性较好:在标准化培养条件下,模型稳定性较高。
灵活性较强:可根据研究需求进行定制化调整。
检测体系适配性高:与常规分子生物学/细胞生物学方法高度兼容,可直接开展qPCR、Western blot、免疫荧光等检测,便于机制研究与多指标评价。
感谢您对本文的浏览。肾脏类器官作为前沿生物技术,不仅在疾病模拟、药物筛选和再生医学研究中展现出巨大潜力,也为精准医疗和新药研发提供了更可靠的平台。目前全球多家监管机构已将其纳入药物评价体系,标志着该技术正逐步走向标准化与应用化。如果您希望进一步了解肾脏类器官的技术细节、合作研究或商业应用,欢迎随时联系咨询:
商务支持 - 李老师 17276665437
技术支持 - 田老师 18843183823
我们期待为您提供专业服务与合作支持。

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

