引言

慢性肾脏病(CKD)全球高发,而现有治疗手段局限,亟需能够支撑新疗法研发的更具转化价值的模型。近年兴起的肾脏类器官(Organoids)与肾小管类器官(Tubuloids)为体外研究带来突破,但在规模化与结构可控性方面仍存在关键瓶颈。Radboud University Medical Center 的 J.G.J. Hoenderop团队在《Trends in Cell Biology》发表的综述系统梳理了肾脏类器官与肾小管类器官在内分泌、转运及滤过等方面的功能证据,并提出了融合单细胞多组学、器官芯片与生物打印等技术的工程化路线图。
这篇经典综述,系统整合了功能证据与面向成熟度、重现性与规模化的前瞻路线,至今仍为研究设计与平台优化提供高价值参照。
学术亮点
新兴模型的价值主张:人源肾脏类器官(Organoids)与肾小管类器官(Tubuloids)正崛起,有望克服传统体外模型的局限,更好再现人肾的功能表型。
应用取决于“像不像真肾”:两类模型的应用前景建立在其对肾脏段特异功能的逼真度之上。
已有功能证据版图:已被描述的能力涵盖段特异药物转运、对胞外微环境的响应、内分泌功能,以及电解质与水的功能性转运。
技术赋能的提质路径:多组学、机器学习、自动化高通量培养系统与器官芯片(Organ-on-a-chip)等工具可加速模型表征并提升成熟度。
面向转化的终极落点:上述进展将推动肾脏类器官与肾小管类器官走向个体化疾病建模与可依赖的前临床研究平台,实现从“能用”到“可转化”的跨越。
肾脏类器官与肾小管类器官一图总览
在进入功能与应用之前,作者先把两类模型的“来历—发育路径—细胞组成”进行了阐述,以建立读者对模型边界与适用场景的共识。图1用一张总览图并列呈现肾脏类器官(Organoids)与肾小管类器官(Tubuloids):前者由胚胎干细胞(ESCs)或诱导多能干细胞(iPSCs)在模拟肾发生的时序化生化/生物力学信号下三维分化、自组织,形成包含近端小管(PT)、粗升支(TAL)、远曲小管(DCT)与集合管(CD)等“分段肾单位样”结构,并可出现足细胞、囊壁上皮(PEC)、间质细胞与内皮祖细胞等,整体涵盖多达15种细胞类型,且改良方案已纳入更明确的集合管段;后者则是将成人肾组织或尿液中的成体干/祖细胞在三维条件下扩增,形成以成熟极化上皮为主、呈球形生长并突出修复与增殖机制的结构,既可来自人或小鼠,又能通过分化培养基富集特定段位(如PT、CD)。
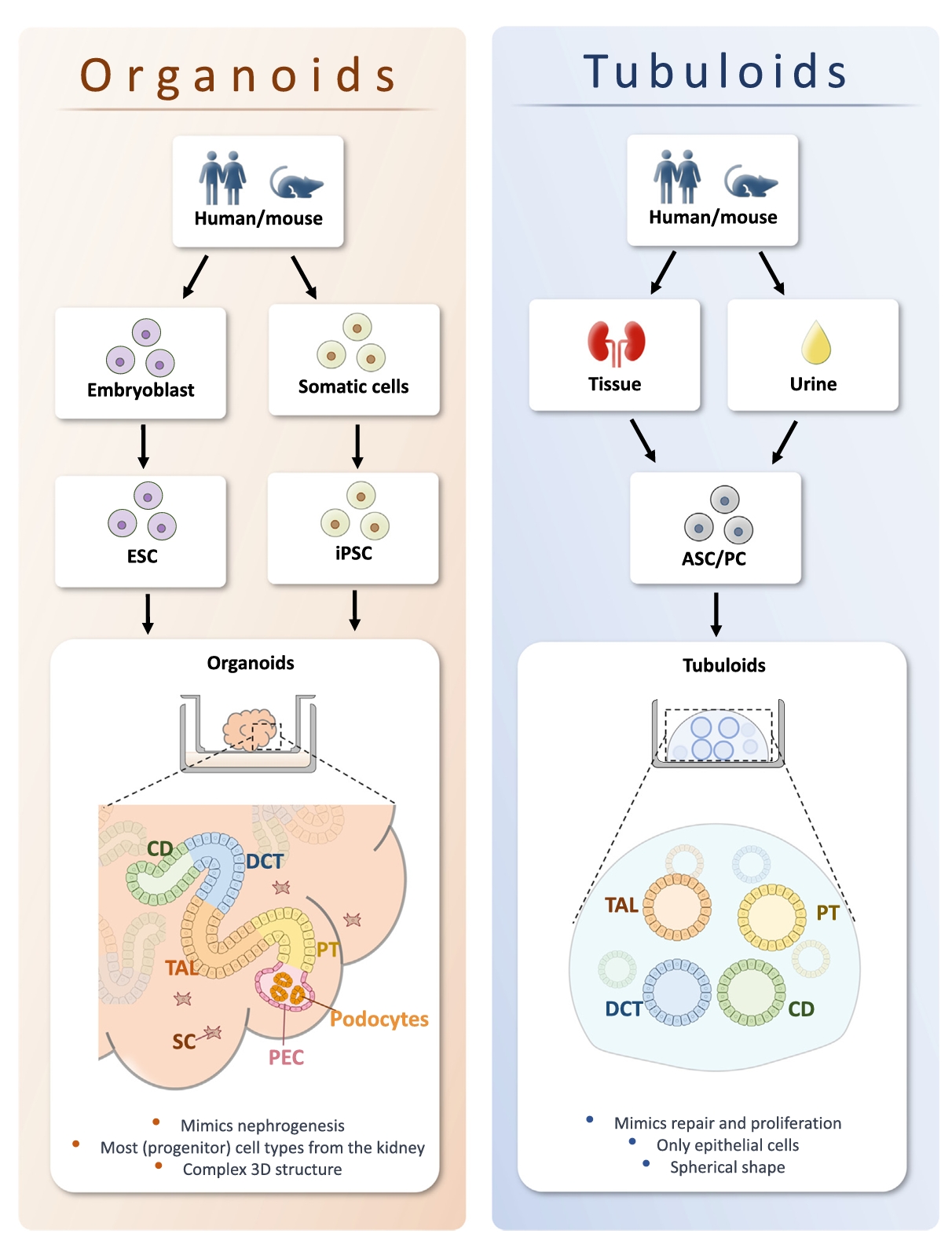
图1. 肾脏类器官和肾小管类器官的起源、发育和细胞组成概述。
两类模型的功能性研究总览
在介绍完肾脏类器官(Organoids)与肾小管类器官(Tubuloids)的来源、发育路径和细胞组成之后,作者顺势把镜头推进到“像不像真肾”的功能层面:作者以图2为主干,将各段位可被体外复现的功能进行成体系的归纳。
药物转运与肾毒性
近端小管(PT)通过OATs、OCTs等转运体清除内源性尿毒素与外源性药物。类器官在暴露马兜铃酸或顺铂后可上调KIM1,用于判定PT毒性;在肾小管类器官平台上,研究者以10种抗癌药进行时间依赖的毒性分级验证。类器官通过KIM1与细胞内ATP读出鉴定氨基糖苷的肾毒性,亦有将ATP/ADP生物传感器嵌入类器官以实现实时毒性评估的做法,并辅以DNA损伤读数评估对足细胞的影响。转运功能方面,类器官用荧光底物验证MDR1/OCT2的腔面蓄积(药理抑制可降低信号);在肾小管类器官中,荧光素摄取受OAT1抑制剂丙磺舒调控,且来自永生化PT细胞的胞外囊泡可促进PT成熟并增强OAT1活性;由iPSC类器官上皮衍生的肾小管类器官还能进一步向远段分化并表现出MRP功能。
对微环境(流动剪切)的生理响应
流动剪切是体内肾小管的重要力学组成。肾小管类器官在Mimetas三通道 OrganoPlate上可形成可灌注、极化且致密的上皮管道;基底侧表达OCT1/2、顶端表达MDR1,基底侧加入罗丹明-123后,顶端腔面出现荧光并可被OCT1/2/MDR1 抑制剂削弱。将类器官来源的PT细胞接入器官芯片同样可改善极性并提升 OCT2/OAT1/OAT3的表达与功能。长期培养的类器官在管段上增加且极化表达机械敏感通道PIEZO1;对微解剖的成熟管段实施灌流,可通过Fura-2记录到 PIEZO1介导的Ca²⁺信号。相对地,培养不足30天的类器官中PIEZO1表达低且不具极性,无法触发该信号,这说明成熟度可以决定流体剪切力的响应能力。
对刺激的生理响应与内分泌功能
尽管现有类器官缺乏成熟血管,但小鼠皮下移植后可与宿主血管连通并形成分子量选择性滤过:70kDa右旋糖酐可见于肾小球毛细血管丛与PT,10kDa可进入鲍曼囊,200kDa及白蛋白滞留于血管腔内;抑制类器官的钙释放会导致肾小球与足突发育异常,提示钙稳态对肾发生的重要性。肾小管类器官方面,囊性纤维化患者来源模型显示对福斯可林(升高cAMP、激活CFTR)的肿胀表型缺失,加入CFTR增效剂可恢复。类器官内可检测到肾素–血管紧张素–醛固酮系统(RAAS)多组分;福斯可林刺激促肾素合成与分泌,且移植后肾素可维持分泌约2个月。此外,类器官对甲状旁腺激素(PTH)的响应体现为Cyp27b1受调控:可检测PTH受体、PT段PKA底物磷酸化增强、Cyp27b1 mRNA上调,并生成1,25-二羟维生素D;通过药理干预可上调Cyp27b1并相应提高产物水平。
电解质与水转运
在类器官中,单细胞膜片钳记录揭示远端细胞存在K⁺电流以及Na⁺吸收。于Transwell膜系统培养的集合管(CD)类器官可检测跨上皮电阻(TEER)、电压与电流;阿米洛利(ENaC 抑制剂)使TEER上升并消除跨上皮电压/电流,而醛固酮上调ENaC活性。Tubuloids经向CD方向的诱导分化后,AQP2在去氨加压素类似物刺激下发生顶端转位;在小鼠及类器官衍生的Tubuloids中,放射性钠示踪显示阿米洛利敏感的ENaC介导Na⁺ 摄取。
蛋白转运、蛋白折叠与酶活性
生物打印的肾类器官在成熟度与可重复性方面表现更好,并在PT细胞中显示TRITC-白蛋白摄取,作为蛋白转运的功能体现。患者来源类器官可重建MUC1 肾病(MKD)的蛋白错误折叠/聚集表型:MUC1突变导致蛋白滞留于早期分泌通路囊泡,该现象在小鼠模型中得到验证,并据此筛得候选小分子用于表型矫正。针对法布里病(GLA基因突变),患者iPSC-类器官显示Gb-3在足细胞中累积并导致功能减退,这说明类器官也可以适用于酶缺陷–病理表型的体外研究。
迈向更具功能性的体外“肾”
肾类器官的分化仍存在批内/批间变异、离靶细胞与未分化残留等问题,整体状态更接近胎肾且缺乏血管化;成人肾与胎肾在OAT/OCT等通路的表达差异也限制部分应用。通过增强中肾定向的分化方案,可提高PT成熟(OAT1/OCT2上调)并改善药物响应。肾小管类器官更接近成人上皮,但仍需外源刺激拉近与人肾表达谱的差距;引入间质细胞、内皮细胞等以促进小管–间质串扰有望进一步提升成熟度。规模化亦是关键约束:人肾约100万个肾单位,而典型分化方案每个类器官约100个;此外,组织空间排布随机与腔侧向内导致顶端/基底外侧可及性受限。为此,作者提出了以多组学结合机器学习优化分化决策,结合器官芯片/合成水凝胶重建微环境,并叠加生物打印、生物反应器与自动化,在成熟度、极性与可重复性上实现可验证的改进,推动在体外更可靠地重建肾脏功能。
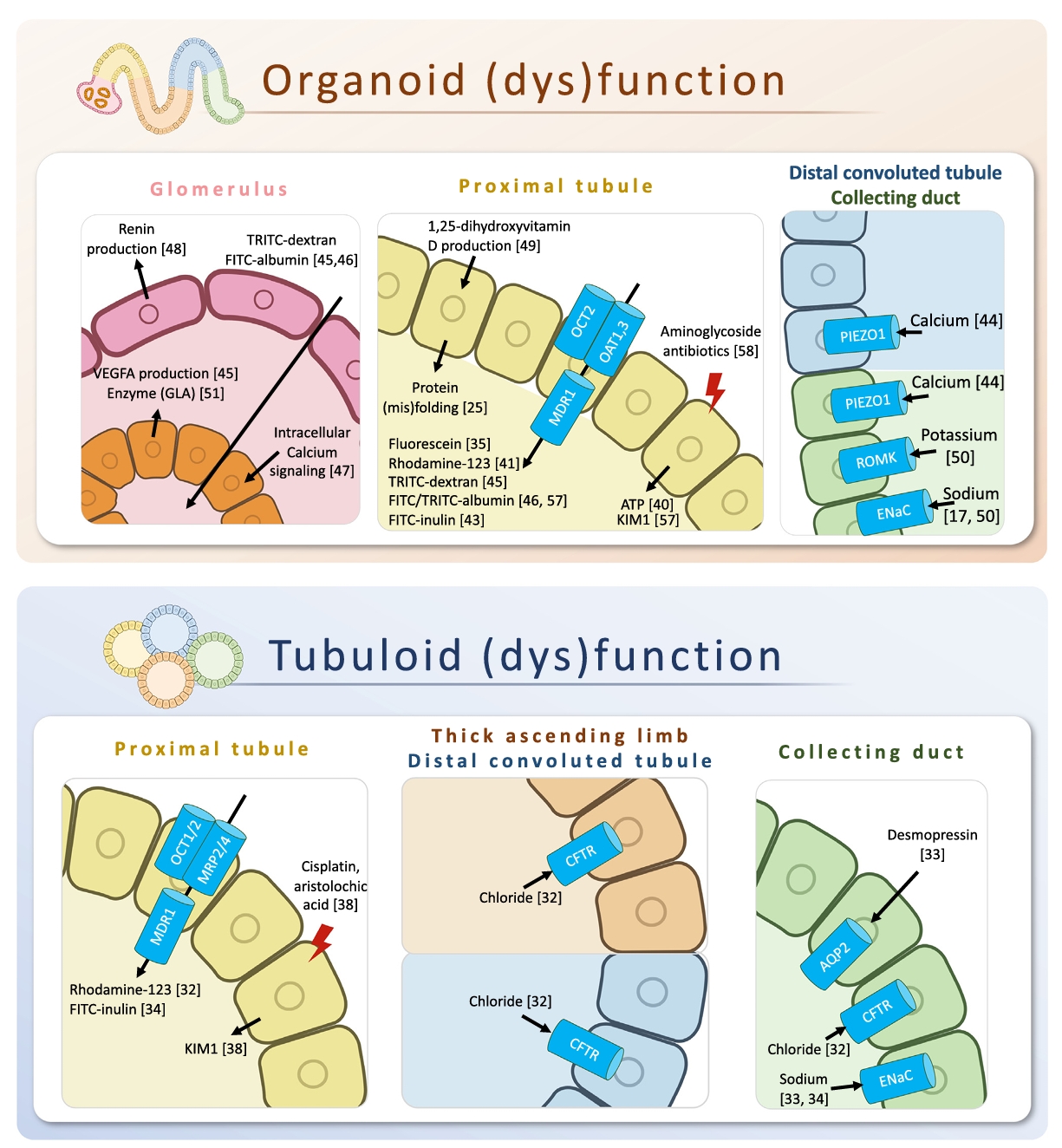
图2. 在肾脏类器官和肾小管类器官模型中重现的节段特异性肾(dys)功能。
利用先进工具克服类器官培养的局限
随着肾脏类器官与肾小管类器官研究的快速发展,科学家们正积极探索多学科融合的方法,以克服当前模型在成熟度、可重复性与规模化培养方面的瓶颈。图3总结了多种先进技术的应用路径——包括计算工具、生物工程策略以及活细胞识别与分离方法——这些创新手段的整合为实现“生命化”的体外肾组织培养奠定了基础。
计算与多组学工具
借助单细胞转录组学与空间组学等前沿技术,研究者能够深入解析类器官中不同细胞的发育轨迹和转录状态,从而发现影响特定分化方向的关键分子通路。例如,通过单细胞转录组学手段,成功鉴定并抑制了导致非目标神经细胞生成的信号途径,使这类脱靶细胞比例减少了约90%。此外,多组学整合分析在器官发育研究中展现出巨大潜力,可为优化类器官分化协议提供数据驱动的指导。通过机器学习与知识图谱的构建,这些复杂数据能够转化为预测模型,为培养体系的参数调控与环境优化提供智能化参考。
生物工程策略
细胞的增殖与分化在很大程度上受生物力学信号的调控,因此重建接近体内环境的培养系统至关重要。利用合成水凝胶可以调控材料的弹性与刚度,同时嵌入生长因子或特定空间结构,为类器官提供类生理支持。进一步地,将水凝胶与器官芯片结合,能够实现多细胞间动态相互作用与流体剪切力模拟。此外,生物打印、生物反应器及自动化培养系统的引入,使得类器官的培养更加标准化与可扩展。结合机器人技术与机器学习算法,可实现对培养过程的实时监测、自动化维持与高通量分化指导,从而显著提升实验的可重复性与效率。
活细胞识别与特定细胞类型的分离
肾脏类器官与肾小管类器官内包含多种异质细胞群体,因此准确识别与分离特定细胞类型是深入研究的重要前提。当前可通过报告基因细胞系和荧光标记凝集素实现细胞可视化标记,从而在不显著破坏细胞间连接的情况下进行筛选。结合微切割技术与大颗粒分选系统,可高效分离单个细胞或小群体细胞。分离后的细胞群体可重新进入优化培养体系,用于验证特定细胞的功能、发育潜能及其在整体组织中的作用。
技术整合的前景
图3所展示的多维策略体现了计算工具、生物工程与细胞操控三者的深度融合。这种多学科协同为肾脏类器官与肾小管类器官体系提供了更完善的研究框架。通过AI驱动的培养条件预测、生物材料构建的微环境再现、以及特定细胞群的精准操控,研究者有望进一步提升体外肾组织的成熟度、特异性、可重复性与可扩展性。从长远来看,这些进展将加速实现真正具备生理功能的“生命化”肾组织,为疾病模型构建与再生医学应用奠定基础。
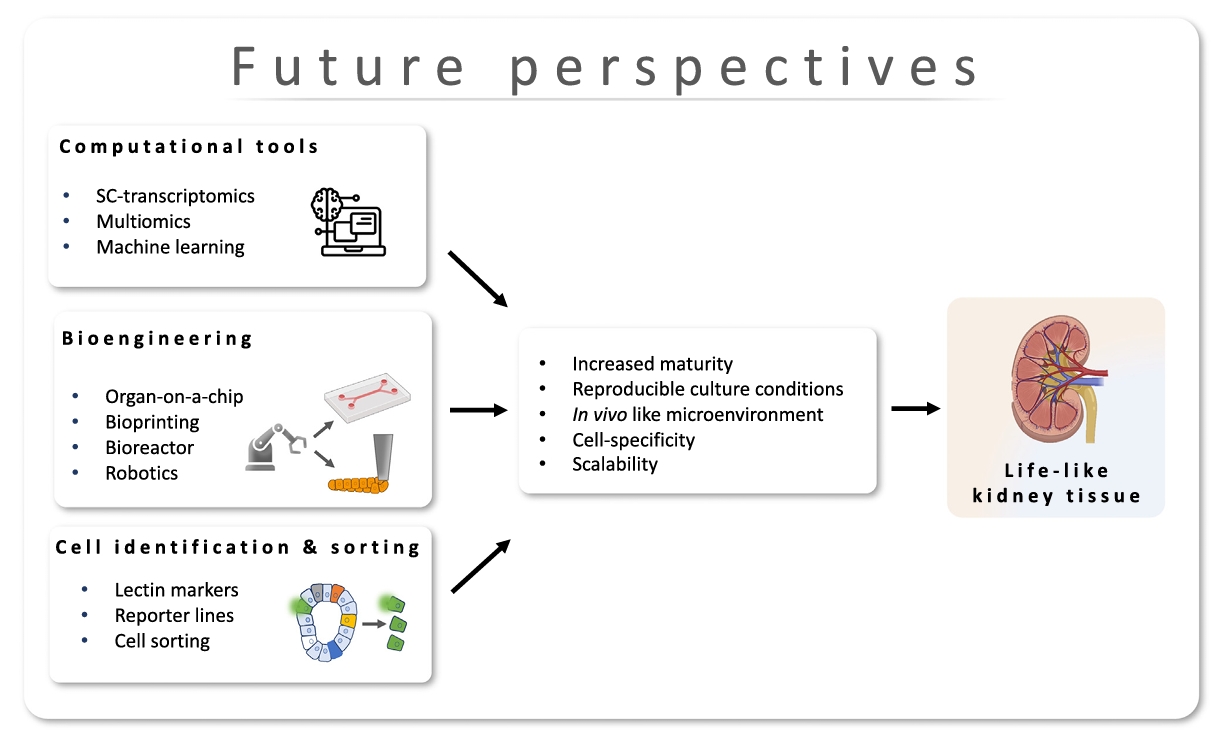
图3. 使用先进的工具来克服目前在类器官和肾小管培养中的限制,从而能够在体外发育成类似生命的肾组织。
总而言之,肾脏类器官与肾小管类器官正在补位传统永生化细胞系与动物模型的不足,已在多层面重现实/功能:移植后表现出分子量选择性肾小球滤过;在体外呈现 RAAS 调控、PTH-Cyp27b1-维生素D轴等内分泌活动;并能读出药物与溶质转运(OAT/OCT/MDR/MRP)、损伤与肾毒性(KIM-1、ATP/ADP、DNA 损伤)、以及电解质/水通道功能(ENaC、ROMK、BKCa、AQP2)。生物打印、器官芯片与单细胞转录组学等技术的引入,进一步提升了模型的表征深度与功能可测性。
同时,成熟度、重现性与规模化仍是落地应用的关键瓶颈。面向这些限制,作者提出以多组学与机器学习优化分化与培养条件,结合合成水凝胶与器官芯片重建在位微环境,并辅以生物打印、生物反应器与自动化实现标准化与高通量。整体目标是增强(失)功能可复现性与可靠性,推动肾脏类器官与肾小管类器官在疾病建模、药物筛选/肾毒性评估,以及个体化与再生医学中的转化应用。
参考文献:
Dilmen, E et al. “Advancements in kidney organoids and tubuloids to study (dys)function.” Trends in cell biology vol. 34,4 (2024): 299-311. doi:10.1016/j.tcb.2023.09.005

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

