
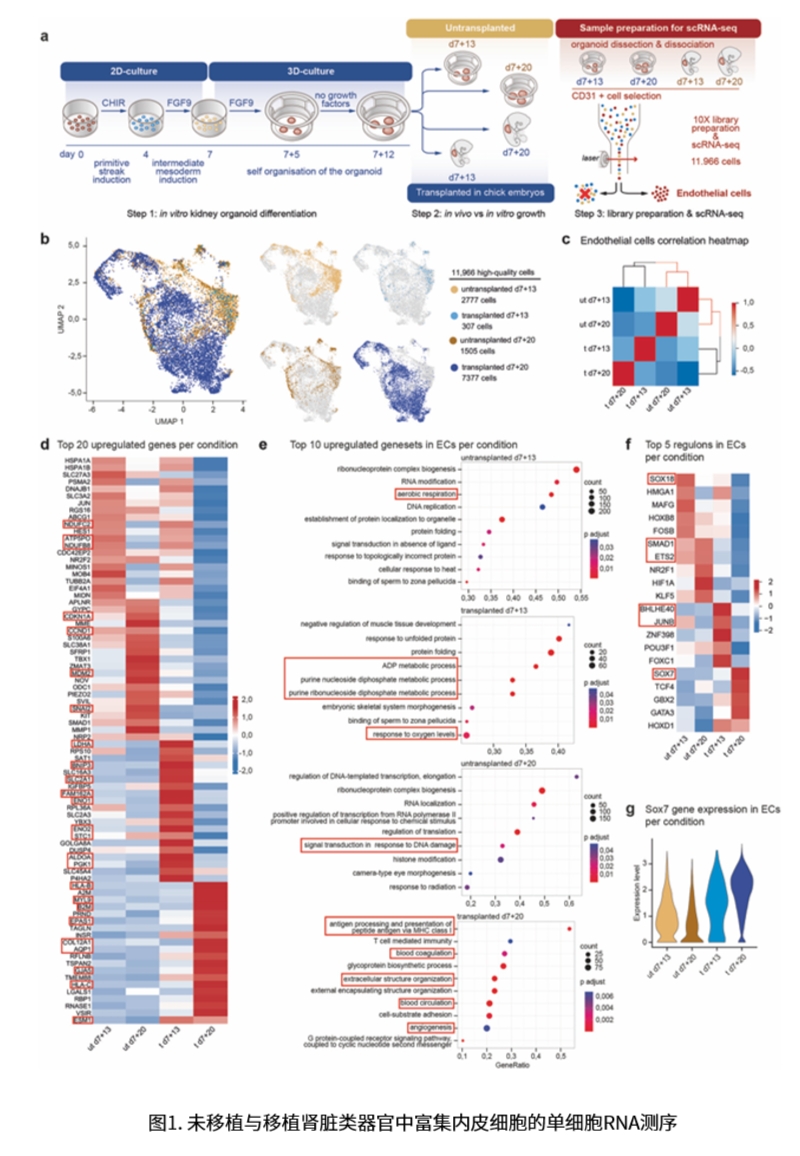
人源iPSC诱导的肾类器官在体外培养中缺乏功能性血管系统,限制了其成熟和应用。已有研究发现,移植进入鸡胚可促进血管化,但其分子机制尚不明确。本研究利用单细胞转录组测序(scRNA-seq)对 ~12,000 个肾类器官来源的内皮细胞(ECs)进行了系统分析,揭示了移植对内皮细胞组成、代谢特征和动脉分化的重大影响。
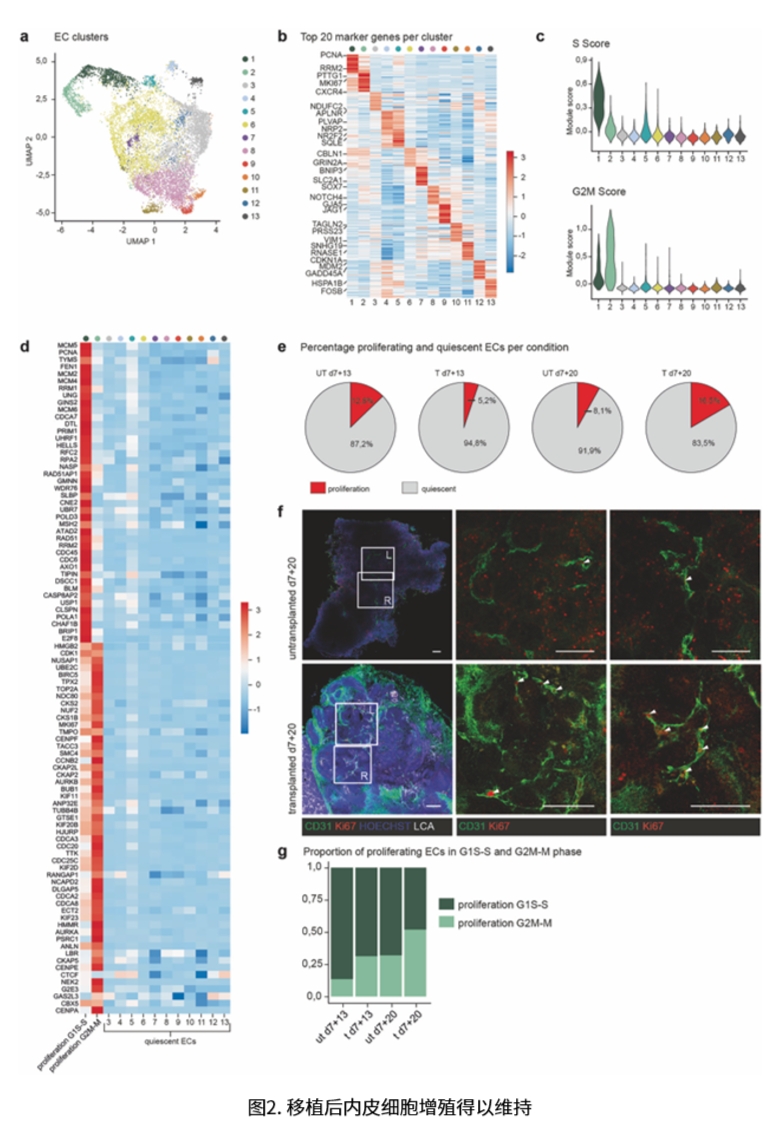
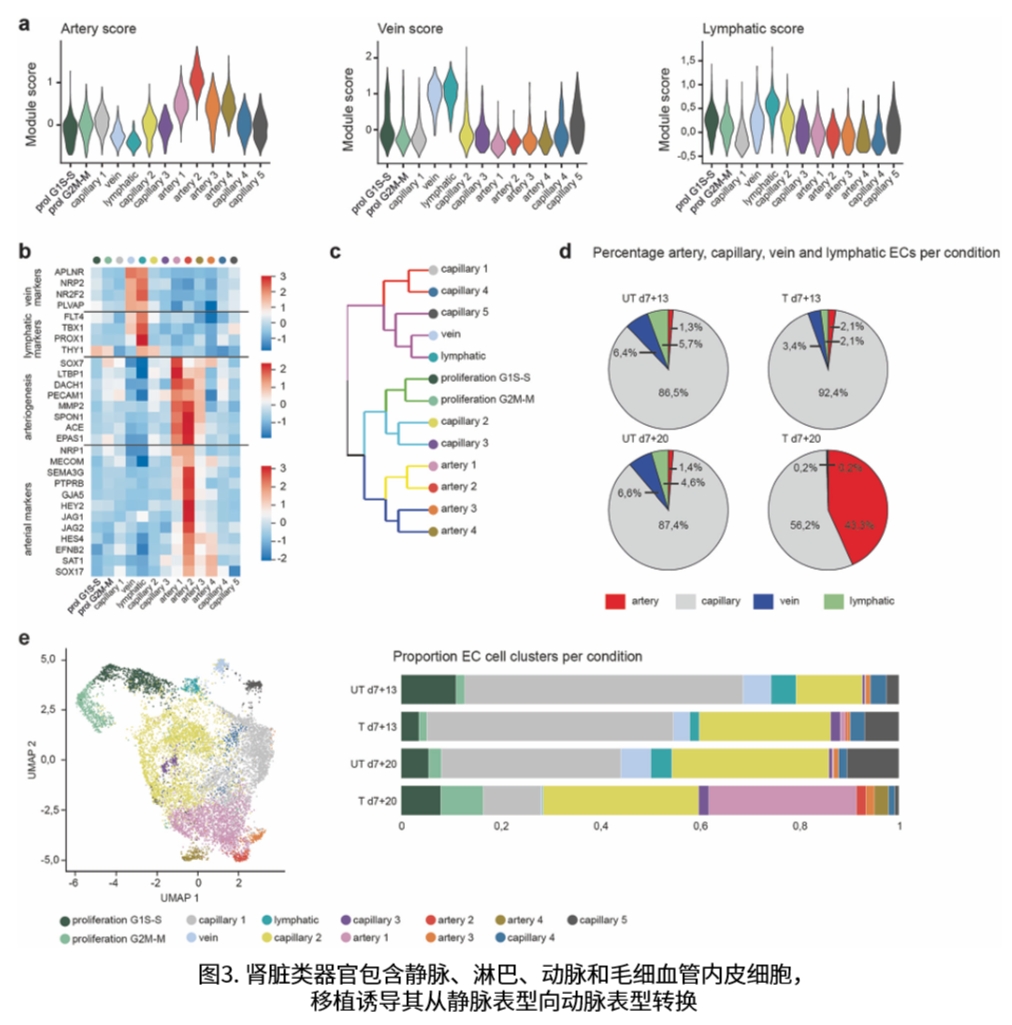
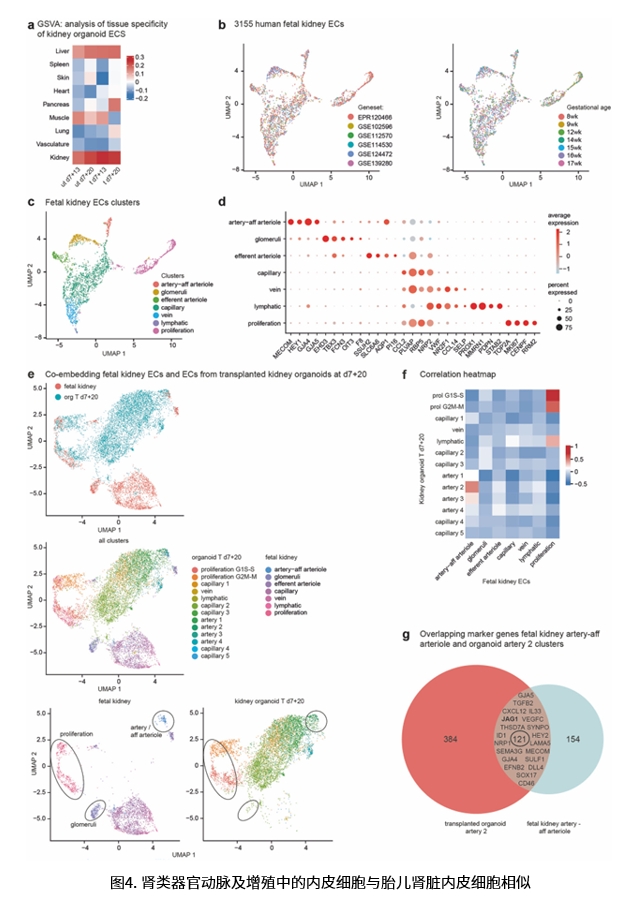
研究表明,体外培养的肾类器官ECs稀少且逐渐凋亡,而移植后不仅维持了人源ECs的存活,还显著促进了其增殖,并发生了从静脉型向动脉型的表型转换。其中一个移植特异性的动脉亚群表现出与人类胎儿肾脏入球小动脉内皮细胞高度相似的转录特征,并富集了与血流剪切力相关的基因和Notch信号通路。SOX7等转录因子被鉴定为潜在的关键调控因子,为改善类器官血管化提供了新的靶点。
创新点
- 首次在近 12,000 个类器官ECs上进行系统性单细胞转录组研究,全面解析了移植前后ECs的异质性。
- 移植后的ECs由以氧化磷酸化为主转向糖酵解和缺氧相关通路,符合血液灌注与低氧环境下的适应性反应。
- 移植8天后,类器官ECs中约 43% 具备动脉表型,呈现与胎儿肾脏入球小动脉 ECs 高度相似的转录特征,这是体外培养无法实现的。
- SOX7在移植后ECs中显著上调,驱动血管生成与动脉分化,提示其可作为未来体外优化血管化的重要靶点。
- 移植类器官ECs显著上调与层流剪切力相关的基因(如JAG1、KLF2、SMAD6/7),证实血流灌注是促进动脉化和组织特异性分化的核心机制。
- 结果提示通过调控血流、低氧和关键转录因子(如SOX7),可在体外条件下增强肾类器官的血管化和成熟度,为疾病建模、药物筛选和再生医学应用奠定基础。
参考文献:Koning et al. NPJ Regenerative medicine vol. 10,1 32. 1 Jul. 2025


