近年来,肾类器官作为新兴工具,已成为模拟损伤修复过程的强大平台。然而,如何将肾类器官与其他细胞类型共培养以评估特定信号调控通路,仍需要更多创新的办法。而就在今年初,发表于《Journal of the American Society of Nephrology》上关于T调节细胞(Tregs)的研究给出了一个全新的思路。本研究独创了kidney organoids (KDOs)低氧共培养系统,结合转录组分析和小鼠缺血再灌注损伤(IRI)模型,揭示ST2+ Tregs通过分泌amphiregulin(AREG)保护肾前体细胞,为AKI免疫修复研究提供了宝贵范式。
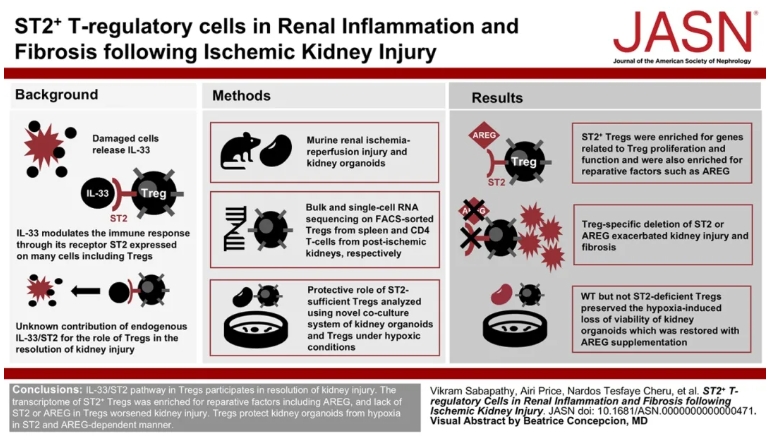
(点击查看大图)
【脾脏Tregs转录组分析揭示ST2调控的独特基因签名】
为阐明ST2在Tregs中的基础调控机制,作者从脾脏分离ST2-high、ST2-low和ST2敲除(KO)Tregs,进行bulk RNA测序分析。这是因为脾脏Tregs代表稳态下的“原型”,能反映其在损伤前的特性。
结果显示,三组Tregs的基因表达呈现明显聚类差异:ST2-high和ST2-low更相似,而ST2 KO独立成簇。主成分分析(PCA)和欧氏距离聚类确认样本间差异稳定。差异表达分析揭示ST2-high vs ST2 KO上调基因包括修复因子AREG和GDF15,以及Treg功能相关基因如Ctla4、Il10、Tgfb1、Cd73、Tnfr2和Cd44;下调基因包括Cd39、Nrp1、Sell和Ghrl。其中,Areg在ST2-high Tregs表达最高,Gdf15在ST2-high和ST2-low相似但显著高于KO组。这表明ST2调控Tregs的增殖、免疫抑制和组织修复相关基因表达。
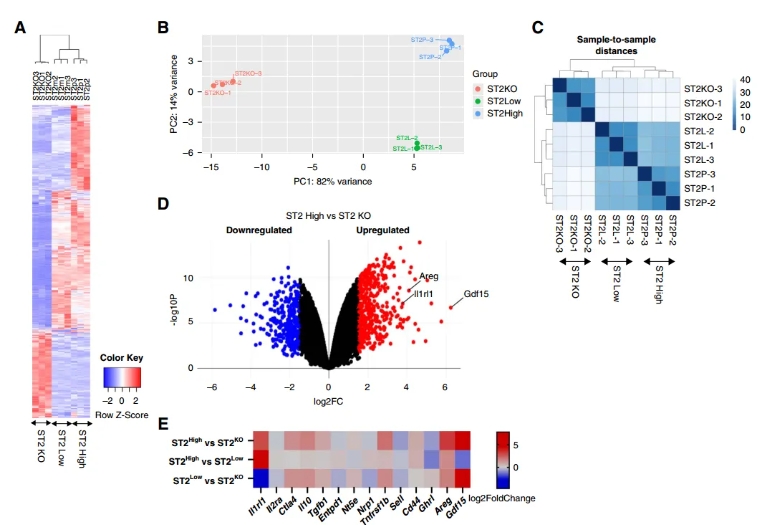
图1a:无监督聚类热图展示三组Tregs基因表达模式;图1b:PCA二维图分离样本组;图1c:样本间欧氏距离热图;图1d:火山图突出差异基因;图1e:选定Treg相关基因表达变化。(点击查看大图)
【GO和KEGG通路分析鉴定ST2调控的功能路径】
鉴于这些差异基因提示ST2影响Tregs的功能路径,作者进一步进行GO和KEGG通路分析,以识别潜在生物过程。这一步基于转录组数据,旨在连接基因表达与生理功能。
GO分析显示,ST2-high Tregs相对于KO组上调过程包括细胞周期正调控、细胞增殖、细胞因子介导信号和炎症响应;下调过程包括蛋白质泛素化、核质转运负调控和IFN-β产生。KEGG通路分析类似,上调路径涵盖EGFR、Jak-STAT、T细胞受体(TCR)、NF-κB和细胞周期;下调路径包括Fas信号、炎症小体和TLR信号。ST2-high vs ST2-low的比较进一步突出NF-κB上调和转录负调控下调。这些结果强化了ST2促进Tregs激活和修复功能的假设。
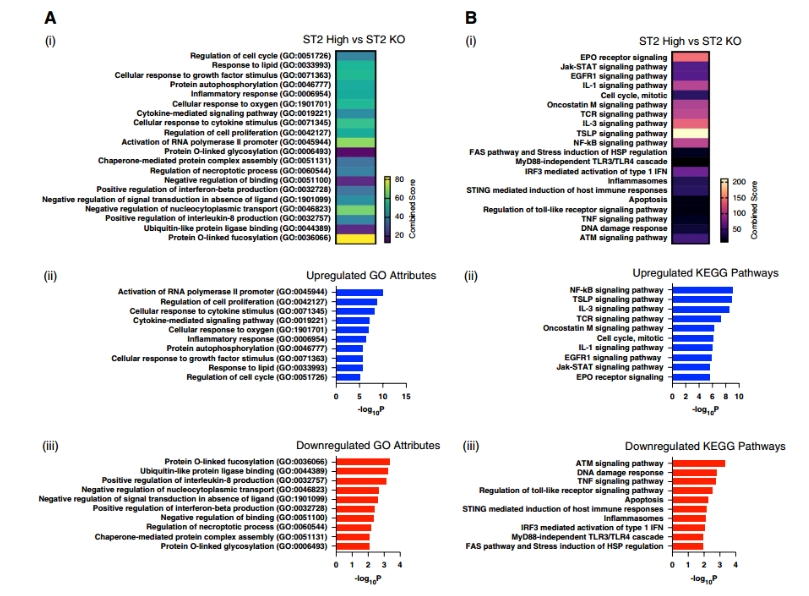
图2a:GO属性热图与上/下调条形图;图2b:KEGG路径热图与上/下调条形图。(点击查看大图)
【IRI模型验证Treg中ST2缺失加剧肾功能衰退】
基于转录组揭示的修复基因富集(如Areg),作者假设ST2缺失将削弱Tregs在肾损伤中的保护作用。为此,他们生成Treg特异性ST2敲除小鼠,并采用IRI模型验证体内效应。体外抑制实验首先确认ST2+ Tregs对T细胞增殖的抑制更有效。
双侧IRI模型显示24小时后肾功能损失相似,表明ST2在急性损伤抑制中非关键。但单侧IRI模型(14天后移除对侧肾)结果显示,敲除组血浆肌酐和血尿素氮(BUN)水平显著升高,提示ST2+ Tregs对损伤后期恢复至关重要。
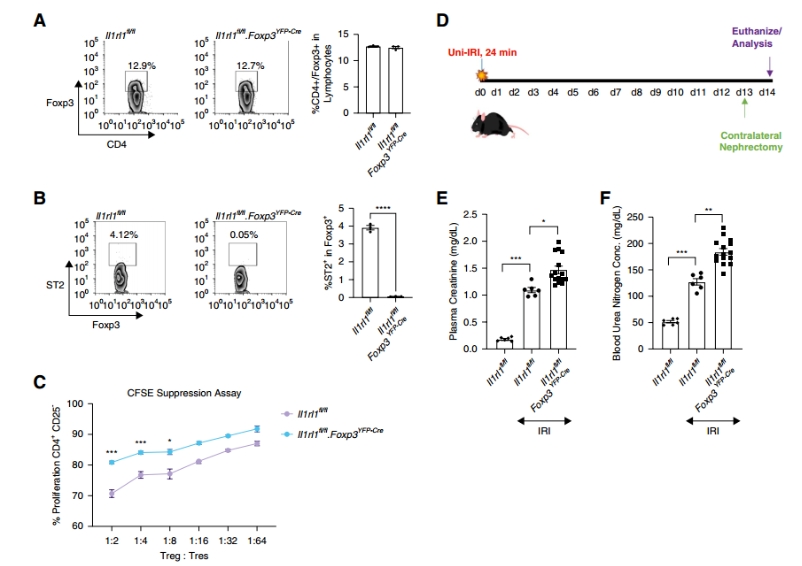
图3a–b:脾Tregs流式分析确认敲除效率;图3c:体外抑制实验;图3d:单侧IRI实验流程;图3e–f:肌酐和BUN水平对比。(点击查看大图)
【组织学分析确认ST2缺失加剧肾损伤和纤维化】
为评估结构变化,作者进行组织学分析,以连接功能衰退与病理表现。这一步基于功能指标,旨在量化损伤程度。
结果显示敲除组肾小管坏死、铸型形成、扩张和间质白细胞浸润更严重,损伤评分更高。肾损伤标志物Kim1和Ngal mRNA表达上调。Masson三色染色量化显示敲除组纤维化面积增加,qPCR确认纤维化标志物Col1a1、Col3a1、Acta2(Sma)和Vimentin(Vim)表达升高。这证实ST2缺失加剧肾损伤和纤维化。
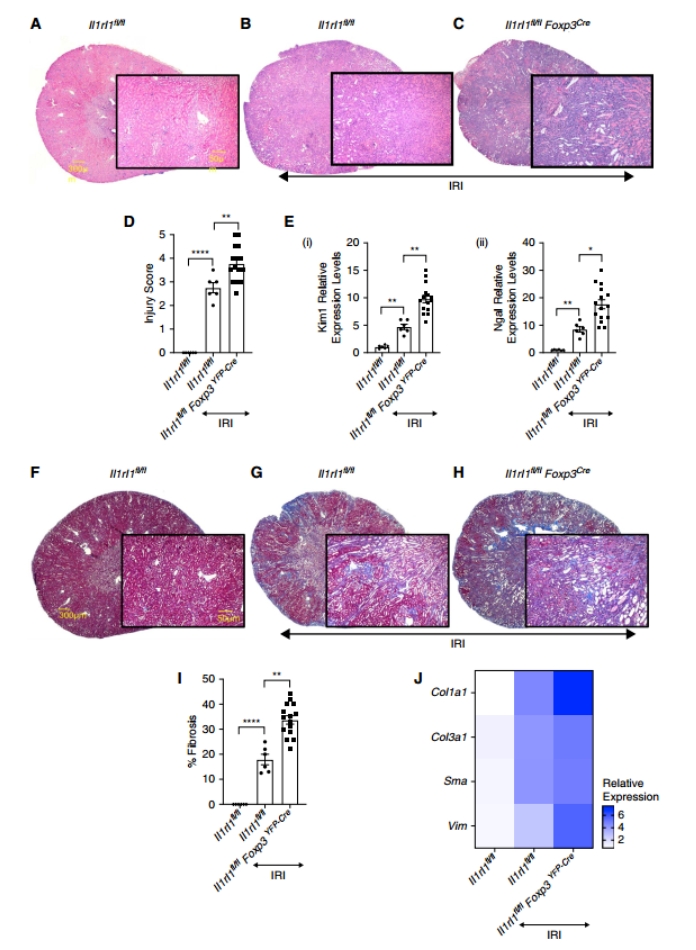
图4a–c:H&E染色图像;图4d:损伤评分;图4e:Kim1和Ngal表达;图4f–h:Masson染色图像;图4i:纤维化量化;图4j:qPCR热图。(点击查看大图)
【免疫细胞动态分析揭示ST2缺失的炎症机制】
因为观察到病理变化提示炎症加剧,作者进一步分析了免疫细胞动态,以探讨ST2缺失的免疫机制。这一步基于组织学结果,旨在揭示细胞水平变化。
流式细胞术显示IRI后Tregs在血液和肾脏增加、在脾脏减少;敲除组肾中性粒细胞浸润显著增多。脾CD4+ T细胞中IFNγ和TNFα产生增加,IL-10产生减少,IL-4无明显差异。免疫荧光证实敲除组肾间质中性粒细胞更多。这表明ST2+ Tregs通过抑制促炎响应维持肾稳态。
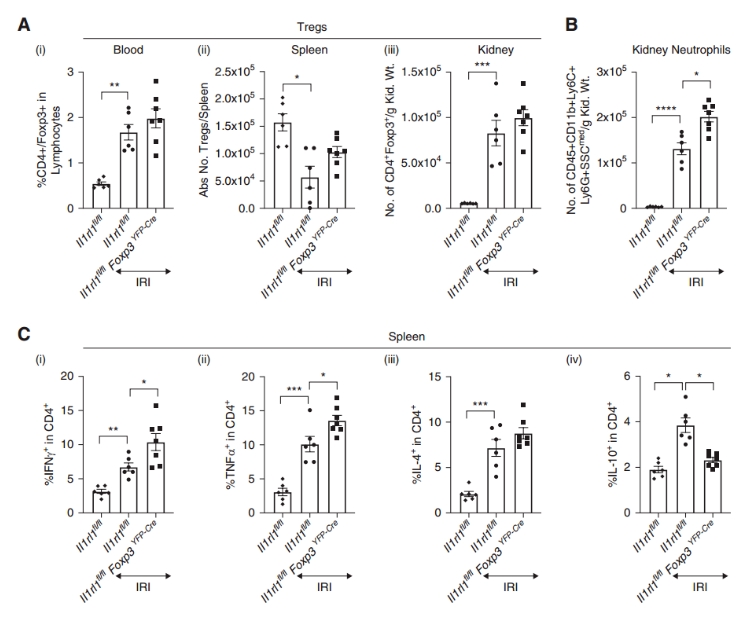
图5a:Tregs在血/脾/肾分布;图5b:肾中性粒细胞计数;图5c:脾CD4+细胞细胞因子产生。(点击查看大图)
【KDO共培养模型证实AREG依赖的保护机制】
体内结果暗示ST2+ Tregs可能通过分泌因子(如转录组中富集的AREG)发挥保护作用,但具体机制需体外验证。
为此,作者开发了一个独创的体外共培养系统,使用同系KDO和Tregs模拟低氧损伤环境。这项创新是论文的核心亮点,因为此前并无针对KDO与Tregs的标准化共培养协议,作者通过系统优化填补了这一空白。该模型的重要性在于,它直接桥接了体内观察与细胞水平机制,证明了ST2+ Tregs在肾修复中的关键作用,为未来药物筛选和免疫疗法提供了可靠的体外平台。
首先,作者从C57BL/6J小鼠胚胎干细胞生成KDO,通过优化分化协议,确保KDO表达肾标志如Nephrin、Pax8、Sox9和Lgr5,并具备初期肾结构特征。
其次,他们测试多种培养介质(如RPMI、EB Basal和α-MEM),发现α-MEM(补充核糖核苷酸、脱氧核糖核苷酸、L-谷氨酰胺和10% FBS)在维持KDO和Tregs活力方面最佳(图6a)。
然后,使用0.4μm Trans-well系统分离细胞:上室放置约10^5个从脾脏分离的Tregs,下室放置约50个KDO,避免直接接触但允许分泌物交换(图6b i)。为模拟IRI下的低氧损伤,他们将系统置于密封低氧室(1% O2、5% CO2、氮气平衡,37°C),维持6小时低氧后,切换到正常氧(20% O2)再氧合1小时。KDO活力评估结果显示低氧导致活力显著下降,但与ST2+ Tregs共培养可保护活力,而ST2 KO Tregs无效(图6b ii)。
进一步,作者收集Tregs的过滤上清(FSM),ELISA检测显示野生型FSM中AREG水平更高(约40 pg/ml);使用ST2 KO FSM时活力未恢复,但补充重组AREG后恢复正常,证实AREG依赖机制(图6c)。这一独创模型不仅验证了分泌物的关键作用,还突出了其在肾损伤研究中的潜力。
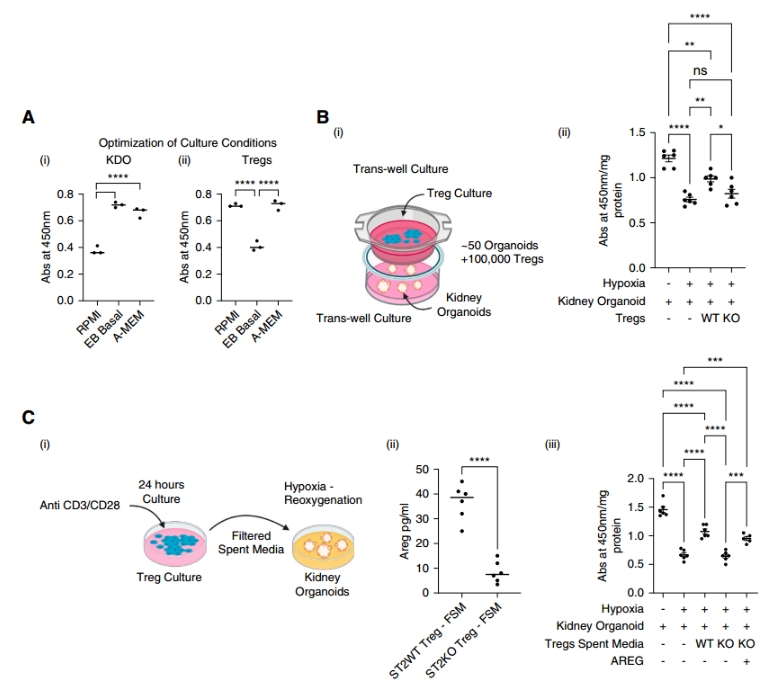
图6a:培养介质优化对比;图6b:Trans-well系统示意图及活力评估;图6c:FSM中AREG水平、补充AREG的活力恢复。(点击查看大图)
【AREG敲除模型验证其在体内的必要性】
为确认AREG在体内的必要性,作者生成Treg特异性AREG敲除小鼠,并重复IRI实验,以验证其对肾损伤的贡献。这一步基于KDO结果,旨在桥接体外机制与体内效应。
敲除组显示血浆肌酐、BUN和损伤评分升高,组织学损伤更严重。qPCR显示Kim1、Ngal和纤维化标志物上调。Tregs在血液、脾脏和肾脏数量减少;脾CD4+ T细胞中TNFα产生增加,IL-10和IL-4产生减少,IFNγ略升。这与ST2缺失现象相似,强调AREG在Treg稳态和保护中的核心作用。
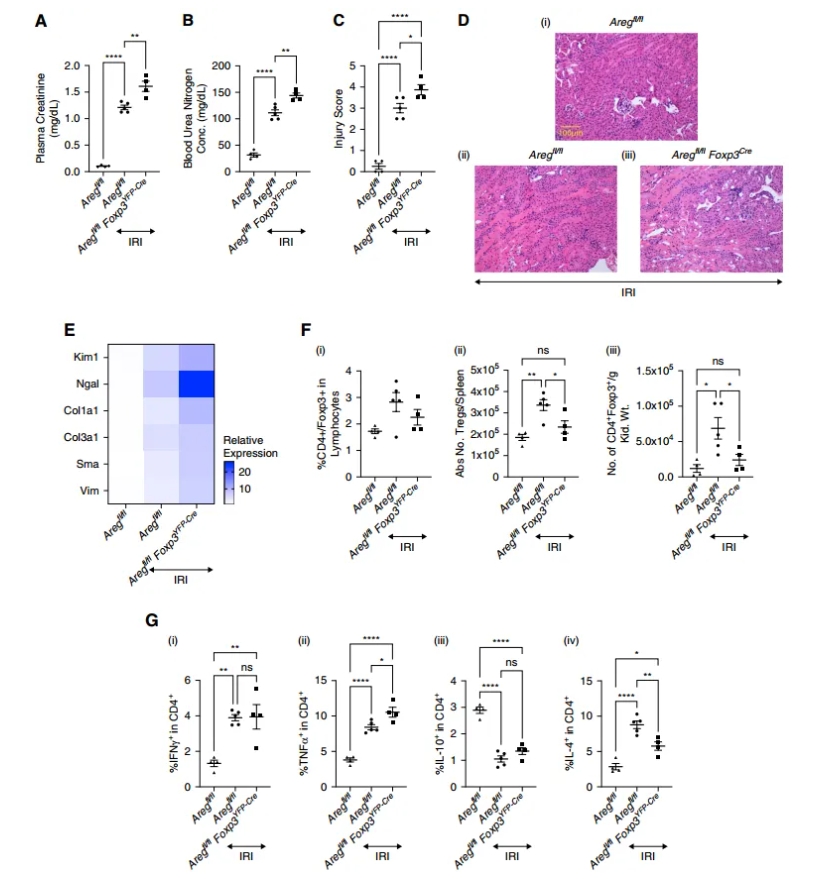
图7a–b:肌酐和BUN;图7c–d:损伤评分和H&E图像;图7e:qPCR热图;图7f:Tregs分布;图7g:细胞因子产生。(点击查看大图)
【单细胞RNA测序确认肾特异性ST2+ Tregs修复机制】
鉴于脾转录组代表稳态,为探讨肾损伤后Tregs的特异变化,作者从IRI肾脏分离CD4+ T细胞,进行单细胞RNA测序(scRNA-seq)分析。这一步基于整体结果,旨在确认肾特异性机制。
UMAP显示野生型(WT)和敲除组(KO)聚类不同;Tregs中Foxp3、Areg和Il1rl1共表达,并在WT更高。Il1rl1+子集更激活,与KO分离;KEGG分析显示上调路径包括细胞周期、mTOR、AMPK和TCR。这确认肾ST2+ Tregs在损伤环境中具有增强的修复功能,与脾结果一致。
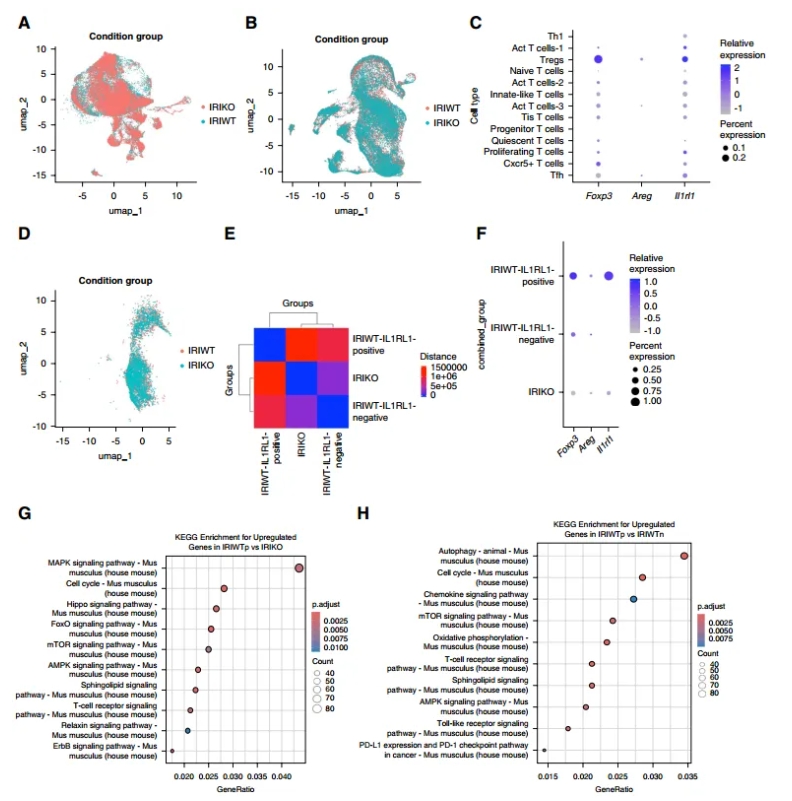
图8a–b:UMAP聚类;图8c:基因共表达;图8d–f:子集分析;图8g–h:KEGG富集。(点击查看大图)
1. IL-33/ST2通路与肾脏损伤:研究重点关注IL-33/ST2信号通路如何通过Tregs调节肾脏的炎症和纤维化。
2. ST2缺失的影响:在IRI模型中,Tregs中特异性缺失ST2或AREG的小鼠表现出更严重的肾脏损伤、炎症和纤维化,表明ST2表达的Tregs在保护肾脏功能和减轻纤维化方面起着重要作用。
3. 肾脏类器官的共培养研究:研究采用了新型的共培养系统,将肾脏类器官(KDOs)与Tregs在低氧条件下共培养。ST2缺失的Tregs未能保护KDOs免受低氧损伤,而野生型Tregs能够保护,强调了ST2表达的Tregs在肾脏修复中的保护作用。
本文展示了一种肾类器官共培养系统在AKI修复机制研究中的新路径。研究团队通过转录组分析和IRI模型,结合KDO低氧共培养,揭示IL-33/ST2通路调控Tregs产生AREG,促进肾损伤修复。该研究构建了“转录组发现—体内验证—体外机制”的闭环流程,显著提升了免疫调控评估能力。
对于肾类器官而言,该模型的创新在于模拟前体细胞低氧脆弱性,并直接验证Tregs分泌物作用。肾类器官在实际应用中存在一定门槛,如高成本或操作难度大等问题,但随着近十年的发展,肾类器官培养和实验操作已经逐渐趋于系统和标准化。比如本研究中的KDO基于标准胚胎干细胞的分化方法,经过实际操作证明,其成本可控且低于动物模型,而且通过标准优化实验协议,操作难度也可以大大降低。关键在于,研究者需要根据实验需求尝试这一新型研究工具,就能发现其潜力。像华津生物这样的类器官技术平台,能够为研究者提供全方位的技术支持和产品服务,帮助大家更轻松地将KDO整合到实验中。
文章来源:Sabapathy, V. et al. ST2+ T-Regulatory Cells in Renal Inflammation and Fibrosis after Ischemic Kidney Injury. J. Am. Soc. Nephrol. 2025, 36, 73–86.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

