肾脏发育的核心在于肾祖细胞(Nephron Progenitor Cells, NPCs),它们负责生成肾小球、肾小管等功能单元。传统研究依赖于胚胎分离或干细胞诱导,但受限于短期培养、异质性和基因编辑难度,难以实现大规模疾病建模或药物筛选。近年来,肾类器官技术快速发展,三维肾类器官已成为模拟肾发育、遗传性肾病(如多囊肾病)和药物毒性的理想平台。然而,如何实现NPC的长期扩增、提升类器官成熟度,并揭示肾细胞塑性,依旧是挑战。
USC的李中伟团队在2024年开发了一种化学定义的2D培养系统,支持小鼠和人类NPC的克隆扩增,并应用于肾类器官成熟、CRISPR筛选、细胞塑性和ADPKD建模。该系统不仅生成更成熟的足细胞,还揭示了足细胞向NPC的重编程潜力,并通过基因编辑NPC快速筛选多囊肾抑制剂。这一工作为肾类器官智能化与精准医学结合提供了范式,发表于《Cell Stem Cell》,标志着肾再生研究的重要突破。
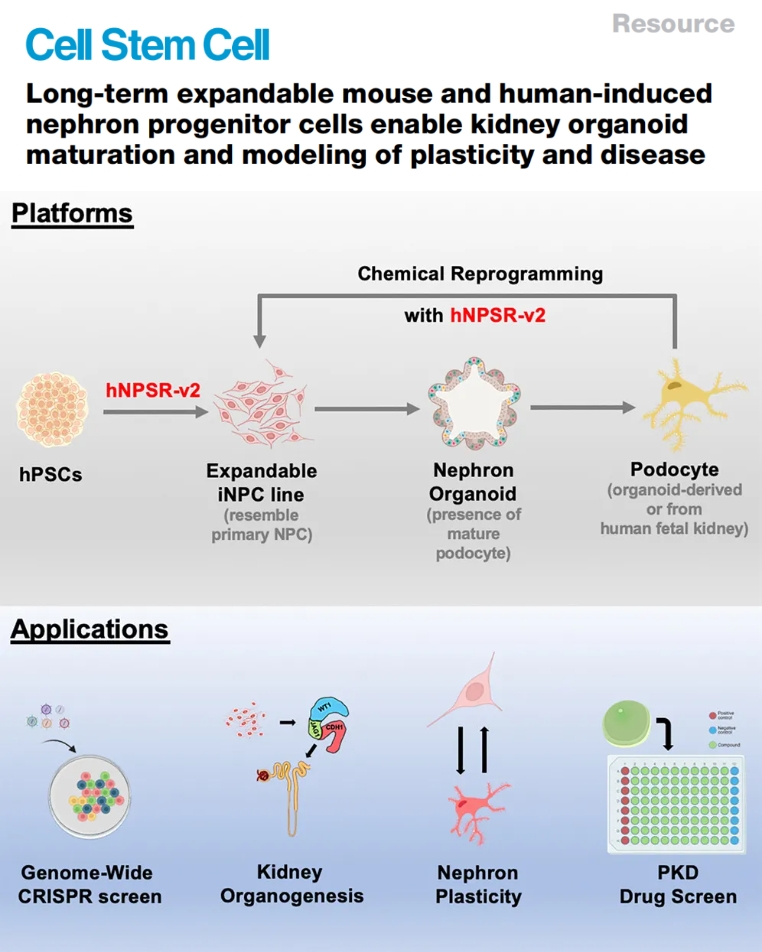
(点击查看大图)
【p38抑制实现任意小鼠品系NPC系的衍生与扩增】
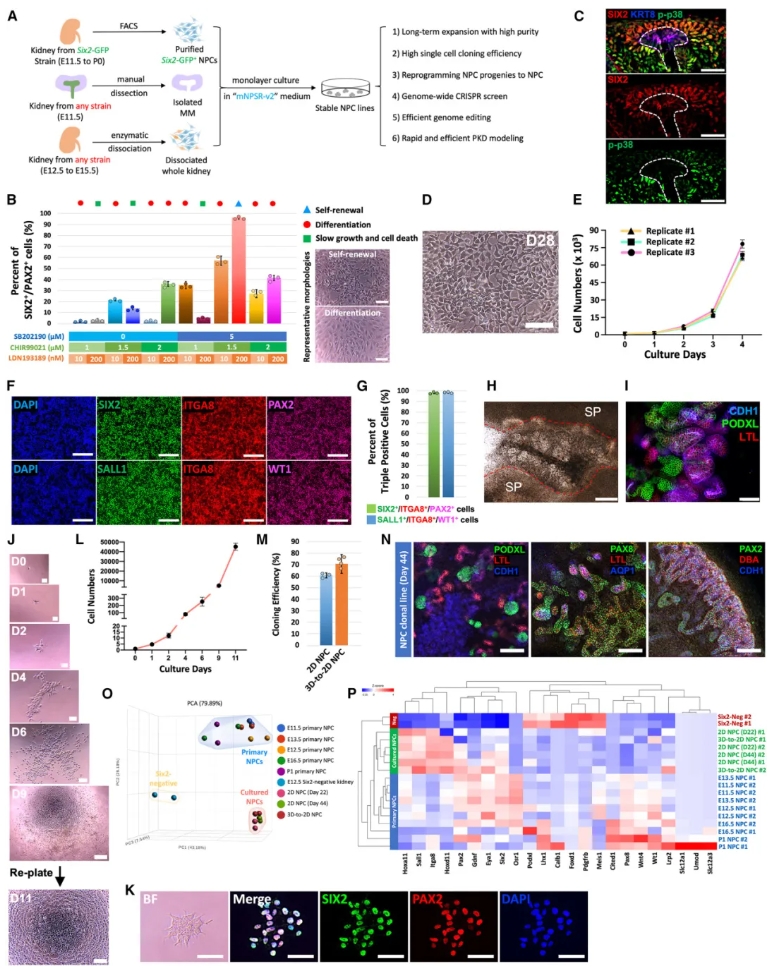
本研究首先优化了小鼠NPC(mNPC)培养介质mNPSR-v2,通过添加p38抑制剂SB202190、Notch抑制剂DAPT、TGF-β抑制剂A83-01和BMP抑制剂LDN193189,并调整CHIR99021浓度,支持mNPC的长期2D克隆扩增(图1A)。实验显示,SB202190对维持SIX2+/PAX2+细胞比例至关重要(图1B),而体内自续mNPC的p38活性本就较低(图1C)。培养的mNPC形态均匀(图1D)、稳定增殖(图1E),并均匀表达NPC标志物如SIX2、PAX2、SALL1、WT1和ITGA8(图1F–G)。体外诱导实验中,mNPC与脊髓共培养形成肾小管样结构(图1H),并分化为PODXL+肾小球、LTL+近曲小管和CDH1+远曲小管(图1I)。克隆效率高达60%–70%(图1J–N),RNA-seq PCA显示培养mNPC与E11.5–E13.5原代NPC高度相似(图1O–P)。该系统适用于任意小鼠品系,包括E11.5元肾间充质或全肾细胞衍生。
(点击查看大图)
图1A:mNPC衍生与应用示意图;图1B:不同条件下SIX2+/PAX2+细胞比例量化;图1C:E13.5肾切片p38活性免疫染色;图1D–E:mNPC形态与生长曲线;图1F–G:标志物免疫荧光与量化;图1H–I:脊髓诱导形成的肾结构亮场与免疫荧光;图1J–N:单细胞克隆扩增、生长曲线、克隆效率与类器官免疫荧光;图1O–P:RNA-seq PCA与标志物热图。
【mNPSR-v2揭示发育中小鼠肾细胞的塑性】
在成功建立小鼠NPC的长期扩增系统后,研究团队注意到培养过程中一些非NPC细胞表现出意想不到的表型转化,这提示了潜在的细胞塑性机制。为了深入探讨这一现象,他们利用该系统进一步考察了发育中小鼠肾细胞在mNPSR-v2介质中的行为变化。
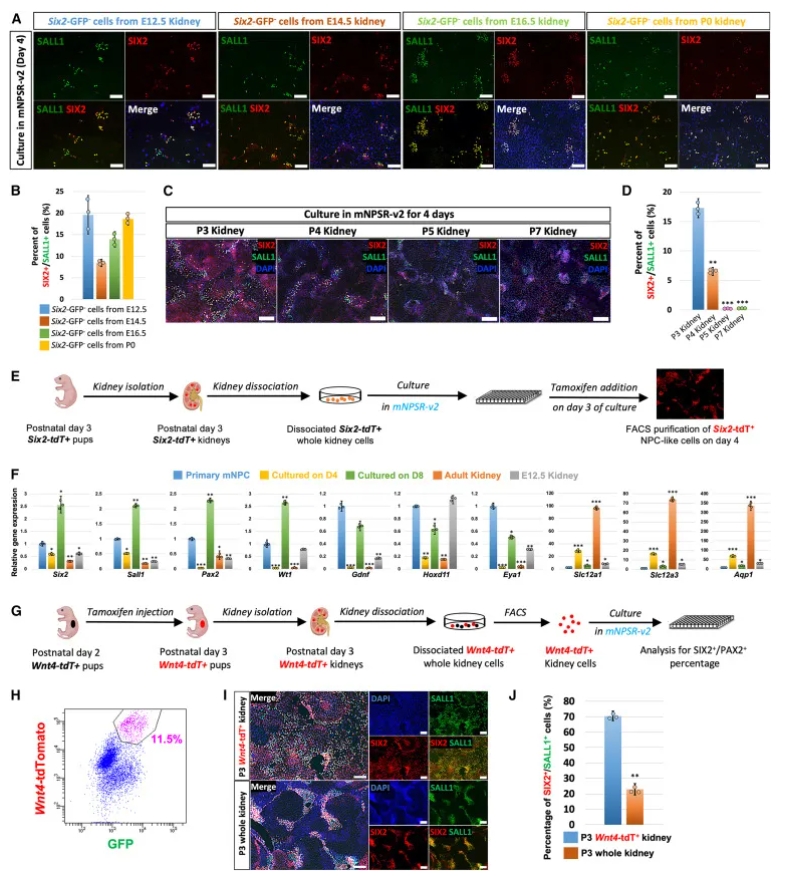
研究观察到mNPSR-v2可诱导非NPC细胞(如Six2-GFP–细胞)转化为SIX2+/SALL1+表型(图2A–B)。从P3–P7肾细胞培养中,约17% P3细胞在4天内诱导为SIX2+/SALL1+(图2C–D),效率在mNPSR-v2中最高(18%)。使用Six2-tdT谱系示踪,诱导细胞表达完整NPC基因谱(Six2、Pax2等),丢失肾标志物(Slc12a1等)(图2E–F)。进一步,Wnt4+细胞(NPC直接后代)在mNPSR-v2中高效逆转为SIX2+/SALL1+(>70%)(图2G–J),表明mNPSR-v2模拟了体内NPC龛,支持Wnt4+细胞的塑性逆转。
(点击查看大图)
图2A–D:Six2-GFP–和新生肾细胞诱导的免疫荧光与量化;图2E–F:Six2-tdT诱导示意图、FACS与qPCR;图2G–J:Wnt4-tdT示踪示意图、FACS、免疫荧光与量化。
【全基因组CRISPR筛选提供肾发育与疾病资源】
基于mNPSR-v2系统对小鼠NPC的稳定支持和塑性揭示,研究者认识到这一平台适合进行大规模基因功能分析。为了从全基因组层面理解NPC自续和相关疾病机制,他们引入CRISPR敲除文库进行筛选实验。
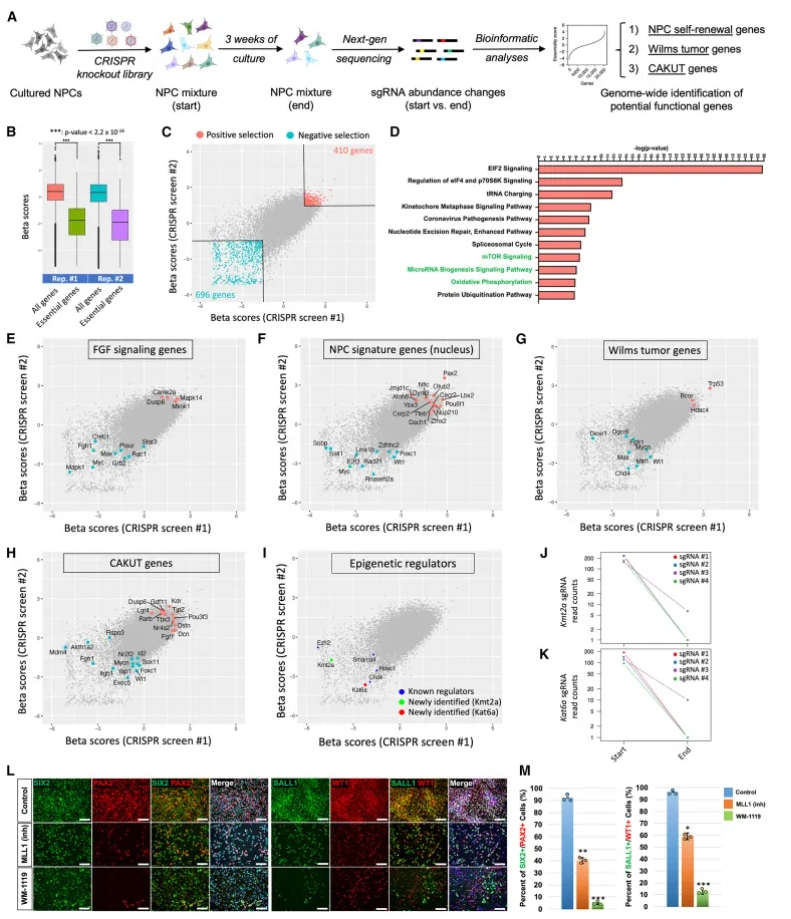
引入全基因组CRISPR敲除文库到mNPC中,筛选自续相关基因(图3A)。Beta分数分析显示负选择“泛必需基因”(图3B–C),IPA富集mTOR、miRNA生物合成和氧化磷酸化路径(图3D)。FGF、WNT和LIF信号基因被负选择(图3E)。筛选出64个潜在NPC自续基因,25个核定位,包括Sall1、Wt1等(图3F)。11/30 Wilms瘤基因和25/330 CAKUT基因被鉴定(图3G–H)。验证Kmt2a和Kat6a为必需(图3I–M),抑制剂处理降低NPC标志物表达。
(点击查看大图)
图3A:CRISPR筛选流程;图3B–C:Beta分数分布与共同基因散点图;图3D:IPA路径富集;图3E–I:信号路径散点图与sgRNA计数;图3J–M:抑制剂免疫荧光与量化。
【YAP激活衍生长期可扩增人类NPC系】
CRISPR筛选结果强调了信号通路在NPC维持中的作用,这启发研究者将小鼠系统的优化经验扩展到人类NPC,以实现更贴近临床的应用。为此,他们调整介质成分,开发支持人类诱导NPC(iNPC)的长期扩增系统。
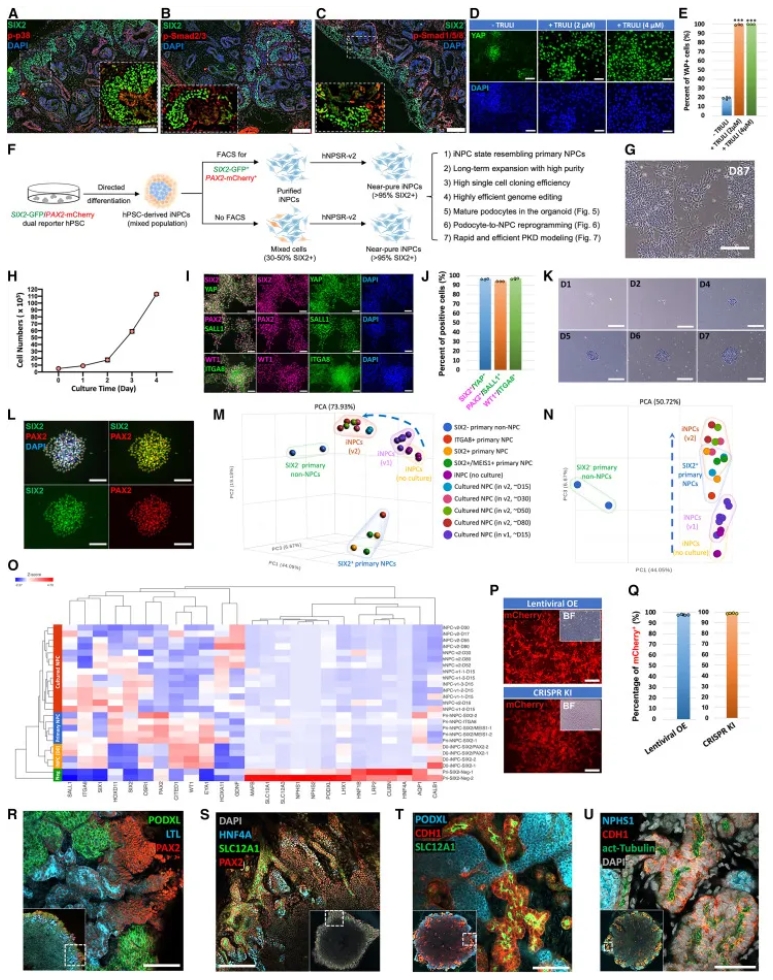
原代hNPC中p38、TGF-β和BMP活性低(图4A–C)。hNPSR-v1支持短期iNPC扩增,但YAP核表达丢失(图4D–E)。添加YAP激动剂TRULI制成hNPSR-v2,支持>3个月稳定扩增(图4F–H),>95%细胞表达SIX2/PAX2等(图4I–J)。克隆效率58%–70%(图4K–L)。RNA-seq显示v2培养iNPC更似原代NPC(图4M–O)。支持基因编辑(图4P–Q)。诱导形成无脱靶细胞的肾类器官,包括成熟PODXL+/NPHS1+肾小球、LTL+近曲小管和SLC12A1+亨勒环(图4R–U)。
(点击查看大图)
图4A–C:人胎肾切片免疫荧光;图4D–E:YAP表达变化;图4F:iNPC衍生示意图;图4G–H:形态与生长曲线;图4I–J:标志物免疫荧光与量化;图4K–L:克隆扩增图像;图4M–O:RNA-seq PCA与热图;图4P–Q:基因编辑图像与量化;图4R–U:类器官免疫荧光。
【单细胞多组学揭示iNPC类器官的体内样肾生成与成熟足细胞】
在确认hNPSR-v2能生成高质量iNPC后,研究团队进一步评估这些iNPC诱导的肾类器官的成熟度和细胞组成,以验证系统是否能产生更接近体内肾生成的结构。
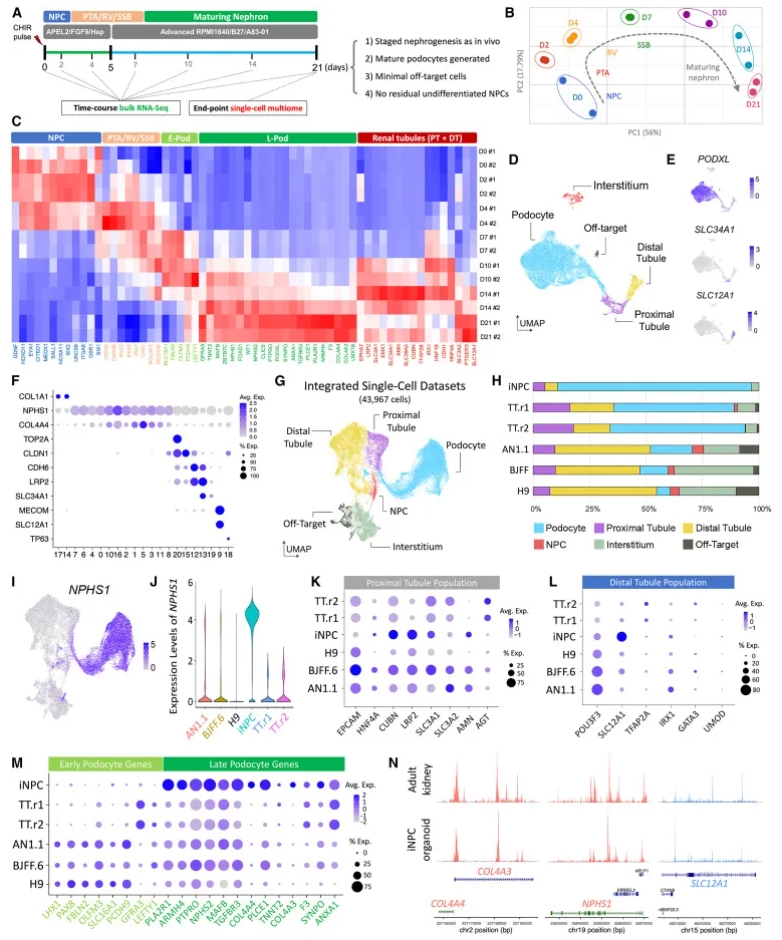
时间序列RNA-seq显示从NPC到成熟肾的渐进变化,早足细胞基因在day7–10、晚足细胞基因(如COL4A3/4)在day10–21上调(图5A–C)。snRNA/snATAC-seq鉴定足细胞、近/远曲小管、间质和少量脱靶细胞(0.67%)(图5D–F)。整合其他数据集显示iNPC类器官足细胞比例更高、脱靶更少、无残留NPC(图5G–H)。足细胞表达更高晚期基因,ATAC-seq开放染色质似成人肾(图5I–N)。
(点击查看大图)
图5A:实验设计;图5B–C:PCA与热图;图5D–F:UMAP、签名基因与点图;图5G–H:整合UMAP与细胞比例;图5I–N:标志物点图与基因组浏览器视图。
【hNPSR-v2揭示人类足细胞塑性】
鉴于iNPC类器官显示出更高的成熟度,研究者借鉴小鼠系统的塑性发现,考察hNPSR-v2是否也能诱导人类肾细胞的逆编程,以揭示人类足细胞的潜在可塑性。
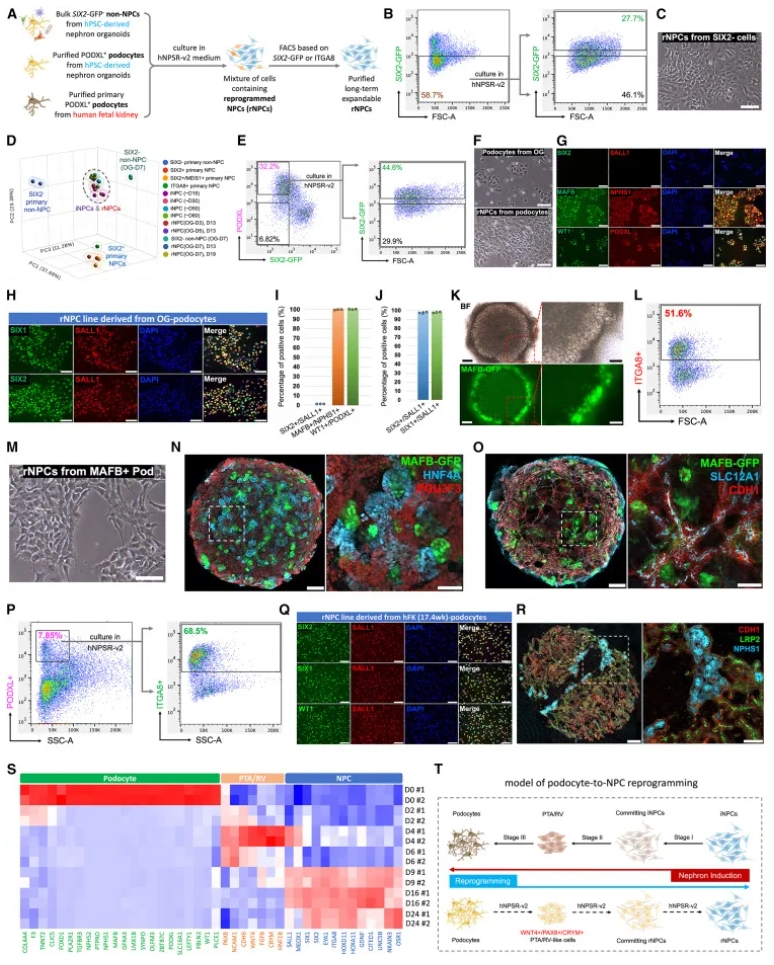
从SIX2-GFP–非NPC诱导rNPC,27.7%转为SIX2-GFP+(图6A–C)。RNA-seq显示与iNPC相似(图6D)。PODXL+/SIX2–足细胞在hNPSR-v2中44.6%转为rNPC(图6E–J)。MAFB-GFP+足细胞类似重编程(图6K–O)。原代足细胞也衍生rNPC(图6P–R)。时间序列RNA-seq显示经PTA/RV中间态逆转(图6S–T)。
(点击查看大图)
图6A–D:重编程示意图、FACS、形态与PCA;图6E–J:足细胞FACS、形态与免疫荧光;图6K–O:MAFB-GFP类器官、FACS、形态与免疫荧光;图6P–R:原代足细胞FACS与类器官;图6S–T:热图与模型。
【基因编辑NPC的快速PKD建模与小分子筛选】
利用该系统的基因编辑兼容性,研究团队将目光转向实际疾病应用,通过敲除PKD基因在NPC中建模ADPKD,并进行小分子筛选,以展示平台的药物发现潜力。
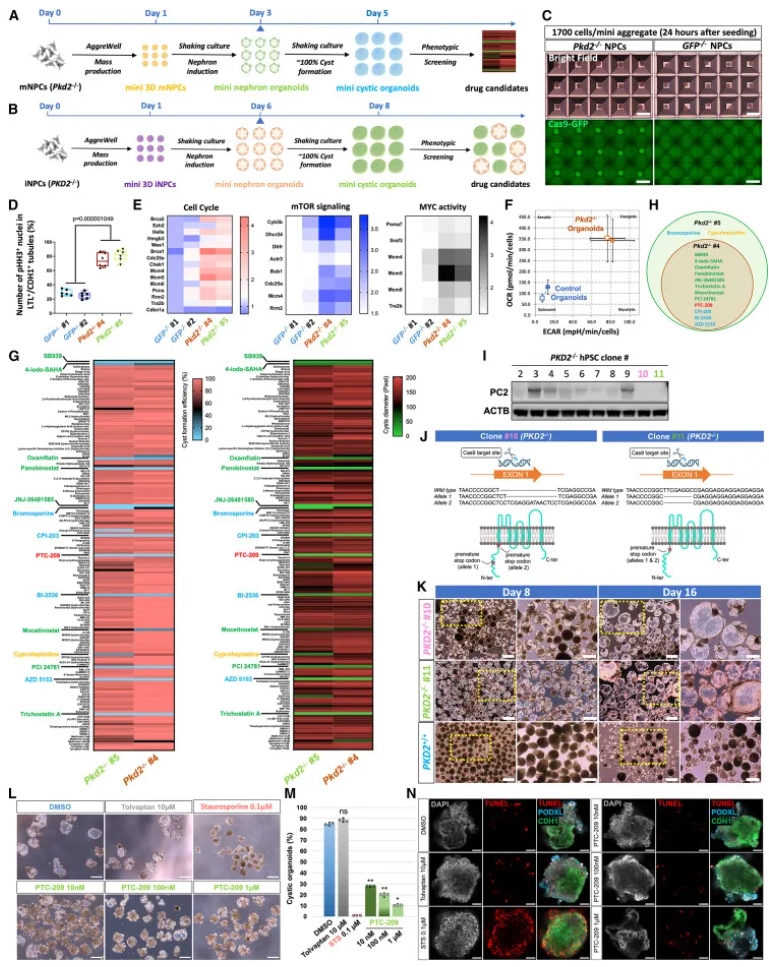
Pkd1/2敲除mNPC诱导囊肿类器官,抑制剂如CFTRinh172降低囊肿(图7A、C–F)。snRNA-seq显示增殖、mTOR/MYC激活和代谢上调(图7E)。筛选148个化合物鉴定HDAC、BRD4和BMI-1抑制剂(图7G–H)。人PKD2–/–iNPC类似建模,PTC-209剂量依赖抑制囊肿(图7I–N)。
(点击查看大图)
图7A–B:建模示意图;图7C:聚集与囊肿亮场;图7D–F:增殖免疫荧光、热图与代谢曲线;图7G–H:筛选热图与命中;图7I–N:PKD2编辑、囊肿图像与抑制量化。
1.创新培养系统:首次实现小鼠和人类NPCs的长期2D克隆扩展,克服了以往3D系统的繁琐性和不兼容性(如CRISPR筛查)。
2.足细胞成熟度提升:iNPCs衍生的肾小器官中,足细胞更接近体内成熟状态,表达COL4A3/4,这在体外模型中是重大进步。
3.细胞塑性揭示:惊人发现hNPSR-v2可诱导WNT4+ committed progenitors和MAFB+/NPHS1+足细胞重编程回NPC状态,揭示人类肾细胞的发育可塑性。
4.基因组筛查与疾病建模:全基因组CRISPR筛查鉴定基因。结合基因编辑NPCs,建立了高效ADPKD模型,并从148种表观遗传小分子库中筛选出BMI-1抑制剂PTC-209作为潜在疗法,展示了平台的药物发现潜力。
这篇发表于《Cell Stem Cell》的论文(Huang et al., 2024)开发了一种化学定义的二维(2D)培养系统(mNPSR-v2和hNPSR-v2),成功实现了小鼠和人类诱导的肾祖细胞(NPCs)的长期克隆扩展。该系统通过调控p38 MAPK和YAP信号通路,不仅支持从多株小鼠和人类多能干细胞(hPSCs)来源的NPCs稳定扩增,还生成肾单位器官(nephron organoids),这些器官中足细胞(podocytes)表现出更高的成熟度,表达关键基底膜成分如COL4A3和COL4A4——这在以往体外肾小器官中仅见于移植到小鼠肾脏后的模型。此外,论文揭示了人类足细胞的惊人塑性:它们可在hNPSR-v2介质中逆转分化,重编程回NPC-like状态,支持肾发育的动态可塑性研究。同时,通过全基因组CRISPR筛查,作者鉴定出调控肾发育、Wilms肿瘤和先天性肾尿道异常(CAKUT)的关键基因,并利用基因编辑NPCs快速建模常染色体显性多囊肾病(ADPKD),并筛选出新型小分子抑制剂。
论文讨论部分强调,该系统将促进对p38 MAPK和YAP在NPC扩展中机制的深入研究,并探索足细胞塑性的分子基础。展望未来,该平台有望优化肾小器官生成全谱肾单位(如Henle环和远端小管),通过筛选条件最大化iNPCs发育潜力。相比传统hPSC系统,其纯净、可操控的NPC基础更适合高通量药物筛查和个性化医学。例如,在遗传性肾病(如Alport综合征)建模中,可利用重编程足细胞开发精准疗法;在再生医学中,扩展NPCs可推动肾组织工程和移植。总体而言,这项工作标志着肾发育研究进入“可扩展、可编辑”时代,将加速从基础洞见到临床转化的进程,为肾病患者带来新希望。期待后续研究扩展到成人肾祖细胞或多器官交互模型,进一步桥接体外与体内差距!
文章来源:Huang et al., 2024, Cell Stem Cell 31, 921–939. doi:10.1016/j.stem.2024.04.002

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

