心血管疾病的发生往往伴随着高度复杂的炎症反应,这种炎症不仅导致心肌细胞损伤、线粒体功能障碍、甚至引发纤维化过程,最终演变为慢性心脏功能衰竭。传统研究依赖于动物模型或二维心肌细胞系统,受限于物种差异和结构简单,难以准确重现人类心脏组织在炎症状态下的病理动态。近年来,随着类器官技术的飞速发展,三维心脏类器官正逐步成为疾病建模和药物筛选的关键载体。然而,如何在结构复杂、收缩异质性高的类器官中,高效、定量、动态地评估炎症水平,依旧是一项极具挑战的问题。
针对这一瓶颈,来自中国科学院化学研究所的王树团队和白浩天团队联合开发了一种集炎症建模、AI评估、代谢干预于一体的“智能类器官系统”。研究人员利用多种炎症因子刺激构建人源心脏炎症类器官,并引入人工智能算法,结合明场视频影像与机器学习,建立了一个可以在30分钟内完成“炎症定量打分”的AI评估平台。该系统能够捕捉类器官的收缩频率、形态变化、图像纹理等多个维度的参数,并通过XGBoost分类器链模型对炎症类型、刺激浓度、作用时间进行高精度识别。不仅如此,研究团队还开发出一种由共轭聚合物与类叶绿体结构组成的光控能量干预系统,可在类器官内实现ATP和NADPH的内源性供给,显著改善炎症诱导下的能量代谢障碍,降低IL-6等炎症因子的表达,最终实现类器官功能的恢复。这一工作不仅验证了AI+类器官在“功能评估+干预反馈”闭环体系中的可行性,也为今后在肾脏类器官中开展炎症分型、药物效应评估与再生治疗测试提供了重要范式。该研究以题为:Artificial Intelligence‐Enabled Quantitative Assessment and Intervention for Heart Inflammation Model Organoids发表于《Angewandte Chemie International Edition》,是类器官智能化与精准医学结合的重要探索。
研究内容
【三步调控Wnt通路,构建结构复杂的心脏炎症类器官】
本研究以人源诱导多能干细胞(hiPSCs)为起点,通过调控Wnt信号的激活与抑制节律,分三步构建出结构复杂、细胞类型多样的心脏类器官:
第一步(Day 0):使用CHIR-99021激活早期Wnt信号,诱导中胚层分化;
第二步(Day 2):用Wnt-C59抑制Wnt通路,促进心肌谱系定向;
第三步(Day 6):短时再次使用CHIR-99021促使器官发育成熟。
类器官中涵盖了心肌细胞(TNNT2+)、心内膜细胞(NFAT2+)、内皮细胞(CD31+)与间质细胞(Vimentin+),显示其具备初期血管网络与心腔结构,是理想的炎症建模平台。为了诱导心脏炎症,研究者将类器官暴露于三种炎症因子(IFN-γ、TNF-α、IL-1β)中,设定不同浓度(0、1、10、100 ng/mL)与不同时间(48 h或96 h)处理条件。通过基因表达分析,发现10 ng/mL IL-1β作用48小时时,IL-1β、IL-6、MMP9 等炎症与纤维化标志物显著上调,成为后续建模标准条件。
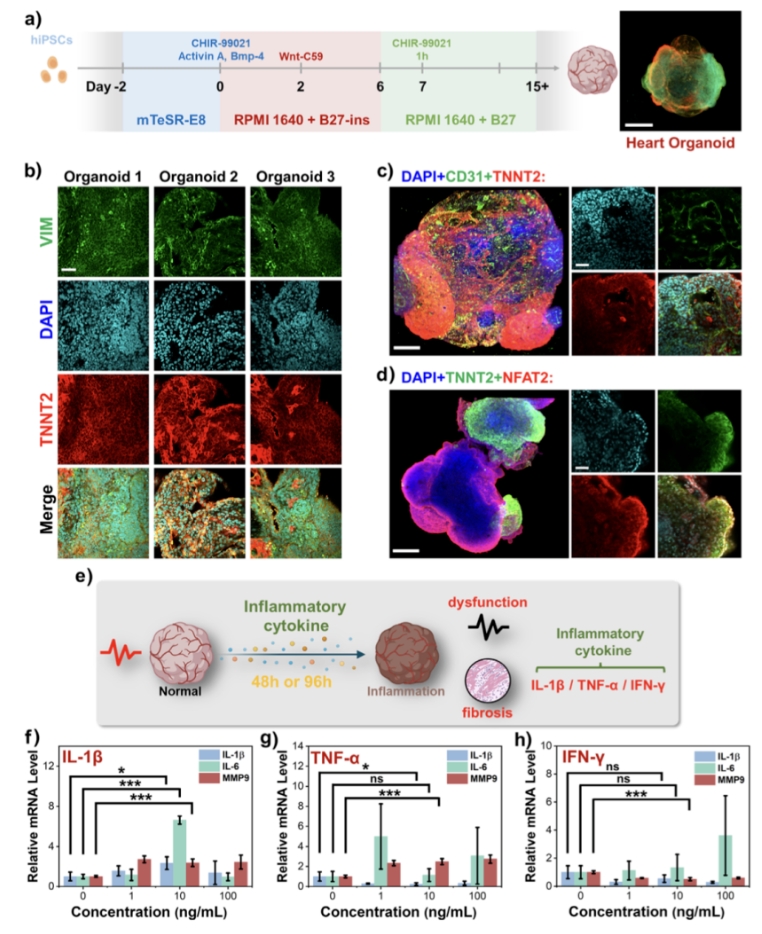
图1a:三步调控Wnt通路生成心脏类器官的流程图;b–d:类器官中多种细胞类型免疫荧光图像;e:炎症诱导策略;f–h:IL-1β、TNF-α、IFN-γ三种炎症因子诱导后,炎症/纤维化基因表达变化。
【明场影像 × 机器学习,构建类器官炎症量化评估平台】
如何判断类器官是否“生病”?传统方法多依赖染色、PCR、ELISA等手段,不仅耗时、成本高,也难以批量筛查。研究者引入人工智能(AI)模型,结合类器官的明场影像,建立了一种无需标记、可快速量化炎症水平的分析系统。
✦ 数据构建:
团队采集了664个心脏类器官的明场视频,覆盖不同炎症因子、浓度与时间处理条件。对每段视频进行图像分割后,提取了110种特征,包括:
时间特征(如收缩频率、节律)
形态特征(如长轴、伸展度)
纹理特征(如灰度非均匀性)
✦ AI模型设计:
基于XGBoost分类器构建三重分类器链模型,用于识别:
1. 炎症因子类型(IL-1β / TNF-α / IFN-γ)
2. 刺激浓度(1 / 10 / 100 ng/mL)
3. 刺激时间(48 h / 96 h)
三重分类器以不同顺序排列并集成,有效提升多标签预测准确度。模型在验证集中的准确率分别达到 80%、76%、87%,性能优异。
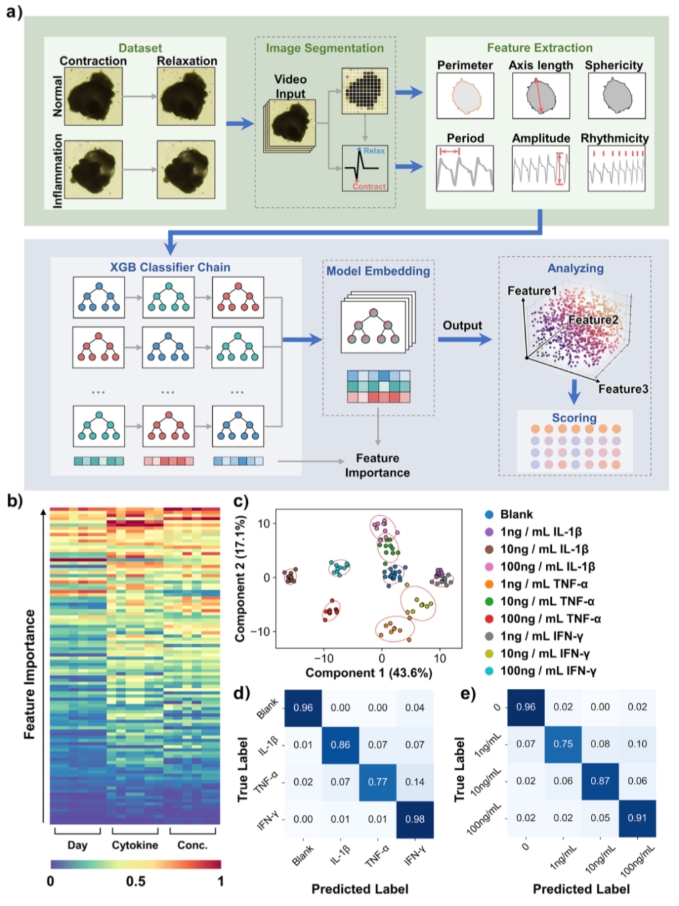
图2a:整体评估流程图:图像处理→特征提取→分类模型→输出“炎症得分”;图2b:各子分类器中不同特征的重要性排序;图2c:LDA降维可视化结果,表明模型能区分不同炎症状态;图2d-e:混淆矩阵显示模型在分类“炎症因子类型”和“浓度”上的表现。
【10个关键特征,构建30分钟内完成的炎症打分体系】
从110个图像特征中,研究团队通过多链XGBoost模型对所有特征进行归一化排序,筛选出最具代表性的10个关键特征,这些特征可用于反映类器官功能状态、结构完整性与组织均质性。核心特征包括:
1. 功能特征:
(1) 收缩频率(period_fft):类器官是否规律跳动
(2) 最大振幅(max_amplitude):搏动强弱
(3) 收缩周期标准差:节律是否紊乱
2. 形态学特征:
伸展度(elongation)、长轴长、面积变化等,反映类器官形态变化程度
3. 图像纹理特征(GLSZM, GLDM):
表示图像中低灰度区的大小、均匀性,间接反映细胞密度和组织结构紧凑性
建模炎症评分:
团队进一步引入Yeo-Johnson变换对每一特征分布进行标准化,并将其偏离健康组的程度赋予权重,最终构建出一个“炎症评分模型”,能对任意一个类器官视频给出0~1之间的炎症量化分值。结果显示:
(1) 在所有诱导条件中,“10 ng/mL IL-1β 处理48小时”的组别炎症评分最高(0.55)
(2) 整个评估流程(从影像采集到打分完成)仅需 30分钟
(3) 与真实生物标志物相关性验证:
1) 研究者使用多元线性回归模型,将图像特征与qPCR检测到的IL-1β、IL-6、MMP9表达水平拟合:
a. 模型R²分别达到 0.66、0.87、0.72
b. 表明少量图像特征即可预测炎症和纤维化基因表达水平
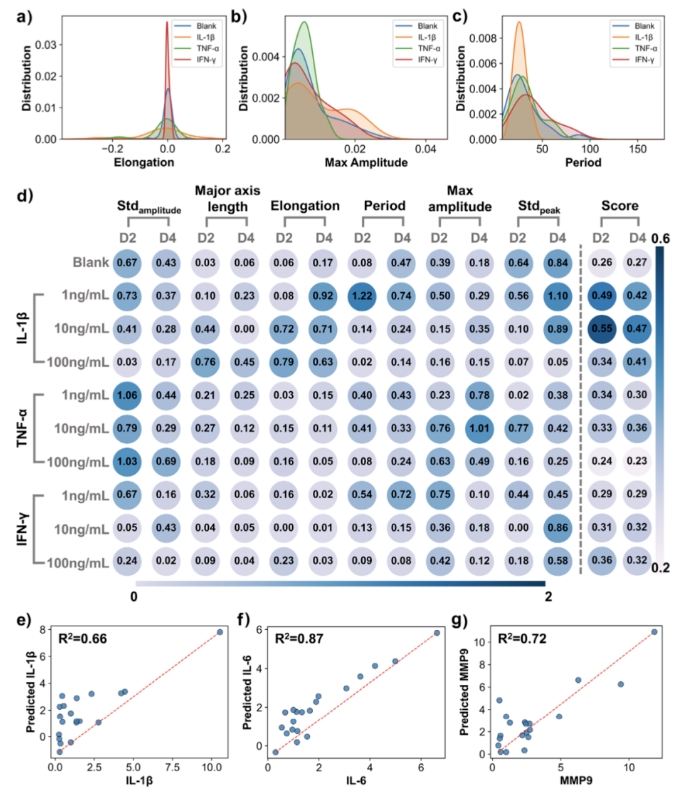
图3a–c:3个关键特征的概率密度分布图;图3d:炎症评分系统的构建流程;图3e–g:模型预测的炎症/纤维化相关基因表达与真实值的拟合效果。
【单细胞测序揭示炎症“逐层瓦解”类器官的结构与功能】
类器官是否“生病”,不能只看表面。为了探究炎症因子对心脏类器官在细胞层面的深远影响,研究团队使用单核RNA测序(snRNA-seq)技术,对健康组与IL-1β刺激组(10 ng/mL × 48 h,该组IL-1β、IL-6(炎症标志物)、MMP9(纤维化标志物)等基因表达上出现了最显著的上调,该组的炎症评分(基于XGBoost回归)最高,达到 0.55)的类器官进行了深入剖析。两组类器官均包含以下核心细胞类型:心房肌细胞 / 心室肌细胞 / 内皮细胞(毛细血管、淋巴管、血管内皮等多亚型)/ 心内膜细胞 / 间充质细胞 / 周细胞 / 成纤维细胞/ 神经细胞 / 脂肪细胞 / 单核细胞等免疫成分。炎症状态下,这些细胞类型虽然仍存在,但其基因表达谱、细胞代谢、分化状态发生显著改变。
(1) GO富集分析结果:
1) 心室肌细胞(Ventricular CMs):表现出线粒体功能障碍,涉及多个能量代谢路径受损
2) 血管内皮细胞(Endothelial Cells): Wnt信号通路与细胞周期调控异常,内皮功能紊乱显现
3) 心室/心房发育相关基因如:MEF2C、NRP2、TPM1 等结构/收缩功能调控基因显著下调。
(2) 炎症相关基因变化:
1) 炎症上调因子:IL32、TNFAIP2
2) 代谢/功能下调因子:AFP、SHB、APOC3、APOA1、APOA2
其中,APOA1/2作为HDL-C的主要成分,与动脉粥样硬化等CVDs呈负相关——这暗示心脏类器官的炎症可能推动真实心血管疾病的进展。
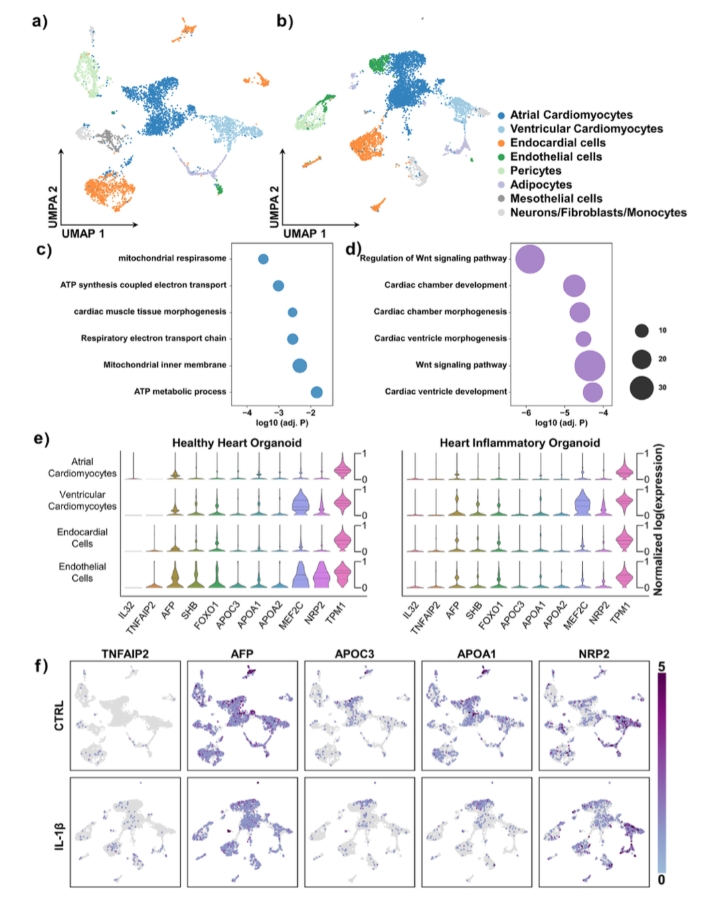
图4a–b:健康类器官 vs IL-1β组类器官的UMAP聚类图,展示多种细胞类型;图4c–d:GO功能通路分析,揭示炎症对能量代谢和细胞周期的影响;图4e–f:多个发育关键基因和炎症指标基因在主要细胞亚群中的表达热图/UMAP分布。
【借光而行,ATP/NADPH能量系统精准干预炎症】
在心脏类器官的炎症过程中,研究者发现线粒体功能紊乱与能量失衡是导致心肌损伤、纤维化的关键原因(GO富集分析)。虽然直接补充外源性ATP或NADPH可以在一定程度上缓解能量不足,但无法有效调节细胞内的代谢网络。因此,团队提出一个创新的想法:通过模拟光合作用系统,原位促进心脏类器官产生自身可用的ATP/NADPH。
研究团队开发了一个复合系统:CM-PBF/NTUs(CM-PBF/NTUs是一种光控纳米能量复合物,可通过培养基加入并靶向进入心脏类器官,在光照下原位生成ATP/NADPH,从而为受损细胞提供代谢支持)。
(1) 该系统由三部分组成:
1) NTUs(纳米叶绿体单元,来源于菠菜叶提取)
2) PBF(共轭聚合物poly(boron-dipyrromethene-co-fluorene),可扩展可见光吸收范围)
3) CM(间充质干细胞来源的细胞膜包裹,提供靶向性和免疫逃逸能力)
(2) 该系统工作机制:
1) PBF扩展光敏范围,覆盖470–600 nm绿色光吸收并发射红光,提升NTUs利用光能的效率;
2) 在NTUs中,光能驱动电子传递链,生成ATP与NADPH;
3) CM包裹结构让该复合纳米颗粒靶向炎症区域并减少巨噬细胞清除,保证在类器官内的停留时间;
4) 最终实现在光照条件下,持续、可控地为心脏类器官提供内源能量支持。
(3) 实验验证:
1) CM-PBF/NTUs在光照条件下,ATP产量从27.8增至50.9 µM/µg总叶绿素,
2) NADPH产量从47.3增至78.5 µM/µg总叶绿素。
3) 还通过荧光寿命、ζ电位、ITC测定确认PBF与NTUs以及CM包裹之间的结合稳定性。
4) 动态光散射与TEM图像表明复合纳米颗粒呈现良好的核心-壳结构。
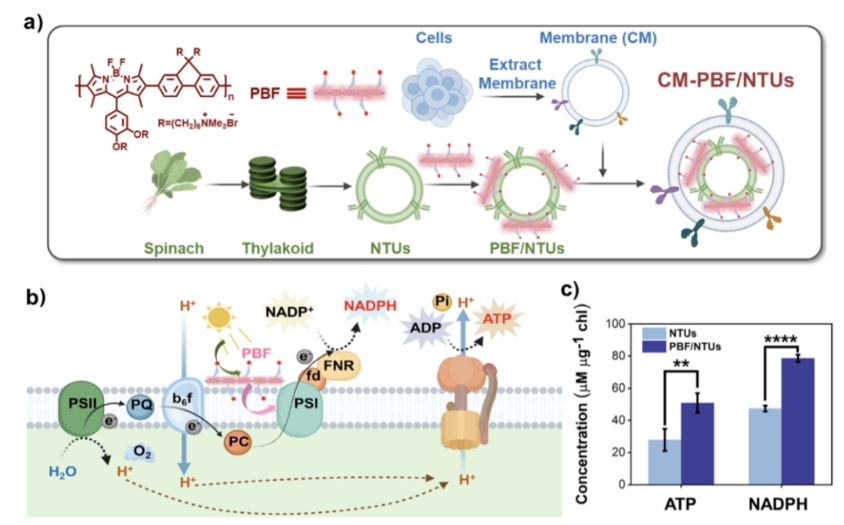
图5a:CM-PBF/NTUs构建示意图;图5b:光敏电子传递链工作流程图;图5c:不同组合体系下ATP/NADPH产量对比柱状图。
【光控纳米干预如何修复心脏类器官?机制验证来了】
在验证了CM-PBF/NTUs可以进入心脏类器官后,研究团队进一步评估它在IL-1β炎症模型中真实的功能修复能力。
(1) 主要功能改善:搏动功能恢复
1) 在光照条件下,CM-PBF/NTUs处理的炎症类器官收缩频率、收缩幅度、节律性均明显改善
2) 收缩频率从炎症模型的 18次/min 恢复到 33次/min,接近健康水平
3) ATP/NADPH水平上升:类器官内ATP含量上升约2倍,NADPH含量也翻倍,提示线粒体能量状态得到有效修复
4) 炎症标志物下降
a. IL-6、TNFAIP2表达下降40%–60%
b. ECM(如MMP9)相关纤维化指标也同步下调
(2) 机制层面验证
1) 通过免疫荧光,研究者观察到CM-PBF/NTUs分布在心肌细胞和血管内皮细胞周围,说明纳米颗粒确实靶向并进入功能区。
2) ROS水平(活性氧)检测:炎症组ROS大量积累,而光控治疗后明显减少,提示氧化应激水平被抑制。
3) 线粒体膜电位(JC-1染料):治疗后线粒体膜电位部分恢复,支撑ATP生成能力
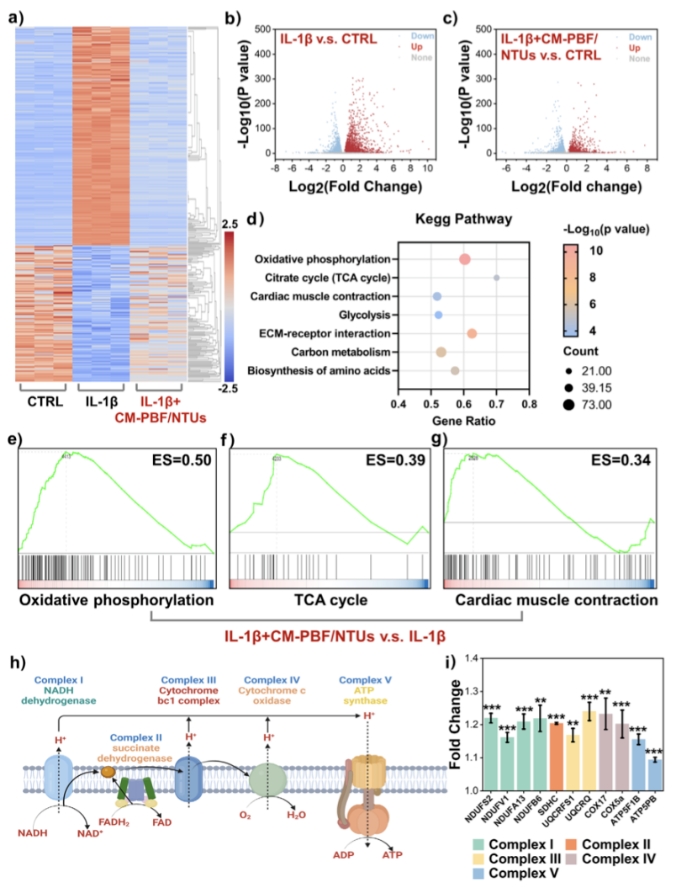
图6a–b:治疗前后心脏类器官外观及节律变化;图6c–d:搏动功能及能量分子含量对比;图6e:炎症/纤维化基因表达变化;图6f–i:CM-PBF/NTUs定位示意、ROS水平及线粒体功能恢复图像。
总结与展望
本文展示了一种AI赋能的心脏类器官炎症建模与干预新路径。研究团队通过多通道Wnt调控构建人源心脏类器官,结合明场影像与机器学习,实现对炎症水平的快速量化;同时利用光控纳米能量系统(CM-PBF/NTUs),在光照条件下为类器官原位补充ATP/NADPH,从而改善能量失衡并修复炎症损伤。该研究构建了“类器官建模—AI识别—可控干预”的闭环流程,显著提升了疾病模型的功能评估和药效验证能力。
对于肾类器官而言,尽管缺少类似心脏的搏动表型,但在炎症或药物毒性状态下,同样可能在明场影像上呈现体积变化、边界模糊或内部光密度异常等特征。未来,若能结合AI算法对这些影像特征进行系统分析,或将逐步探索出一套更高效、客观的健康状态评估方式,并为慢性肾损伤或药物毒性的研究提供可行的参考。随着微流控、代谢调控等技术的进一步发展,肾类器官平台也有潜力向动态响应、自动识别、精准干预方向演进,更好地支撑药物研发和疾病机制探索。
文章来源:Wang, S. et al. Artificial Intelligence‐Enabled Quantitative Assessment and Intervention for Heart Inflammation Model Organoids. Angew. Chem. Int. Ed. 2025, 64, e202501234. doi:10.1002/anie.202501234

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

