面对全球器官供需失衡与移植长期并发症的挑战,来自法国巴黎的Alexandre Loupy 教授团队(Université Paris Cité/INSERM U970)、中国北京的陈香美院士(解放军总医院第一医学中心、国家肾脏疾病临床研究中心)、广州的王海波教授与何建行教授(国家卫生健康委人体组织器官移植与医学大数据中心、广州医科大学附属第一医院),以及温州与澳门的张康教授团队(温州医科大学、澳门科技大学),合作撰写并于2025 年 7 月在《Nature Medicine》发表了综述文章《Reshaping transplantation with AI, emerging technologies and xenotransplantation》。文章系统梳理了移植医学中的核心困境,并重点讨论了人工智能、异种移植以及再生医学中类器官与3D生物打印等新兴技术的应用前景。
学术亮点
人工智能贯穿移植全流程:AI 在供体分配、移植风险预测、数字病理与空间组学中展现出优势,其中 iBox 系统 已获得 EMA 与 FDA 认证,用于预测肾移植远期结局。
个体化免疫抑制探索:通过 AI 辅助剂量调整、靶向递药新材料与调节性 T 细胞(Treg)治疗,有望减少长期药物负担并降低排斥风险。
异种移植取得突破:经过基因修饰的猪心、猪肾和猪肝已在临床案例与体外模型中显示功能,但仍面临免疫与凝血障碍等挑战。
组织工程与再生医学进展:3D 生物打印、先进生物材料与细胞包裹推动了功能性组织构建;类器官因能保留患者基因背景和功能特性,被用于药物筛选和作为潜在修复工具。
伦理与监管挑战:文章强调,所有新技术在进入临床前必须依赖严格的伦理审查、监管框架和 GMP/GCP 标准。
移植医学的核心挑战
文章首先指出,移植是治疗终末期心脏、肾脏、肝脏和肺脏疾病的唯一根本性选择。但现实中存在三大难题:
1.供体严重短缺:等待名单人数远超供体数量,美国超过10万人等待器官,欧洲 Eurotransplant 区域亦存在巨大缺口。
2.长期免疫抑制风险:尽管药物能维持移植物存活,却引发感染、肿瘤、代谢紊乱和心血管疾病,增加远期负担。
3.排斥反应复杂性:肾移植中的 AMR、心脏移植的微血管病变、肺移植的慢性功能障碍、肝移植的 T 细胞介导排斥,均显著影响长期预后。

图1:器官移植连续体中的现有和新兴技术
人工智能在移植中的应用
供体分配与候补名单管理
传统 MELD 指数存在局限,机器学习方法(如 XGBoost)在候补排序和死亡率预测方面表现更优,提高器官分配效率,减少浪费。
移植预后预测
iBox 系统 是代表性成果,结合临床、病理和免疫学数据,可预测肾移植 10 年失败风险,已获 EMA 与 FDA 认可为替代终点,标志着 AI 工具首次获得国际监管承认。
数字病理与空间组学
Banff Automation System(BAS)在 >4000 例肾活检中实现自动分级,30–50% 病例被重新分类,大幅提高一致性。
空间转录组学揭示了炎症细胞浸润与局部免疫反应机制,为精准诊疗提供新线索。
个体化免疫抑制
AI 模型可根据遗传、代谢与社会学变量预测个体化他克莫司剂量,避免药物水平失衡,降低排斥风险。
新兴技术的应用前景
异种移植
基因编辑猪肾在脑死亡受体中恢复尿液生成并维持数周至数月,猪心脏在个别患者中维持循环支持。
难题仍在于:内皮损伤、凝血异常、病毒再激活和长期免疫排斥。
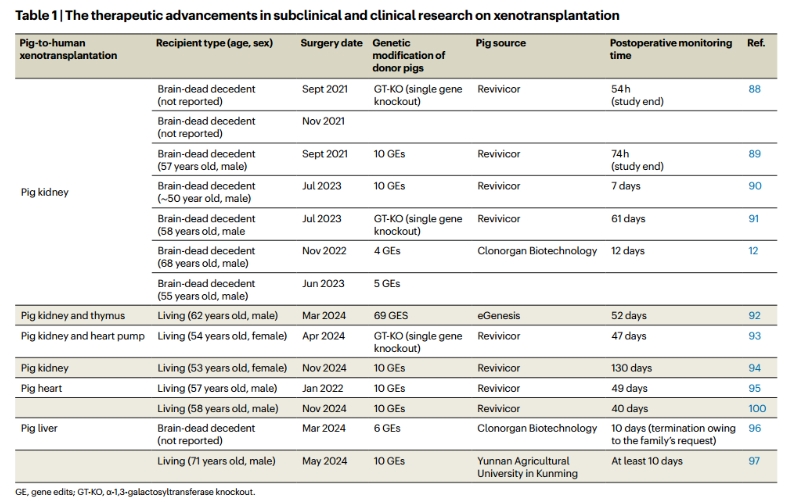
表1:异种移植亚临床和临床研究的治疗进展
类器官与 3D 生物打印
类器官:由干细胞或患者细胞形成的 3D 结构,保留遗传和功能特征,可用于个体化药物测试和作为组织补片,促进血管化和修复。
3D 生物打印:利用生物墨水逐层构建血管化组织,与器官芯片结合可进行动态药物评估。
主要瓶颈:批次差异、规模化生产困难和血管化不足。
生物材料与细胞包裹
新一代支架不仅提供力学支撑,还释放生长因子和信号分子,改善细胞分化和整合。
细胞包裹技术可减少免疫攻击,提升长期存活。
改良的支架(天然、合成、去细胞或杂交)与物理线索(刚度、表面特性)进一步优化组织工程效果。
伦理、监管与社会考量
AI 的透明性:需明确其在临床决策中的责任与作用,避免“黑箱化”。
异种移植的风险:跨物种病原传播与动物伦理必须得到监管保障。
类器官与组织工程:涉及人源细胞与个性化组织,亟需伦理框架支持。
合规要求:包括 GMP 与 GCP,是创新技术转化的前提。
总结
尽管供体短缺与排斥反应依旧是移植医学的核心挑战,但机遇正在展开:AI 工具已走进临床与监管体系,异种移植取得关键突破,再生医学正开辟新的器官来源与修复路径。在多学科协作与完善伦理监管的前提下,未来的移植医学将由 “AI + 新兴技术” 双轮驱动,迎来重塑。肾类器官不仅是疾病建模与药物筛选的平台,更有望成为缓解移植困境的潜在解决方案。
参考文献:
Loupy A, Preka E, Chen X, Wang H, He J, Zhang K. Reshaping transplantation with AI, emerging technologies and xenotransplantation. Nat Med. 2025 Jul;31(7):2161-2173. doi: 10.1038/s41591-025-03801-9. Epub 2025 Jul 14. PMID: 40659768.

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

