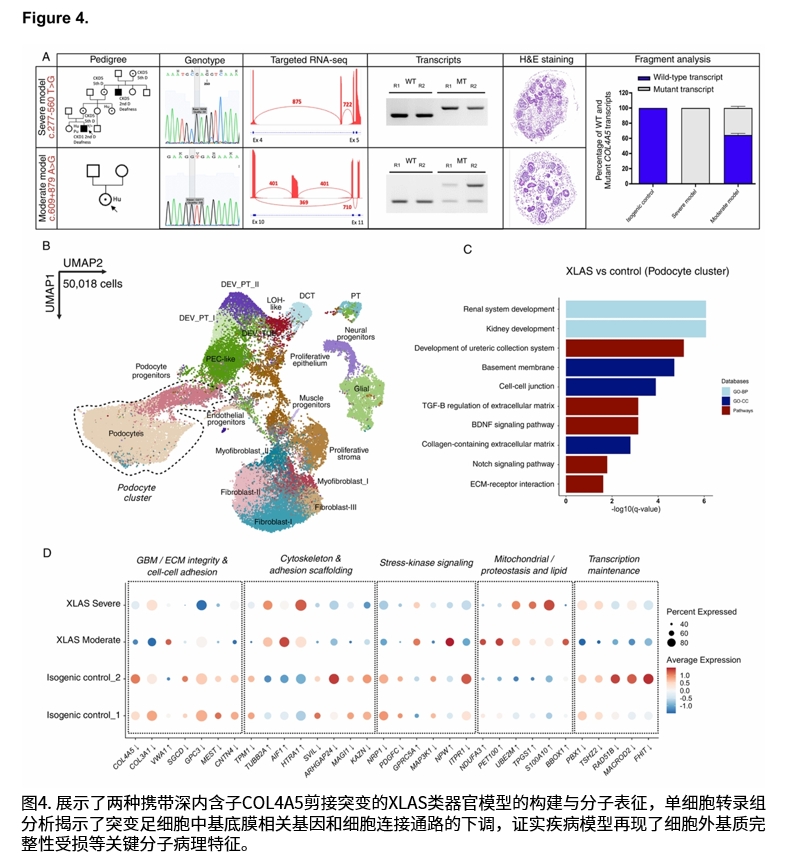
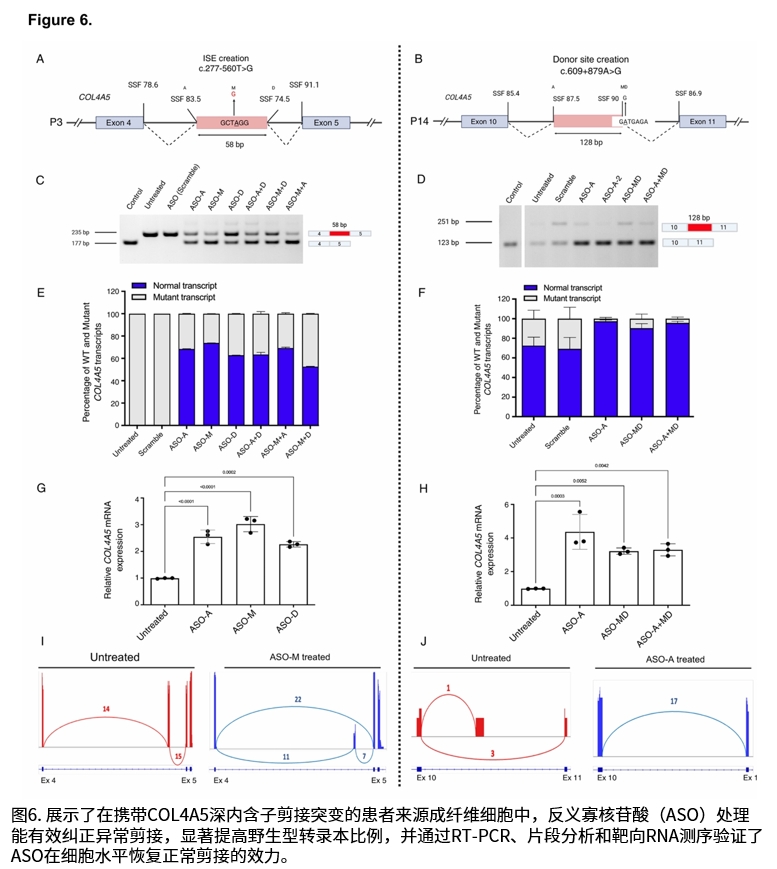
团队首先在携带COL4A5基因深内含子剪接突变的患者成纤维细胞中,筛选出能够有效纠正异常剪接的ASO。随后,通过CRISPR-Cas9技术将两种患者突变(c.277-560T>G和c.609+879A>G)引入对照iPSC系,构建了严重型和中等型XLAS肾类器官模型。
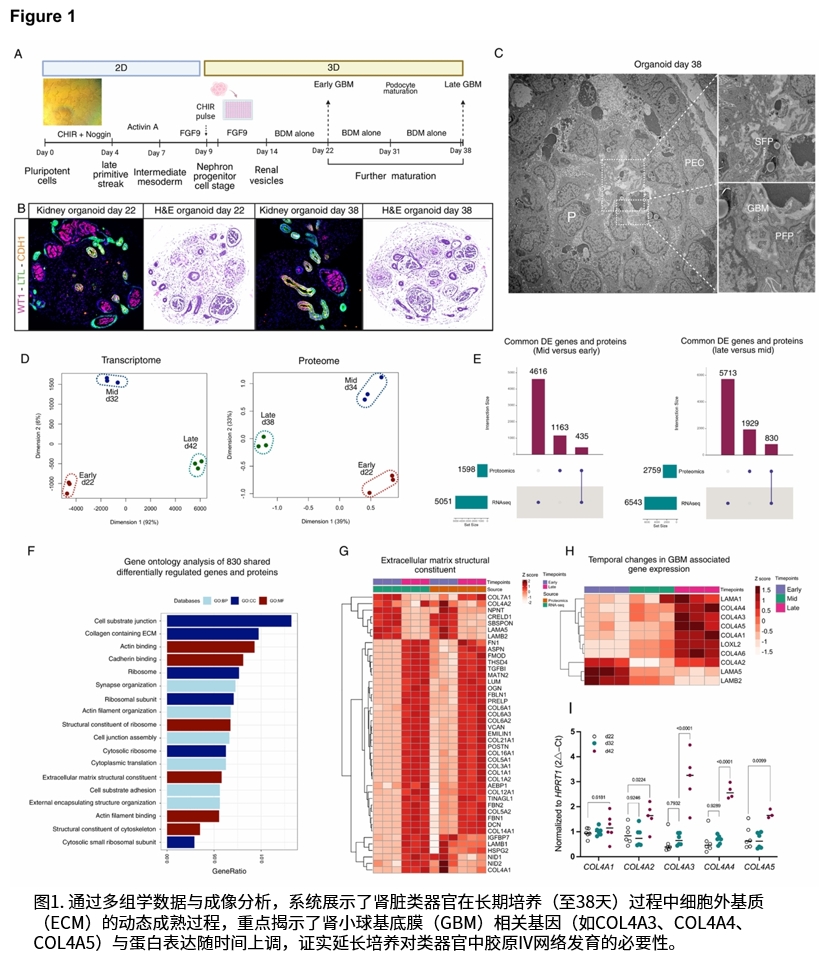
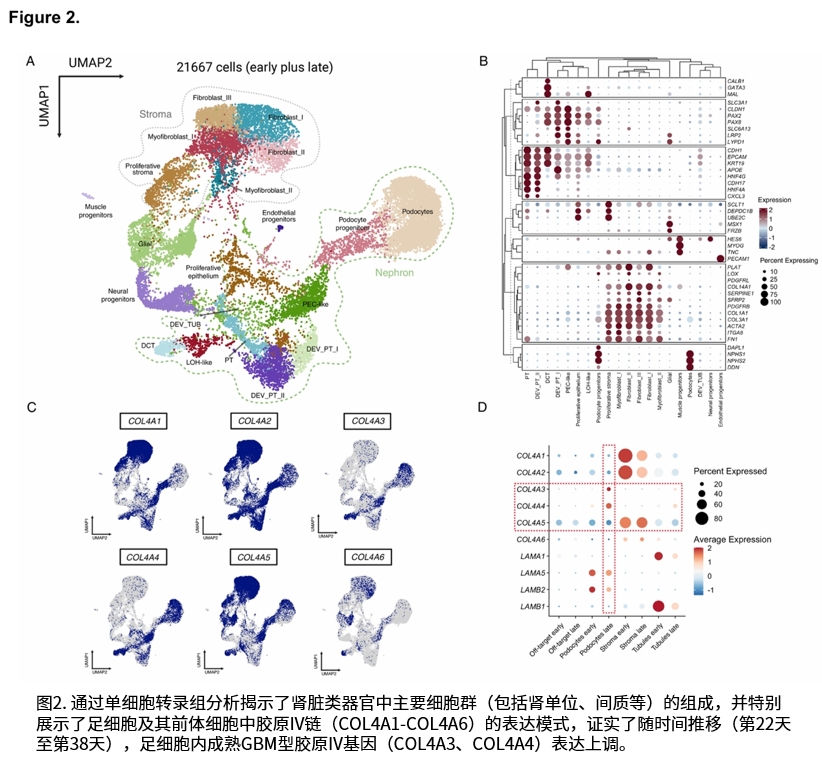
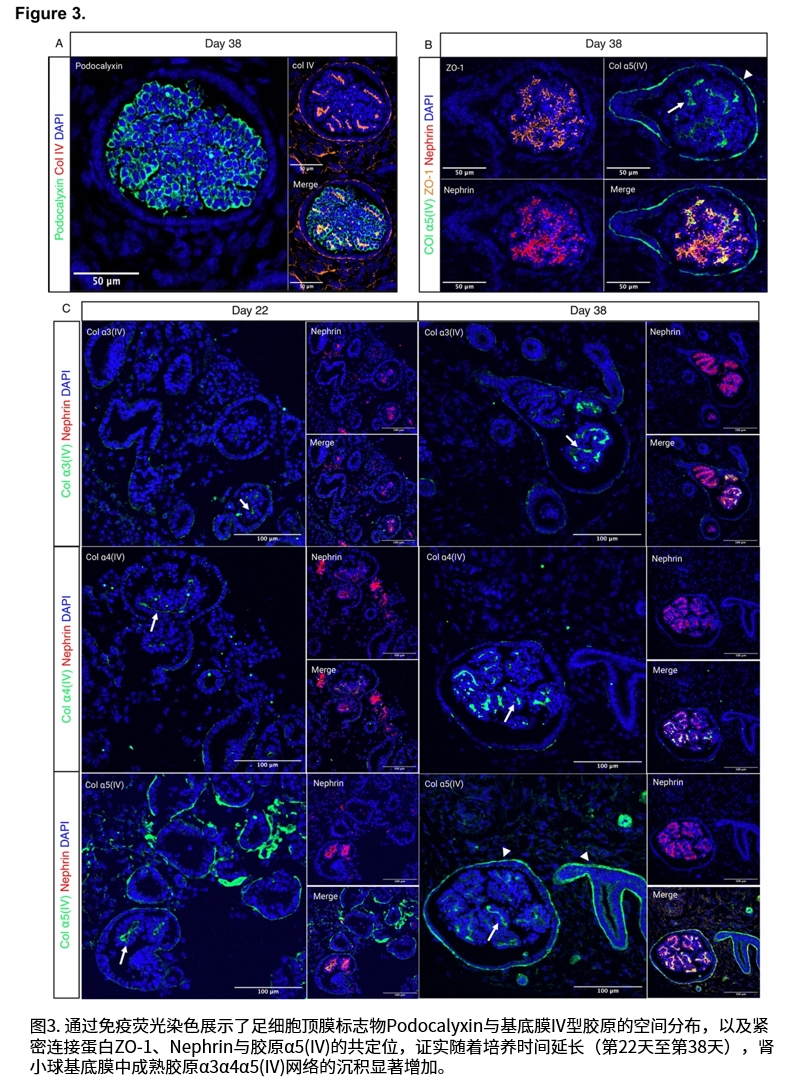
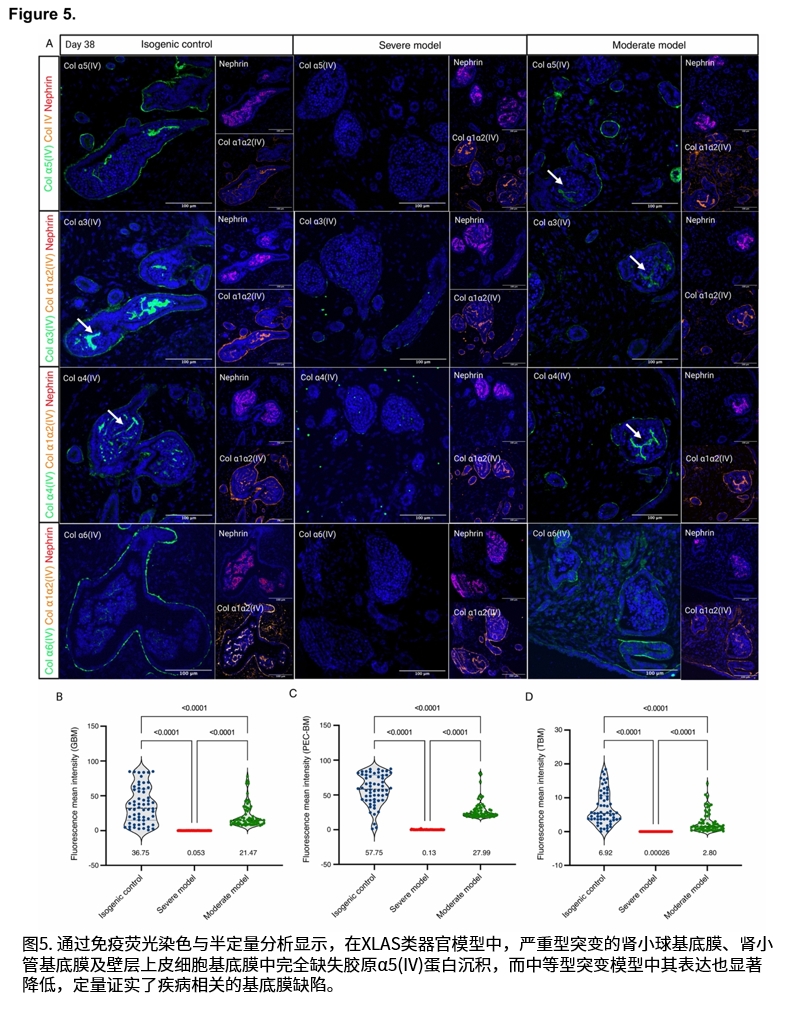
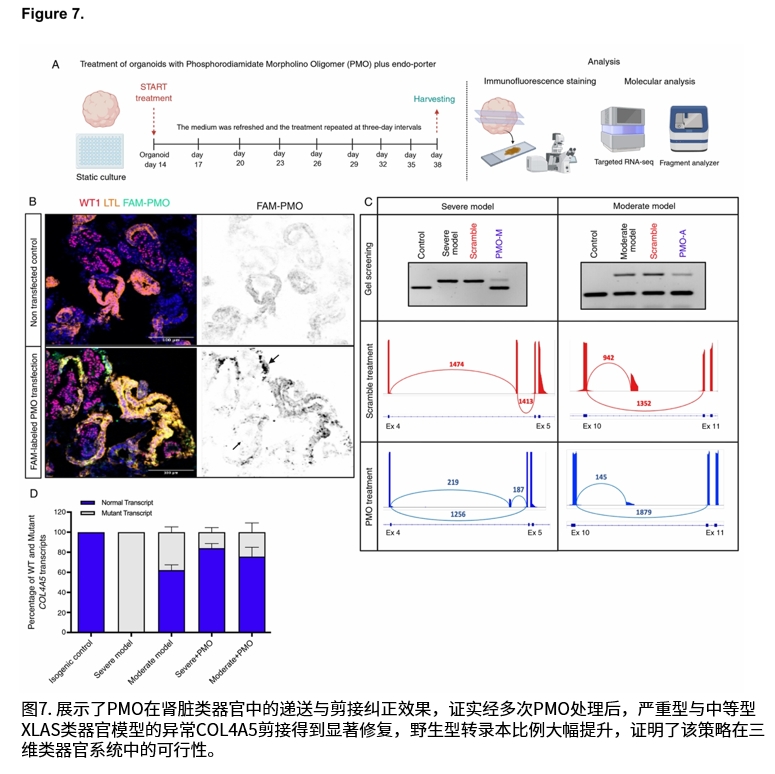
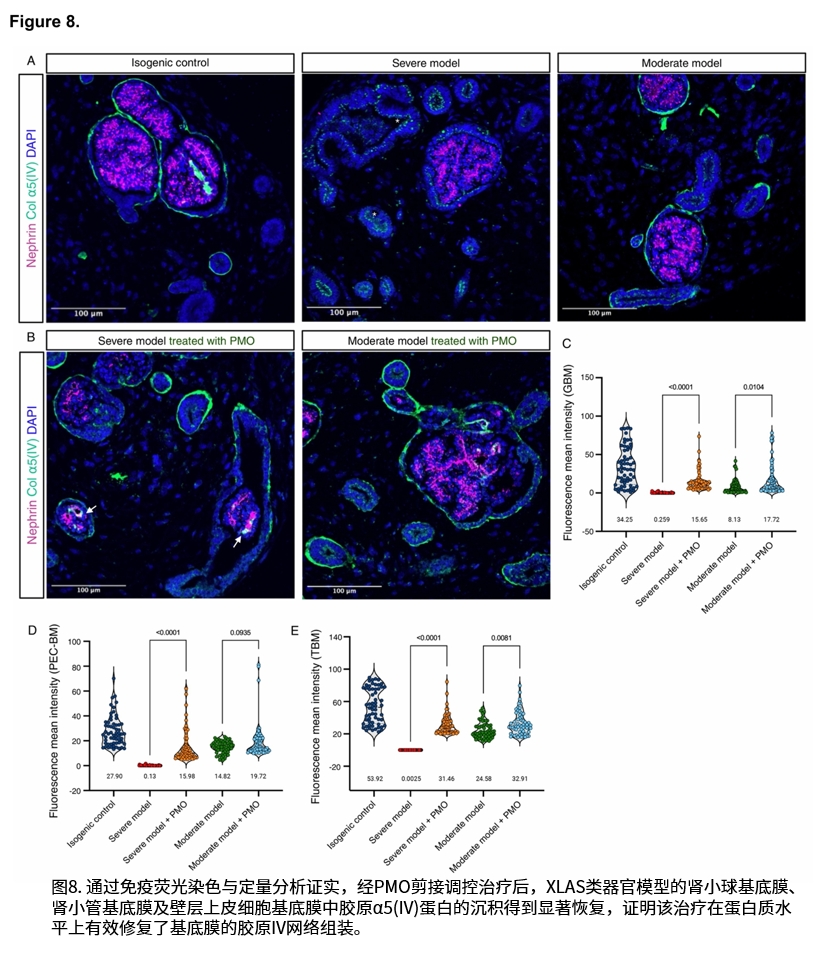
研究证实,延长培养时间(至38天)对于肾脏类器官中细胞外基质成熟,特别是胶原IV型网络的发育至关重要。在疾病模型中,免疫荧光染色显示胶原α3(IV)、α4(IV)、α5(IV)和α6(IV)链在基底膜中缺失或显著减少。经磷酰二胺吗啉寡核苷酸(PMO)处理后,两种模型的异常剪接得到有效纠正,野生型转录本比例显著升高,并在蛋白质水平上观察到胶原α5(IV)链在肾小球基底膜、肾小管基底膜及壁层上皮细胞基底膜中的沉积恢复。
该工作建立了一个结合患者原代细胞和肾脏类器官的两步临床前评估体系,为XLAS及其他由剪接缺陷引起的遗传性肾病的疗法开发提供了可扩展的研究模型。