
近日,发表于Biomedicine & Pharmacotherapy的《Leveraging multi-organ models for drug combination therapy safety》研究,建立了一个包含肝脏、心脏和肾脏模型的多器官体外毒性评估平台。该研究使用患者来源的肾脏类器官、可分化肝细胞和工程化心肌细胞等模型,对两种针对肾细胞癌的优化药物组合进行了系统性毒性评估。研究发现,较复杂的体外模型能够检测到传统模型中未能观察到的毒性特征。
肿瘤治疗已进入联合疗法时代,药物间的相互作用可能导致全身性毒性,传统基于动物模型或单一器官细胞系的评价体系存在物种差异大、通量低、生理相关性不足等局限。虽然治疗引导的多药物优化(TGMO)等技术已能筛选出具有协同抗肿瘤活性的药物组合,但其安全性初筛通常仅依赖于来源组织的非癌变细胞系(如HEK293T),未能全面评估其对肝、心、肾等主要毒性靶器官的潜在影响。因此,开发一种能够在临床前阶段评估药物组合多器官毒性的体外平台具有重要价值。
1.模型构建:
肾脏模型:采用新鲜分离的患者来源肾脏类器官(PHK28),培养于基质胶中。
肝脏模型:使用HepaRG细胞,分为未分化状态(ndHepaRG)、二维分化状态(2D dHepaRG)及三维球体分化状态(3D dHepaRG)。
心脏模型:采用H9c2(2-1)细胞,通过不同浓度的全反式视黄酸(RA)诱导分化为心肌样细胞(dH9c2(2-1))。
2.药物处理:
测试两种TGMO平台优化的药物组合:C2(埃罗替尼HCl、达沙替尼、tubacin、tacedinaline)与REMP(埃罗替尼HCl、小白菊内酯、盐酸二甲双胍、RAPTA-C)。
3.毒性评估指标:
细胞活力:采用CellTiter-Glo®(CTG)法检测ATP水平。
肝毒性标志物:在3D dHepaRG模型中,检测ALT、AST及LDH活性。
形态学观察:通过高内涵成像系统记录形态变化。
4.数据分析:
毒性阈值依据ISO 10993-5:2009标准设定,统计学差异采用单因素方差分析(ANOVA)进行检验。
1.肾脏毒性评估:在患者来源肾脏类器官中,C2组合导致细胞活力下降至50.4%,REMP组合引起活力下降至74.7%。
2.肝脏毒性评估:在3D球体模型中,C2组合的毒性最强(活力23.2%),且LDH释放增加。REMP组合在所有肝脏模型中未显示强肝毒性。
3.心脏毒性评估:C2组合在未分化及分化的H9c2(2-1)模型中均表现出心脏毒性(活力66.1%-83.7%)。
4.模型比较分析:相较于未分化细胞系,分化模型对测试组合表现出不同的响应模式。
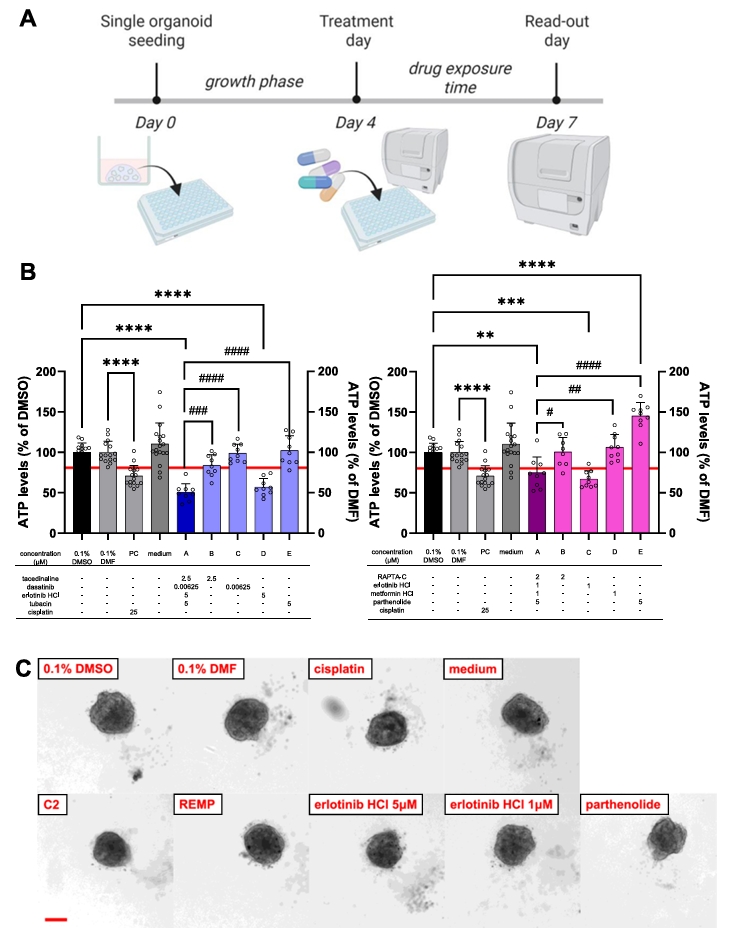
图1. 患者来源的肾脏类器官(PHK28)在药物处理后的安全性评估结果。通过ATP水平测定发现,C2药物组合导致细胞活力显著下降至50.4%,毒性强于阳性对照药物顺铂(70.7%),而REMP组合仅引起轻度活力下降(74.7%)。同时,形态学观察显示毒性反应与器官大小变化相关。
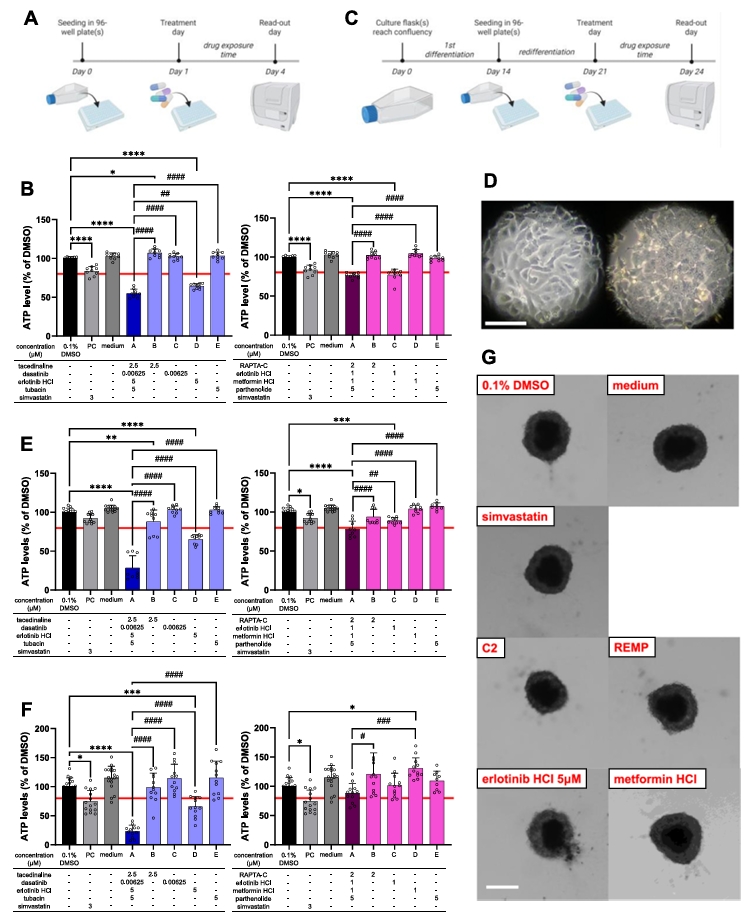
图2. 肝细胞模型中药物毒性评估的结果。该研究使用HepaRG细胞在不同分化状态(未分化、二维分化和三维球体分化)下评估C2和REMP药物组合的肝毒性。结果显示模型复杂度显著影响毒性检出:在三维分化球体模型中,C2组合显示出最强的肝毒性(细胞活力下降至23.2%),而REMP组合在所有模型中均未显示强肝毒性。形态学观察进一步证实了毒性反应与细胞结构变化的相关性。
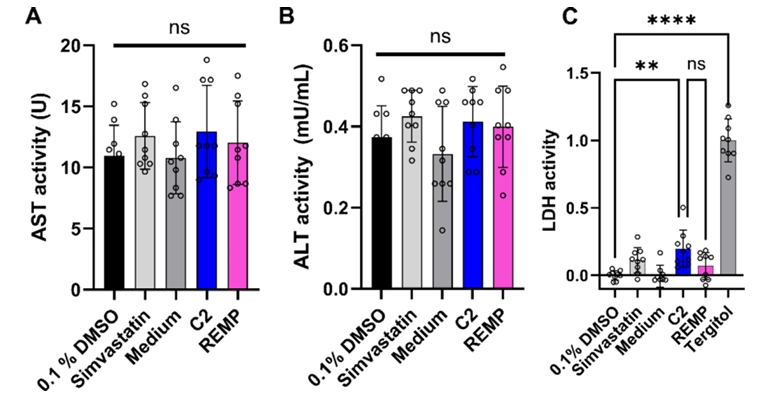
图3. 肝损伤标志物在3D分化的HepaRG细胞模型中的检测结果。通过对丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)和乳酸脱氢酶(LDH)活性的测定,发现只有C2药物组合处理组的LDH活性显著增加,而ALT和AST活性在各处理组间无统计学差异。这一结果表明在该模型中,C2组合可能主要通过影响细胞膜完整性而非典型的肝脏酶泄漏途径引发肝毒性。
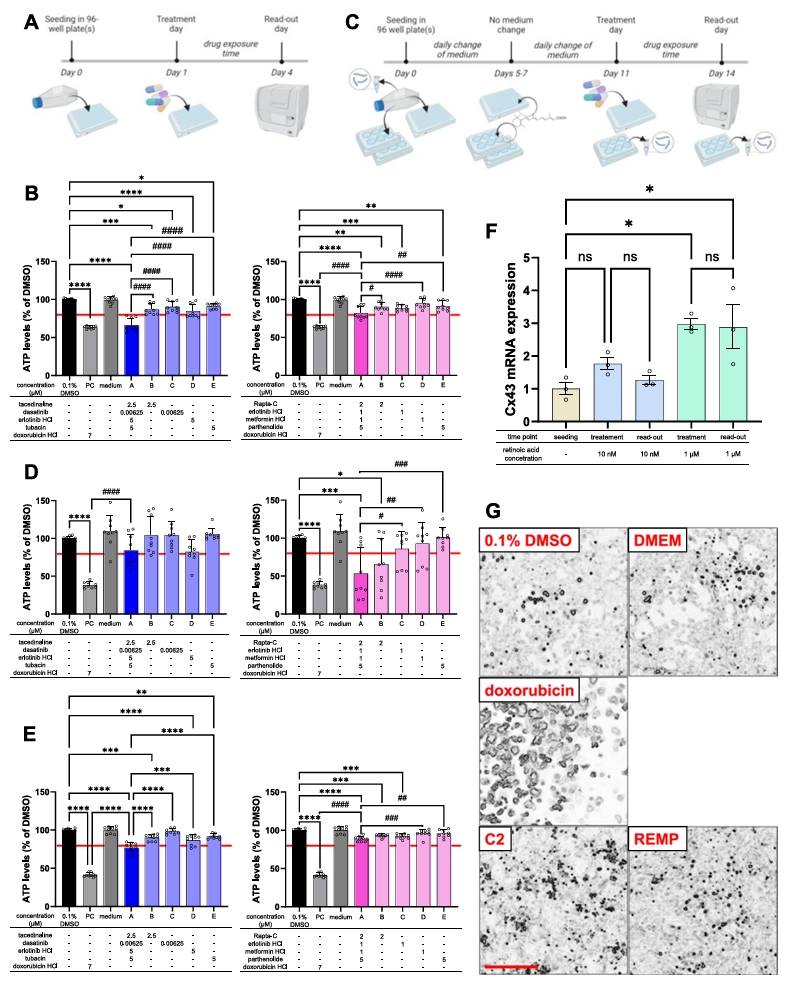
图4. 心脏模型(H9c2(2-1)细胞)中药物毒性评估的结果。研究发现C2和REMP药物组合均在不同分化状态的H9c2(2-1)细胞中表现出心脏毒性,其中C2组合的毒性效应更为显著。分化程度和视黄酸浓度均影响细胞对药物的敏感性,分化过程通过检测连接蛋白43(Cx43)表达水平进行验证。形态学观察进一步证实了药物处理导致的细胞形态变化与毒性反应的关联性。
本研究显示,用于药物组合初筛的简单细胞模型可能低估对特定器官的毒性风险。患者来源的肾脏类器官提供了更接近体内的毒性反应。分化状态是评估器官特异毒性的关键变量。
当前平台存在局限性,包括缺乏药物代谢与清除的动态模拟、无法评估免疫介导的毒性。未来方向包括与微流控器官芯片技术整合,纳入更多毒性靶器官模型。
本研究构建了一个多器官体外毒性筛选平台,能够识别联合用药方案在肝、心、肾等关键器官的潜在毒性。平台采用的差异化细胞模型提升了毒性预测的准确性。该平台可与现有的药物组合优化流程相结合,为肿瘤治疗策略提供工具。
该研究展示的多器官毒性评估平台通过整合不同器官的体外模型,能够对联合用药方案的毒性进行更全面的评估。患者来源的类器官和分化细胞模型比传统的二维细胞系更能反映毒性反应。尽管平台仍需进一步完善,但这一研究为药物开发过程中的安全性评估提供了技术支持。
参考文献:
Mieville V, Gubala J, Han S, Ota M, Andreu-Carbó M, Molica F, Benamran D, Kwak BR, Valerio M, Nowak-Sliwinska P. Leveraging multi-organ models for drug combination therapy safety. Biomed Pharmacother. 2025 Dec;193:118847

公司地址
深圳
广东省深圳市龙华区观澜银星智界2期A座11楼
广州
广东省广州和盛广场
武汉
湖北武汉光谷生物城
联系电话
商务支持
17276665437(李先生)
技术支持
18843183823(田先生)

